ゲノム編集による動物受精卵の遺伝子組み換え・遺伝子治療の簡便化に成功
ゲノム編集による動物受精卵の遺伝子組み換え・遺伝子治療の簡便化に成功
東京大学医科学研究所の中内啓光特任教授(スタンフォード大学教授兼任)、山口智之特任准教授、水野直彬特任研究員らの研究グループは、アデノ随伴ウイルスベクターとCRISPR/Cas9ゲノム編集により、動物胚に外来遺伝子を挿入する新たな技術の開発に成功した。
ゲノム編集技術による遺伝子挿入は、遺伝子改変動物を用いた基礎研究の基盤であるだけでなく、遺伝子疾患の治療にも有用な技術である。近年の技術的進歩により、ゲノム編集技術を受精卵段階で適用することが可能となったが、遺伝子破壊と異なり、遺伝子挿入には高度な手技が必要で、導入できる遺伝子の長さにも制限があった。高効率で簡便な細胞内への遺伝子導入法として、ウイルスベクターを用いた方法が知られているが、一般的な細胞と異なり、哺乳類受精卵は透明帯に保護されているため、適用することは困難と考えられてきた。
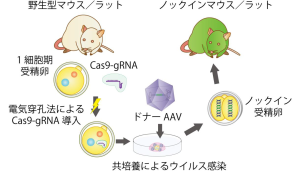 本研究グループは、アデノ随伴ウイルス(AAV)が一般的なウイルスベクターと異なり、さまざまな哺乳類受精卵に対し、透明帯を通過して感染しうることを発見した。この特性を利用して、電気穿孔法によるCRISPR/Cas9ゲノム編集に、アデノ随伴ウイルスベクターによるドナーDNAの導入を組み合わせることで、特殊な機材・技術を用いることなく、受精卵段階で長鎖外来遺伝子をノックインする事に成功した。さらに同手法を用いて、免疫不全モデル動物であるヌードマウスの遺伝子治療にも成功した。
本研究グループは、アデノ随伴ウイルス(AAV)が一般的なウイルスベクターと異なり、さまざまな哺乳類受精卵に対し、透明帯を通過して感染しうることを発見した。この特性を利用して、電気穿孔法によるCRISPR/Cas9ゲノム編集に、アデノ随伴ウイルスベクターによるドナーDNAの導入を組み合わせることで、特殊な機材・技術を用いることなく、受精卵段階で長鎖外来遺伝子をノックインする事に成功した。さらに同手法を用いて、免疫不全モデル動物であるヌードマウスの遺伝子治療にも成功した。
本手法はマウス・ラットだけでなく、牛をはじめとする家畜など、広範な哺乳類に適用可能と考えられ、生物学・医学研究において基盤的な技術となりうると共に、遺伝子疾患をもつ家畜等において遺伝子治療を可能とすると期待される。
本研究成果は 2018年11月2日付の科学雑誌 「iScience」のオンライン版に掲載された。
