| 発表のポイント |
|---|
|
概要
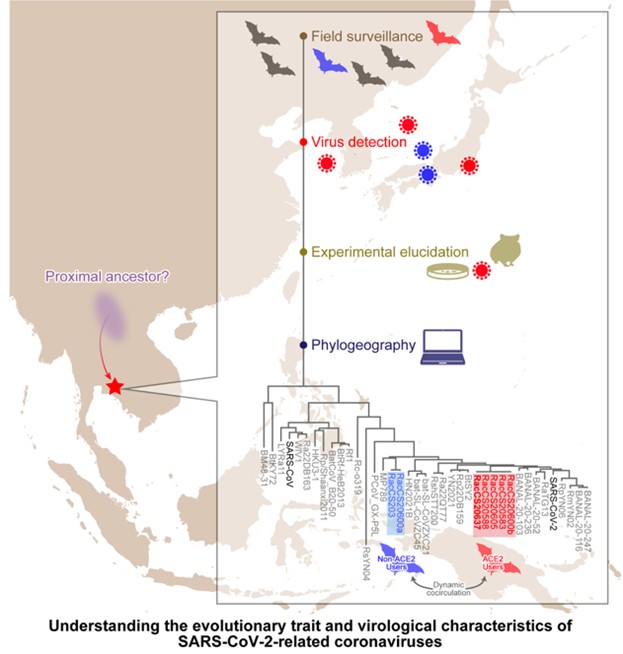
東京大学医科学研究所システムウイルス学分野の佐藤佳教授が主宰する研究コンソーシアム「The Genotype to Phenotype Japan (G2P-Japan) Consortium」(注1)は、タイ・チュラロンコン大学らの研究チームと共同し、新たな国際共同研究コンソーシアム「The Genotype to Phenotype Asia (G2P-Asia) Consortium」(注2)を結成しました。本研究では、タイに生息する野生のキクガシラコウモリ(Rhinolophus acuminatus)から新たに新型コロナウイルス(SARS-CoV-2)に系統学的に近縁なコロナウイルスを多数同定し、そのひとつのウイルス学的性状を、培養細胞や実験動物を用いたウイルス実験から明らかにしました。さらに、地理情報を含めた系統解析(地理系統解析)から、東南アジア地域におけるSARS-CoV-2関連コウモリコロナウイルスの時空間的動態を明らかにしました。本研究成果は2026年5月6日付で、米国科学雑誌「Cell」オンライン版で公開されました。
発表内容
2019年に突如出現した新型コロナウイルス(SARS-CoV-2)は、瞬く間に全世界に拡がりパンデミック(世界的大流行)を引き起こしました。近年、SARS-CoV-2と系統学的に近縁なウイルス(SARS-CoV-2関連コロナウイルス)(注3)が、野生のコウモリから発見されています。これらの知見は、元々コウモリが保有していたウイルスが、ヒトに異種間伝播(注4)することでSARS-CoV-2が誕生したことを示唆しています。すなわち、SARS-CoV-2関連ウイルスを探索・同定し、そのウイルスがどのようなウイルス学的性状を持つのかを明らかにすることは、将来起こり得る新たなパンデミックに備える上で重要な科学的知見となります。最近のウイルス調査から、東南アジア地域に生息する野生のコウモリからいくつかのSARS-CoV-2関連コロナウイルスが検出されています(Wacharapluesadee et al., Nature Commun., 2021; Zhou et al., Cell, 2021; Delaune et al., Nature Commun., 2021)。本研究では、タイ・チュラロンコン大学らとの共同研究により、タイに生息するコウモリを対象としたウイルス調査を行いました。その結果、以前に検出されていた、ヒトの感染受容体であるアンジオテンシン変換酵素2(ACE2)を利用できないSARS-CoV-2関連コロナウイルス(図1, Clade A)とは異なる、新たなSARS-CoV-2関連コロナウイルス(図1, Clade B)を新たに複数同定しました。重要なことに、このClade Bのウイルスは、自身の複製に必要なタンパク質をコードする領域(RdRp)はClade Aと類似していた一方で(図1左)、ウイルス感染に重要な、スパイクタンパク質(注5)の受容体結合ドメイン(RBD)(注6)は、ヒトのACE2を利用可能なSARS-CoV-2などに近縁でした(図1右)。この結果は、Clade Bのウイルスは、Clade Aとは異なり、ヒトACE2を利用できる、すなわち、ヒトに感染できる能力を持っている可能性を示唆しています。
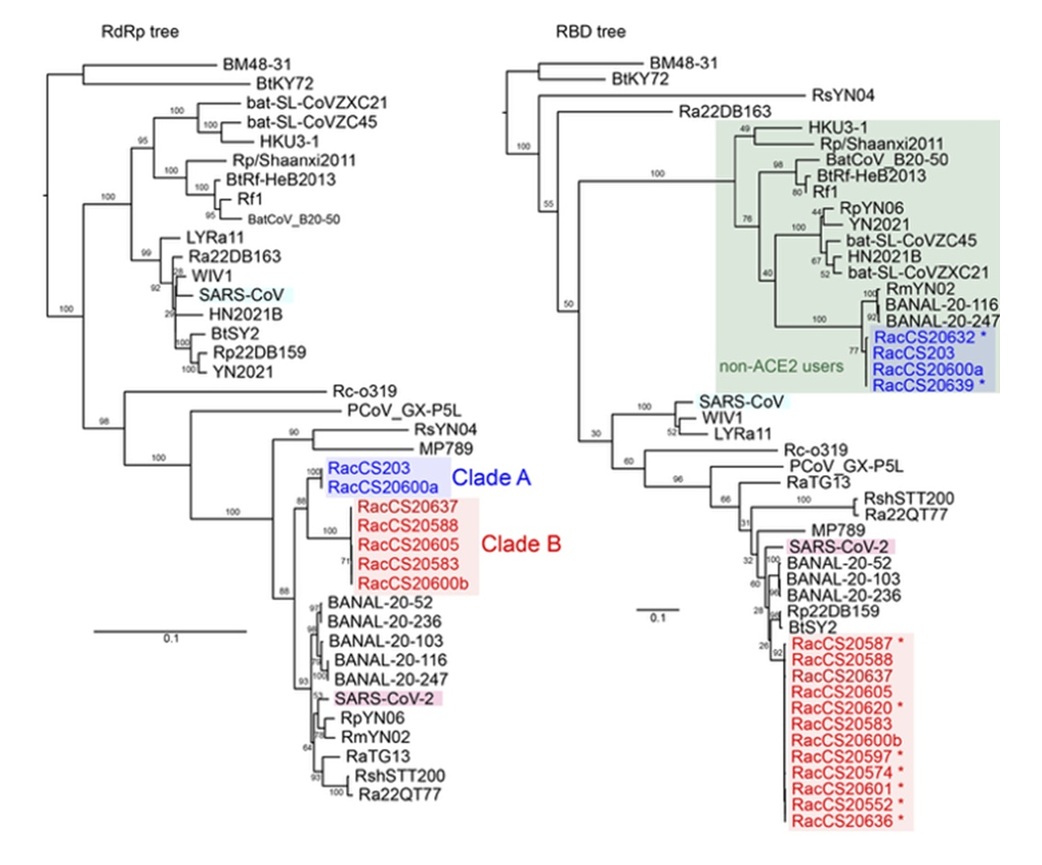
SARS-CoV-2、および、タイで新たに同定された新型コロナウイルスに近縁なコウモリ由来コロナウイルスを含むSARS-CoV-2関連ウイルスの分子系統樹。RdRp領域(左)とRBD領域(右)における系統樹をそれぞれ示す。
この可能性を検証するために、Clade Bのひとつのウイルス(以下、RacCS20637)のスパイクタンパク質の受容体結合ドメイン(RBD)とヒトACE2タンパク質を用いて、これらのタンパク質の結合力を調べました。その結果、RacCS20637のRBDは、SARS-CoV-2のRBDと比較して、ヒトACE2タンパク質に対する結合力が高いことがわかりました。この結果についてさらに詳細に調べるために、クライオ電子顕微鏡法(注7)を用いてRacCS20637のRBDとヒトACE2のタンパク質複合体の構造を明らかにしました(図2)。構造解析から、RacCS20637のRBD内の477番目のアスパラギン(N477)および498番目のヒスチジン(H498)がより安定的にヒトACE2に結合することで、SARS-CoV-2のRBDと比べて、RacCS20637のRBDがより強くヒトACE2に結合していることがわかりました(図2)。
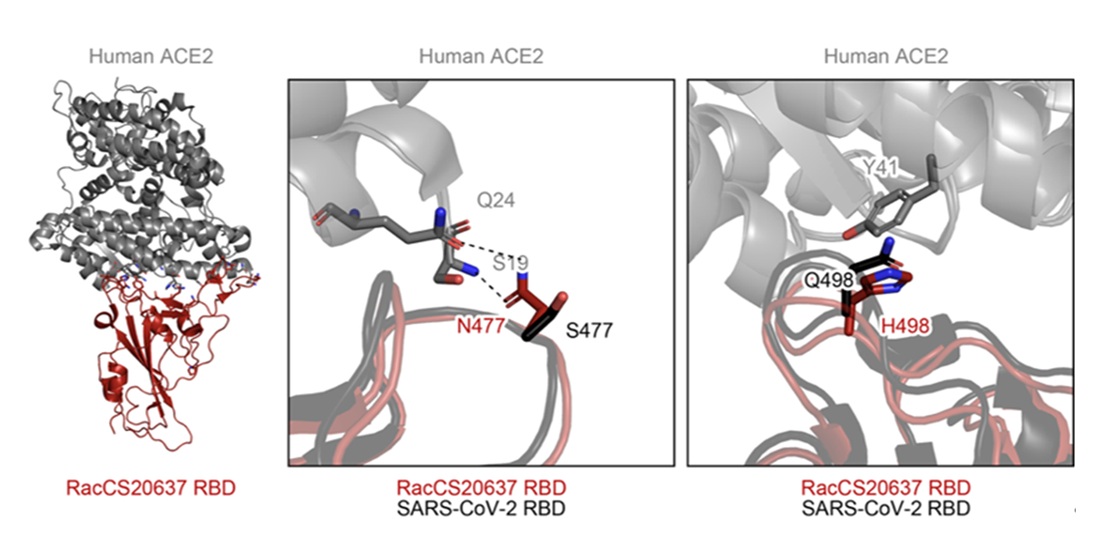
RacCS20637スパイクタンパク質の受容体結合ドメイン(RacCS20637 RBD:赤)とヒトACE2感染受容体(Human ACE2:灰色)の複合体構造(左)。両タンパク質の結合に重要な箇所を拡大した(中央および右)。
文部科学省の大臣確認実験の承認、および、東京大学研究用微生物安全委員会の承認の下で、リバースジェネティクス法(注8)によって、RacCS20637の全長ウイルス配列からウイルスを人工合成することに成功しました。なお、SARS-CoV-2とRacCS20637のウイルス人工合成、および、これらのウイルスを使用したすべての実験は、東京大学医科学研究所のバイオセーフティーレベル3の実験室で実施されました。
作出したウイルスを用い、まずは、RacCS20637に対する既存のワクチンや抗ウイルス薬の効果を検証しました。新型コロナウイルス感染症(COVID-19)ワクチンを3回接種した人由来の血清を用いた感染中和試験の結果、RacCS20637はSARS-CoV-2よりも中和されやすいことがわかりました(図4)。加えて、COVID-19の治療等に用いられるレムデシビルやニルマトレルビルなどの医療用抗ウイルス薬についても、SARS-CoV-2と同様に、RacCS20637に対しても有効性が確認されました。以上のことから、将来Clade Bのウイルスによる新たな感染症が発生した際には、既存のワクチンや治療薬が有効であることが示唆されました。

レポーターウイルス(注9)を用いた感染中和試験。COVID-19ワクチンを3回接種した人由来の血清を用いて、ウイルス感染中和試験を実施した。50%感染中和力価は、血清がウイルスの感染を中和する力を示しており、値が大きいほど中和能力が高いことを示している。
次に、RacCS20637のヒト細胞におけるウイルス増殖能を調べるために、ヒト由来の鼻腔上皮細胞、気道上皮細胞、および、肺胞上皮細胞を用いたウイルス感染実験を行いました。SARS-CoV-2はこれらの細胞で効率よく増殖しましたが(図3、黒線)、RacCS20637はヒト肺胞上皮細胞ではSARS-CoV-2よりも低い増殖動態を示し、その他の2種類の細胞ではウイルス増殖が認められませんでした(図3、赤線)。これらの結果は、RacCS20637は、SARS-CoV-2と比べ、感染受容体であるACE2には効率よく結合できるものの、細胞に感染した後の増殖力は弱いことを意味しています。さらに、RacCS20637の感染による病態を調べるため、ハムスターを用いた感染実験を実施しました。細胞での感染実験の結果と一致して、SARS-CoV-2感染ハムスターでは一過性の呼吸機能の低下や気道・肺組織におけるウイルス増殖が確認されましたが、RacCS20637感染ハムスターではそのような病態は認められませんでした。このことは、RacCS20637の病原性は、SARS-CoV-2よりも著しく低いことを示唆しています。
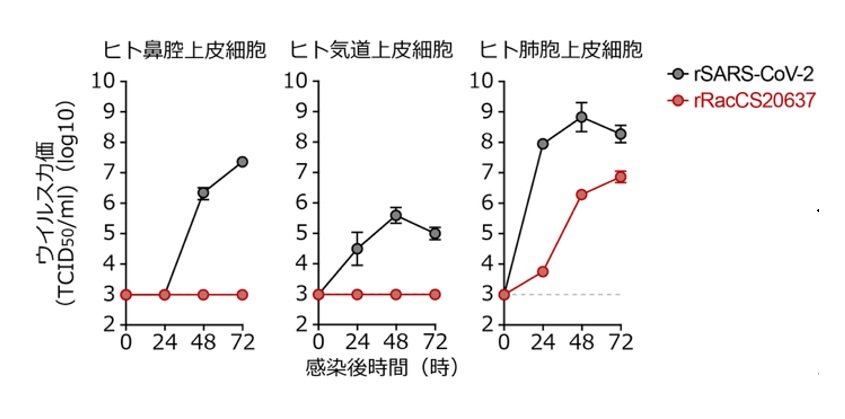
細胞におけるウイルス増殖曲線。SARS-CoV-2、および、RacCS20637のウイルス増殖能を、ヒト由来鼻腔上皮細胞(左)、気道上皮細胞(中央)、肺胞上皮細胞(右)を用いて調べた。縦軸はウイルス力価を示しており、値が大きいほどウイルスが増殖していることを示している。点線は検出限界を示す。
最後に、タイを含む東南アジアのインドシナ半島における、SARS-CoV-2関連ウイルスの時空間的動態を、系統地理解析(注10)によって調べました。まず、Clade Bのウイルスゲノム配列のさまざまな領域で組換えを起こしていることがわかりました。それぞれの組換え部位の間にあたる領域(非組換え領域、NRR)について地理情報を合わせた解析の結果、Clade Bのウイルスゲノムは、インドシナ半島において大規模に移動していること、また、その移動パターンはNRRの領域によって異なることがわかりました(図5)。このことは、東南アジア地域において、SARS-CoV-2関連コロナウイルスが複雑に移動し、その結果、多様なウイルスの出現に繋がっている可能性を示唆しています。
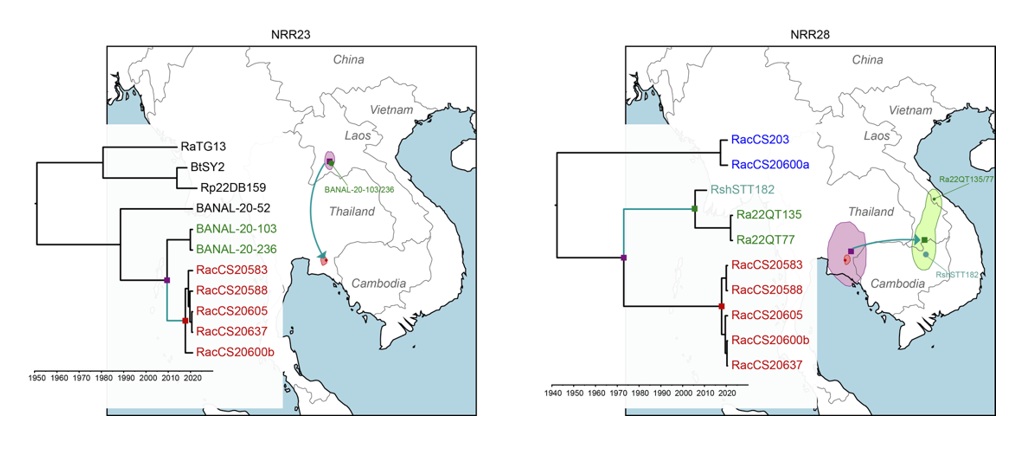
本研究で同定したウイルスを含む、SARS-CoV-2関連コロナウイルスの時間系統樹と推定された拡散経路。ゲノムの組換え領域ごとに、異なる時間軸・経路で拡散してきたことを示している。
本研究では、研究コンソーシアム「The Genotype to Phenotype Japan (G2P-Japan) Consortium」を、アジア諸国の研究チームとの国際共同研究コンソーシアム「The Genotype to Phenotype Asia (G2P-Asia) Consortium」へと発展的に展開しました。G2P-Japan、およびG2P-Asiaは、「次のパンデミック」に備える体制構築に向けた基礎ウイルス学研究を展開しています。特に、本研究のように、SARS-CoV-2関連コロナウイルスが多数検出されている東南アジア地域を中心に、リスクのあるウイルスを調査・同定し、そのウイルス学的性状を実験的に明らかにするための研究を推進しています。このような研究を通して、「次のパンデミック」が起こる前に、より良い感染症対策体制が整備されるために必要な科学的知見を発見し、世界に共有するための研究を推進します。なお、本研究は、東京大学医科学研究所における動物実験委員会の審査を受け、東京大学が定めた動物実験実施規則等(承認番号: A2024IMS067)に則り実施されました。
発表者・研究者等情報
東京大学
医科学研究所 感染・免疫部門 システムウイルス学分野
佐藤 佳 教授
Wilaiporn Saikruang 特任研究員
Spyros Lytras 特任研究員(研究当時)
瓜生 慧也 特任研究員
Alfredo Hinay Jr. 特任研究員(研究当時)
現:近畿大学医学部
郭 子毅 特任研究員
Arnon Plianchaisuk 特任研究員
陳 犖 特任研究員
大学院医学系研究科 病因・病理学専攻
Ananporn Supataragul 博士課程
小杉 優介 博士課程(研究当時)
藤田 滋 博士課程(研究当時)
大学院新領域創成科学研究科 メディカル情報生命専攻
Maximilian Stanley Yo 修士課程(研究当時)
研究コンソーシアム「The Genotype to Phenotype Japan (G2P-Japan) Consortium」
研究コンソーシアム「The Genotype to Phenotype Asia (G2P-Asia) Consortium」
医科学研究所 感染・免疫部門 システムウイルス学分野
佐藤 佳 教授
Wilaiporn Saikruang 特任研究員
Spyros Lytras 特任研究員(研究当時)
瓜生 慧也 特任研究員
Alfredo Hinay Jr. 特任研究員(研究当時)
現:近畿大学医学部
郭 子毅 特任研究員
Arnon Plianchaisuk 特任研究員
陳 犖 特任研究員
大学院医学系研究科 病因・病理学専攻
Ananporn Supataragul 博士課程
小杉 優介 博士課程(研究当時)
藤田 滋 博士課程(研究当時)
大学院新領域創成科学研究科 メディカル情報生命専攻
Maximilian Stanley Yo 修士課程(研究当時)
研究コンソーシアム「The Genotype to Phenotype Japan (G2P-Japan) Consortium」
研究コンソーシアム「The Genotype to Phenotype Asia (G2P-Asia) Consortium」
論文情報
雑誌名:Cell題 名:Virological characteristics of SARS-CoV-2-related coronaviruses dynamically circulating in Southeast Asia
著者名:Supaporn Wacharapluesadee#*, Wilaiporn Saikruang#, Spyros Lytras#, 松本 玄, 瓜生 慧也, Alfredo Hinay Jr., 郭 子毅, Khwankamon Rattanatumhi, Ananporn Supataragul, Sasiprapa Ninwattana, Nattakarn Thippamom, Tanawut Srisuk, Patarapol Maneeorn, Kirana Noradechanon, Prateep Duengkae, Nutthinee Sirichan, 小杉 優介, 藤田 滋, Maximilian Stanley Yo, 松長 遼, Bingjie Hu, Lianzhao Du, Lei Wang, 津田 真寿美, 小田 義崇, Hesham Nasser, 赤坂 浩明, 浅倉 弘幸, 長島 真美, 貞升 健志, 吉村 和久, 山本 佑樹, 永元 哲治, 朝倉 崇徳, 志甫谷 渉, 池田 輝政, 田中 伸哉, Hin Chu, 津本 浩平, 濡木 理, The Genotype to Phenotype Japan (G2P-Japan) Consortium, The Genotype to Phenotype Asia (G2P-Asia) Consortium, Arnon Plianchaisuk, 佐藤 佳*
(#Equal contribution; *Corresponding author)
DOI: 10.1016/j.cell.2026.04.019
URL: https://www.cell.com/cell/fulltext/S0092-8674(26)00454-X
研究助成
本研究は、佐藤佳教授に対する日本医療研究開発機構(AMED)「医療分野国際科学技術共同研究開発推進事業 先端国際共同研究推進プログラム(ASPIRE)(パンデミックの 5W1H を理解するための研究)」、AMED 先進的研究開発戦略センター(SCARDA)「ワクチン開発のための世界トップレベル研究開発拠点の形成事業(UTOPIA, 東京フラッグシップキャンパス(東京大学新世代感染症センター))」、AMED SCARDA「ワクチン・新規モダリティ研究開発事業(100日でワクチンを提供可能にする革新的ワクチン評価システムの構築)」、AMED「新興・再興感染症に対する革新的医薬品等開発推進研究事業(重点感染症の病態発現と宿主の遺伝的背景の関連解析とその実証)」、AMED「新興・再興感染症研究基盤創生事業(海外拠点活用研究領域)(ベトナムを拠点としたSARS-CoV-2関連コウモリコロナウイルスの探索とそのウイルス学的特性の解明)」、および日本学術振興会(JSPS)「国際共同研究加速基金(国際先導研究)(JP23K20041)(ポストコロナ時代を見据えた学際ウイルス学研究の推進)、JSPS「基盤研究A」(パンデミックウイルスの誕生原理の解明)、JSPS「二国間交流事業 共同研究・セミナー」(次のパンデミックリスクとなるコウモリコロナウイルスの探索と流行動態の解析)」などの支援の下で実施されました。
用語解説
(注1)研究コンソーシアム「The Genotype to Phenotype Japan (G2P-Japan) Consortium」東京大学医科学研究所 システムウイルス学分野の佐藤佳教授が主宰する研究チーム。日本国内の複数の若手研究者・研究室が参画し、研究の加速化のために共同で研究を推進している。現在では、イギリスを中心とした諸外国の研究チーム・コンソーシアムとの国際連携も進めている。
(注2)研究コンソーシアム「The Genotype to Phenotype Asia (G2P-Asia) Consortium」
東京大学医科学研究所 システムウイルス学分野の佐藤佳教授が主宰する研究チーム。特にアジア地域の諸外国との共同研究を円滑に進めるための研究コンソーシアム。
(注3)SARS-CoV-2関連コロナウイルス
SARS-CoV-2と系統的に近縁なウイルスのこと。中国およびカンボジア、ラオスといった東南アジアの国々の野生動物から多く発見されている。これらの国々から見つかるウイルスと比べるとSARS-CoV-2と遠縁ではあるが、日本のコウモリからもSARS-CoV-2関連コロナウイルスが検出、分離されている。
(注4)異種間伝播(スピルオーバー)
病原体が元来感染している自然宿主から、別の動物種に感染すること。
(注5)スパイクタンパク質
サルベコウイルスのエンベロープ表面に存在する膜タンパク質。細胞の受容体と結合し、膜融合を引き起こすことによって、ウイルスの侵入に大きく関与する。
(注6)受容体結合ドメイン(RBD)
スパイクタンパク質の中で、ACE2との結合に関与する領域。サルベコウイルス間でこの領域のアミノ酸配列は多様化しており、サルベコウイルスのACE2トロピズムが異なる要因の1つと考えられている。
(注7)クライオ電子顕微鏡法
タンパク質の構造解析手法の一つで、超低温に冷却したサンプルに対して電子線を照射することで構造を決定する手法。タンパク質の構造を高い分解能で観察できることから近年応用が進んでいる。
(注8)リバースジェネティクス法
遺伝子の塩基配列を基に、そこから作られるウイルスや生物の表現型(性質)を解析する手法。
(注9)レポーターウイルス
新型コロナウイルスのスパイクタンパク質を持たせたウイルス様粒子。細胞に一度感染できるが、増殖することはできない。感染を検出するためのレポーター遺伝子を持っている。
(注10)系統地理解析
生物やウイルスの遺伝的系統と地理的分布の関連を解析する技術
問合せ先
<研究内容について>東京大学医科学研究所 感染・免疫部門 システムウイルス学分野
教授 佐藤 佳(さとう けい)
https://www.ims.u-tokyo.ac.jp/imsut/jp/lab/ggclink/section04.html
<機関窓口>
東京大学医科学研究所 プロジェクトコーディネーター室(広報)
https://www.ims.u-tokyo.ac.jp/