| 発表のポイント |
|---|
|
概要
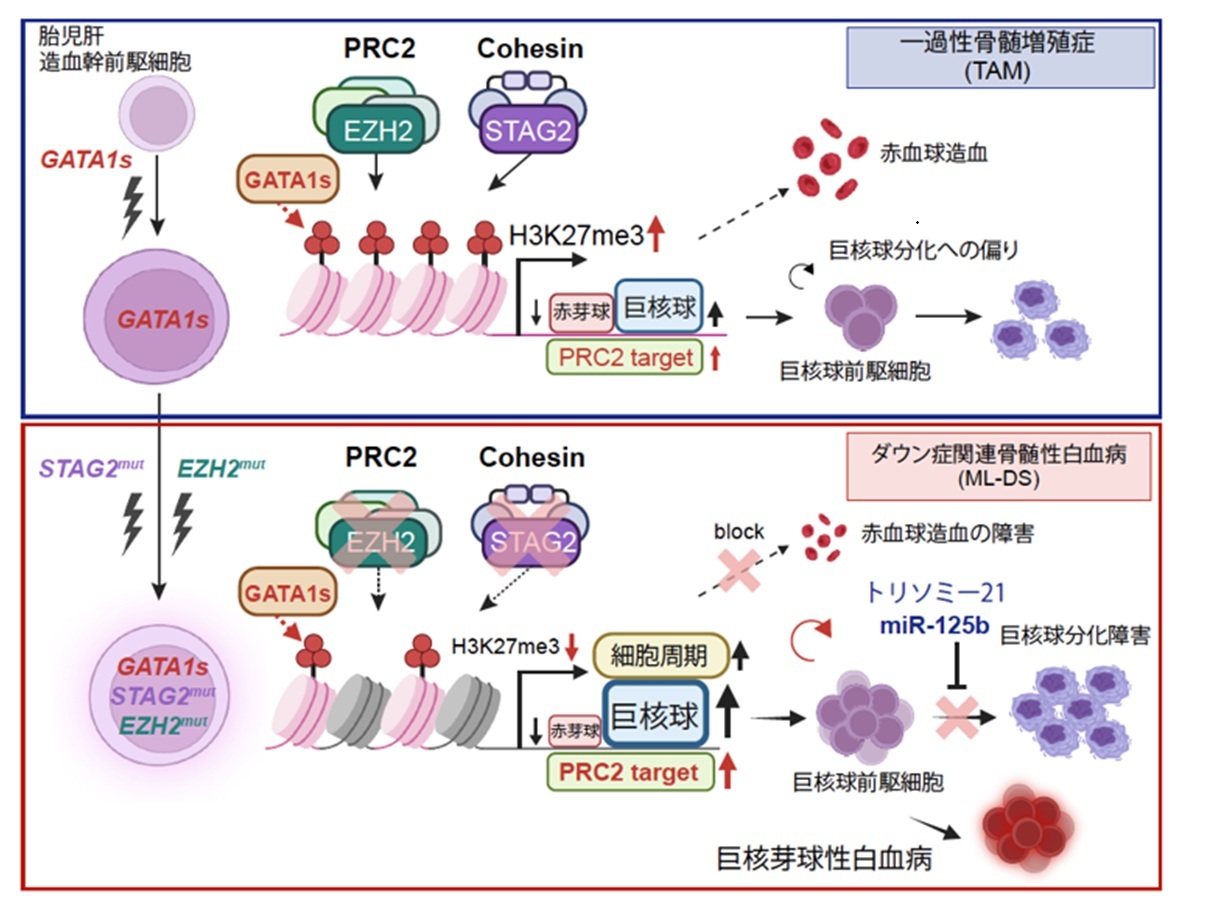
東京大学医科学研究所附属幹細胞治療研究センター幹細胞分子医学分野の岩間厚志教授と鈴木雄太郎特任研究員らの研究グループは、弘前大学大学院医学研究科地域医療学講座の伊藤悦郎特任教授および京都大学医学研究科腫瘍生物学講座の小川誠司教授らの研究グループとともに、ダウン症関連骨髄性白血病の発症に重要であると考えられるSTAG2およびEZH2遺伝子異常が、どのように病態形成に関与しているのかを明らかにしました。ダウン症候群(注1)では、新生児期に一過性骨髄増殖症(TAM:注2)という血液の中に異常な血液細胞が過剰に増加する病態を約10%の割合で発症することが知られています。この病態は名前の通り一過性のものであり、異常な血液細胞は自然に減少して正常化する一方、数年後に約20%の割合でダウン症関連骨髄性白血病(ML-DS:注3)を発症します。TAMの発症はGATA1遺伝子の短縮型変異であるGATA1s変異が原因であることがわかっていましたが、TAM細胞が付加的な遺伝子変異を獲得してML-DSへ進展するメカニズムは解明されていませんでした。
本研究成果は2026年4月8日付で、米国血液学会が発行する血液学専門誌「Blood」オンライン版に掲載されました。
発表内容
白血病は骨髄中の造血幹・前駆細胞に生じた遺伝子異常により、血液細胞が腫瘍化して増殖する血液のがんですが、ML-DSではエピジェネティックな変化(注4)を引き起こす遺伝子変異が多いことが知られています。ML-DS症例(203例)を対象に遺伝子変異プロファイルを解析したところ、コヒーシン(注5)遺伝子およびポリコーム複合体2(Polycomb Repressive Complex, PRC2:注6)遺伝子の変異が約半数の症例でみられ、さらに全体の約14%ではこの2種類の変異が重複して存在することがわかりました(図1)。
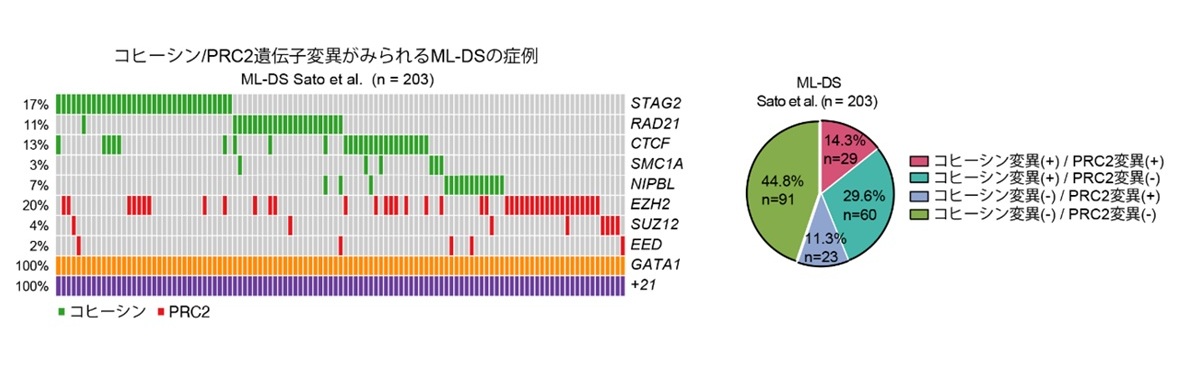
ダウン症候群の小児期にみられる特徴的な骨髄性白血病(ML-DS)では、GATA1変異が全例で陽性であるほか、約半数の症例でコヒーシン変異およびPRC2変異を有する。
本研究では、コヒーシンおよびPRC2遺伝子変異のML-DSの病態形成における役割を解明するため、それぞれの代表的な遺伝子であるStag2遺伝子およびEzh2遺伝子のノックアウトマウスを、Gata1s変異マウスと交配し、骨髄移植モデルを用いて解析を行いました。その結果、Gata1s/Stag2、Gata1s/Ezh2、Gata1s/Stag2/Ezh2遺伝子変異の組み合わせにおいて貧血や血球減少が観察され、骨髄中では赤血球の前駆細胞である赤芽球の減少と、血小板を作る巨核球の前駆細胞と巨核球の異常な増加を認めました。最終的にこれらのマウスは骨髄線維症(注7)を発症し、特にGata1s/Stag2/Ezh2三重変異のマウスでは最も顕著な線維化が見られました(図2a)。
さらに、ML-DSでは21トリソミー(21番染色体を3本有する状態)自体も病態の形成に重要であると考えられ、21番染色体上に位置し巨核球の分化に関わるマイクロRNA(注8)であるmiR-125b遺伝子をGata1s/Stag2/Ezh2変異マウス骨髄前駆細胞に高発現するモデルを作製したところ、ML-DSの一病型である急性巨核芽球性白血病(AMKL)を発症することを確認しました(図2b)。こうした所見は実際のヒトML-DS症例でみられるものと一致し、病態を模倣しているものと考えられました。
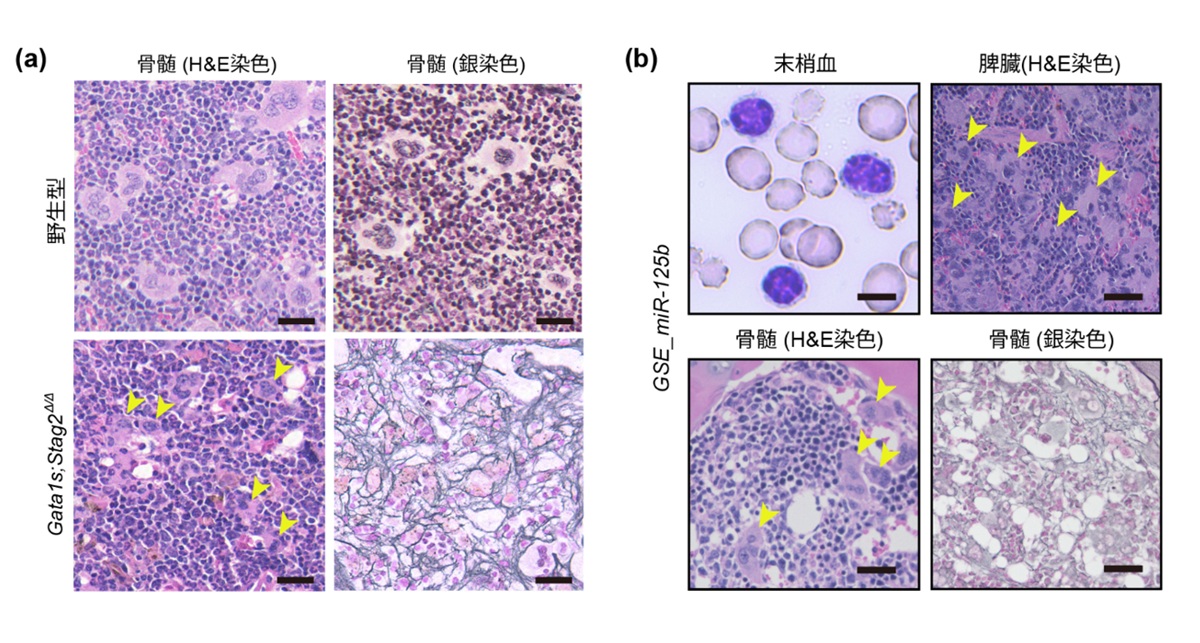
(a)Gata1s変異マウスとStag2およびEzh2ノックアウトマウスを交配すると異常な巨核球が増加し、骨髄線維症を発症する。(b)Gata1s/Stag2/Ezh2変異マウス骨髄細胞にmiR-125b遺伝子を導入すると、ML-DSの一病型である急性巨核芽球性白血病(AMKL)を発症する。
こうしたGATA1sとSTAG2、EZH2の異常がどのように白血病を引き起こすのかを解明するために、RNAシーケンス、ChIPシーケンス、ATACシーケンス、Hi-Cといった、次世代シーケンサーを用いた最新のエピジェネティック解析を統合的に行いました。興味深いことに、Gata1s/Stag2およびGata1s/Ezh2の巨核球前駆細胞では大部分で共通した遺伝子発現の変化がみられ、特に細胞周期に関連した遺伝子群や、PRC2複合体によって抑制的に制御される遺伝子群の発現が上昇していることがわかりました。
PRC2複合体は、遺伝子の発現を抑制するヒストン修飾であるH3K27me3を調節しており、この異常がさまざまな血液疾患の発症の原因となることが報告されています。当研究室ではこれまでPRC2複合体の構成因子であるEZH2の異常が、骨髄増殖性疾患のひとつである骨髄線維症の病態形成に関与していることを明らかにしてきました。今回、ML-DSにおいてEzh2をノックアウトすることで引き起こされるH3K27me3低下を介した遺伝子発現変化が、全く異なるコヒーシン複合体の構成遺伝子であるStag2のノックアウトによっても同様に観察され、病態形成において非常に似た変化を引き起こしていることが明らかになりました。コヒーシンの異常がPRC2複合体の部分的な機能不全を起こす興味深い現象は、ヒト白血病細胞株を用いた実験でも確認され、ML-DS患者サンプルを用いたシングルセルRNAシークエンス解析(注9)の結果からも、STAG2変異を持つML-DS細胞で、PRC2複合体により抑制される遺伝子群の発現が有意に上昇していることがわかりました(図3)。
続いてEzh2変異およびStag2変異に共通してみられる遺伝子の発現異常について、統合的な解析を行った結果、巨核球の分化を負に制御するチロシンキナーゼであるPtk2(注10)の発現がGata1s/Stag2およびGata1s/Ezh2細胞で共通して上昇していること、ML-DS患者サンプルのシングルセルRNAシークエンス解析でもPTK2の発現が上昇していることがわかり、病態の形成において重要な分子であると考えられました。さらに、PTK2の阻害剤であるデファクチニブ(注11)をヒトML-DS細胞株およびマウスML-DS細胞に投与したところ、増殖を有意に抑制し、巨核球への分化を促進することを認め、PTK2がML-DSの治療標的となる可能性が示されました。
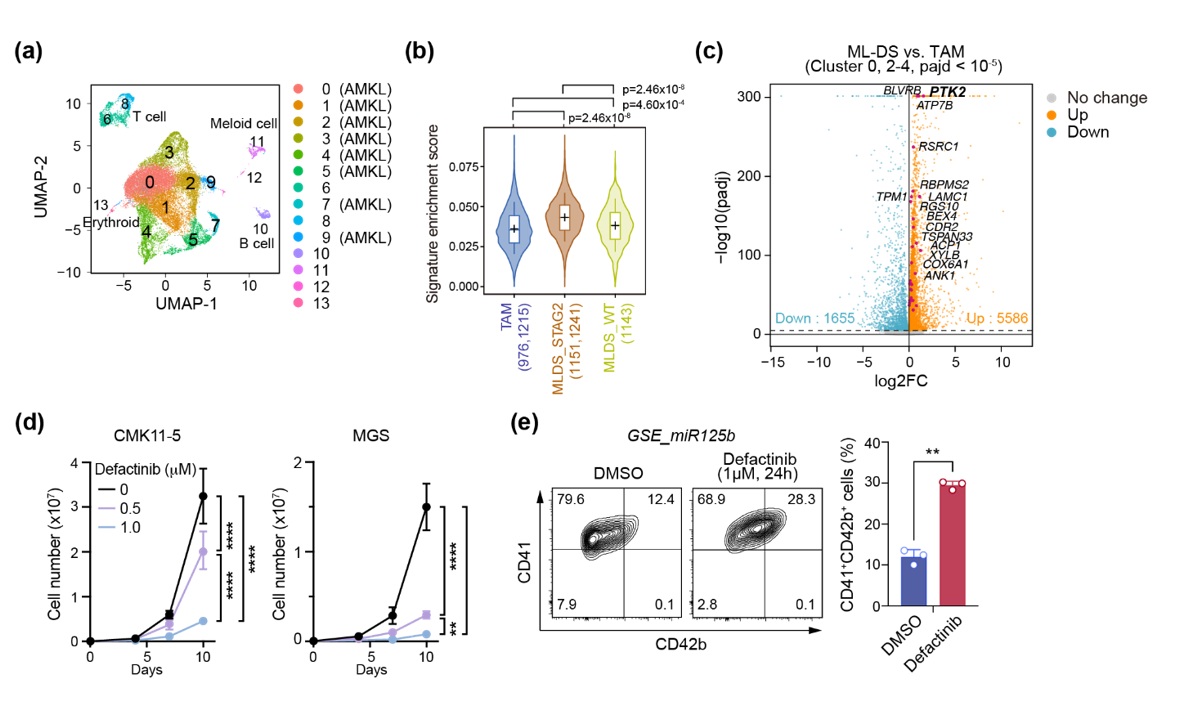
(a)ML-DS患者検体を用いたシングルセルRNAシークエンスのUMAP。クラスター0-5, 7, 9にAMKL細胞が分布する。(b)TAMと比較してSTAG2変異を有するML-DSにおいてPRC2複合体標的遺伝子の発現が上昇。(c)ML-DSとTAMにおける遺伝子の発現の違いを示すvolcano plot。ML-DSでPTK2の発現が有意に上昇する。(d)PTK2阻害剤であるデファクチニブは、2種類のヒトML-DS細胞株CMK11-5およびMGSの増殖を抑制する。(e)また、デファクチニブはGata1s/Stag2/Ezh2変異マウス胎仔肝の造血幹・前駆細胞にmiR-125b遺伝子を導入して形質転換させたML-DS細胞(GSE-miR125b細胞)の分化を促進し、巨核球分化マーカー(CD41、CD42b)を上昇させる。
本研究では、ML-DSの病態メカニズムにおけるPRC2複合体の機能異常の影響を初めて明らかにしました。ML-DSの病態を理解する上で、エピジェネティック制御異常は新たな発見であり、巨核球前駆細胞の分化に関わるPTK2の阻害など、ML-DSの新規治療戦略を考案する上で有用な情報を提示する研究成果といえます。
なお、本研究は、東京大学医科学研究所における動物実験委員会の審査を受け、東京大学が定めた動物実験実施規則等(承認番号: PS18-02)に則り実施されました。
発表者・研究者等情報
東京大学医科学研究所 附属幹細胞治療研究センター 幹細胞分子医学分野
岩間 厚志 教授
鈴木 雄太郎 特任研究員(研究当時)
岩間 厚志 教授
鈴木 雄太郎 特任研究員(研究当時)
論文情報
雑誌名:Blood(オンライン版)題 名:Polycomb repressive complex 2 insufficiency underlies myeloid leukemia in Down syndrome
著者名: Yutaro Suzuki, Yaeko Nakajima-Takagi, Motohiko Oshima, Yotaro Ochi, Akiho Saiki-Tsuchiya, Shuhei Koide, Takako Yokomizo, Shuhei Kurosawa, Ola Rizq, Ayana Kon, Satoru Miyano, Bahityar Rahmutulla, Atsushi Kaneda, Manabu Nakayama, Haruhiko Koseki, Eugene Yu, Tsutomu Toki, Etsuro Ito, Seishi Ogawa, Atsushi Iwama*(*責任著者)
DOI: 10.1182/blood.2025032083
URL: https://doi.org/10.1182/blood.2025032083
研究助成
本研究は、岩間厚志教授に対するJSPS「基盤研究(S)(課題番号:19H05653、24H00066)」、「新学術領域研究(研究領域提案型)(課題番号:19H05746)」、日本医療研究開発機構(AMED)「ASPIRE国際頭脳循環(課題番号:25jf0126013h0001)」などの助成金の支援により実施されました。
用語解説
(注1)ダウン症候群21番目の染色体が通常より1本多い[3本ある(トリソミー)]ことで生じる先天的な遺伝子疾患で、600~800人に1人の割合で発症するとされている。小児期における白血病の発症リスクが高く、臨床上の問題となる。
(注2)一過性骨髄増殖症(Transient Abnormal Myeloproliferative Disease, TAM)
新生児期にみられ、無治療でも数カ月で軽快する場合が多い。全例でGATA1s変異が陽性であり、発症の原因である。胎児期は肝臓が造血の中心であり、成人と異なる特殊な造血システムもTAMの病態形成に関係していると考えられている。
(注3)ダウン症関連骨髄性白血病(Myeloid Leukemia in Down Syndrome: ML-DS)
TAMに続発して小児期に発症する骨髄性白血病であるが、大部分の症例で巨核球系の分化障害と異常増殖を特徴とする急性巨核芽球性白血病(Acute Megakaryoblastic Leukemia, AMKL)を発症する。
(注4)エピジェネティックな変化
エピジェネティクスとは、細胞の遺伝情報(DNA)の塩基配列の変化を伴わない情報記憶と遺伝子発現調節のメカニズムのことを指す。エピジェネティクスを担う機構として、DNAメチル化やヒストン修飾、染色体の3次元構造などがある。
(注5)コヒーシン
SMC1, SMC3, RAD21, STAG1/2の4つのタンパク質で構成される複合体で、リング状の構造をとり、細胞分裂やDNA損傷の修復、更には遺伝子発現の調節など、多彩な機能をもつことが知られている。コヒーシン遺伝子は、これら4つのタンパク質のいずれかをコードする遺伝子を指す。
(注6)ポリコーム複合体(Polycomb Repressive Complex:PRC)
遺伝子の転写を抑制するヒストン修飾複合体であり、PRC1とPRC2の2種類に大別される。PRC2はEZH, SUZ12, EEDを核とする構成要素とし、標的遺伝子座のヒストンH3の27番目のリジンをトリメチル化する(H3K27me3)エピジェネティックな制御因子である。
(注7)骨髄線維症
ML-DSの症例では骨髄や肝臓に線維化を伴うケースが報告されており、巨核球前駆細胞の異常な増殖が線維症の原因として考えられている。
(注8)マイクロRNA
ゲノム上にコードされる微小なRNAで、遺伝子の転写後発現調節に関与している。
(注9)シングルセルRNAシークエンス
個々の細胞の遺伝子発現を網羅的に解析する技術。細胞集団を対象としたRNAシークエンス解析とは異なり、細胞集団全体の平均的な遺伝子発現ではなく、一細胞ごとの遺伝子発現のばらつきを明らかにすることができる。
(注10)PTK2
別名focal adhesion kinase (FAK)。細胞接着や拡散過程(細胞がどのように移動するか)のほか、血液細胞では巨核球分化を負に制御することが報告されている。
(注11)デファクチニブ(Defactinib)
PTK2(FAK)阻害作用を持つ経口小分子化合物で、再発低悪性度漿液性卵巣がんに対する治療効果が認められ、近年アブトメチニブ(RAF/MEK二重阻害剤)との併用療法が承認された。
問合せ先
〈研究内容について〉東京大学医科学研究所 附属幹細胞治療研究センター幹細胞分子医学分野
教授 岩間 厚志 (いわま あつし)
https://www.ims.u-tokyo.ac.jp/imsut/jp/lab/stemcell/section02.html
<機関窓口>
東京大学医科学研究所 プロジェクトコーディネーター室(広報)
https://www.ims.u-tokyo.ac.jp/