| 発表のポイント |
|---|
|
概要
東京大学医科学研究所RNA制御学分野の稲田利文教授、李思涵助教らの研究グループは、翻訳(注1)が円滑に進行せず、リボソーム(注2)間の衝突(注3)が起こることで、翻訳の速度が遅いリボソームの分解が引き起こされることを明らかにしました。翻訳開始時に単独で停滞した機能欠損リボソームが分解されることは知られていましたが、翻訳伸長段階で生じる複数リボソーム間の衝突とリボソーム安定性との関連は不明でした。本研究では、酵母リボソームのコドン解読活性中心(注4)を大腸菌型に改変したリボソームが、翻訳機能を保持しつつ野生型リボソームとの共存時に分解される現象を見出しました。変異リボソームは野生型より翻訳速度が遅く、この速度差による衝突が「敗者」となった変異リボソームの分解を引き起こすことを明らかにしました。また、抗がん剤シスプラチン(注5)や酵母の成長段階(注6)の変化によって、野生型リボソーム同士の衝突も増加し、分解が促進されることを確認しました。本成果は、リボソームの異質性(注7)に起因する疾患や薬物作用の理解に貢献することが期待されます。
本研究成果は2025年12月12日付で、英国科学雑誌「Nature Communications」オンライン版で公開され、Editors’ Highlightsに選出されました。
発表内容
翻訳の異常は、タンパク質の恒常性を乱し、不良タンパク質の蓄積や細胞機能の障害を招く要因となっています。タンパク質合成装置であるリボソームが活性を失い、翻訳開始時に単独で停滞した場合、停滞を感知するMag2とFap1によるリボソームタンパク質uS3の二段階ユビキチン化(注8)を経て、リボソーム小サブユニットが分解へと導かれます。このことから、翻訳動態の異常がリボソームの不安定化を引き起こすことが示唆されてきました。しかし、翻訳伸長中に起こる、より一般的な異常であるリボソーム間の衝突がリボソームの安定性に与える影響は不明でした。本研究チームは、リボソーム衝突と分解との関連を解明することを目的としました。出芽酵母を用いて、コドン解読活性中心の18S rRNA塩基を置換したリボソームの安定性を解析した結果、衝突センサーHel2に依存して分解される変異体を複数同定しました。なかでも大腸菌型の活性中心を模倣した「原核型変異リボソーム(注9)」は、翻訳機能を保ちながらも野生型リボソームと共存すると分解されるという興味深い特徴を示しました(図1)。遺伝学的および生化学的解析により、この変異体は野生型より翻訳速度が遅く、両者の速度差により同一mRNA上で衝突が生じることが示唆されました。リボソーム競合における「敗者」である変異リボソームは、Mag2とHel2によるuS3のユビキチン化を経て分解・淘汰されることが明らかになりました。すなわち、uS3のユビキチン化を介したリボソーム分解経路が、単独停滞に応答するMag2-Fap1経路と、衝突に応答するMag2-Hel2経路の二つに分岐することを示しました。
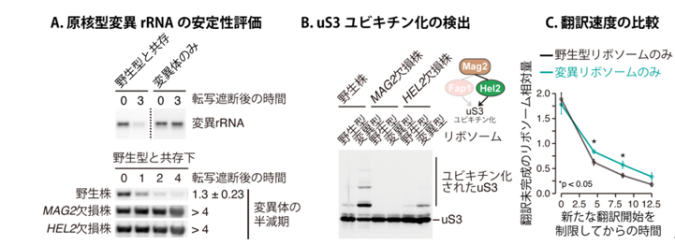
(A)原核型変異rRNAを一定時間発現させた後、その転写を遮断して経時的に細胞を回収し、残存する変異rRNAの量をノーザンブロット法で解析しました。(B)野生型リボソームまたは変異型リボソームを精製し、ウェスタンブロット法によりuS3のユビキチン化状態を比較しました。(C)翻訳開始を阻害する薬剤lactimidomycinで細胞を処理すると、翻訳伸長中のリボソームが順次翻訳を完了してmRNAから解離します。Lactimidomycin処理後、mRNAと結合している(翻訳を終えていない)リボソームの量の経時的変化をショ糖密度勾配遠心法で調べることで、野生型リボソームと変異型リボソームの翻訳速度を比較しました。
研究チームはさらに、リボソーム競合に限らず、さまざまな要因で生じる衝突がリボソーム分解を誘導する可能性を検証しました(図2)。抗がん剤シスプラチンは、トリプトファンコドンでのリボソーム停滞・衝突を増加させ、Mag2-Hel2によるuS3のユビキチン化および小サブユニット分解を促進することが観察されました。また、連続培養による増殖段階の変化過程でも、Mag2-Hel2依存的に小サブユニット量の一時的な低下が見られました。衝突に起因するリボソーム分解は、非最適なリボソームの排除のみならず、翻訳動態の変化に応じたリボソーム量の調整にも関与することが示唆されました。
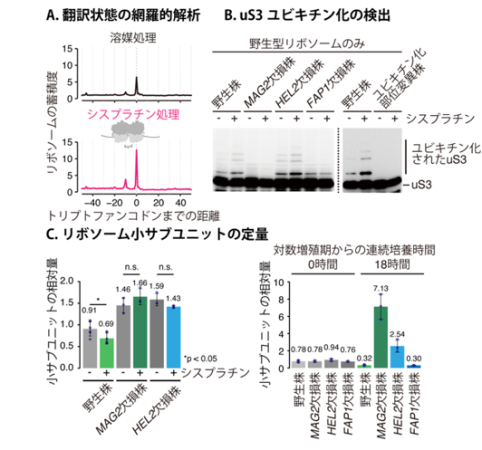
(A)溶媒またはシスプラチンで処理した細胞を用いて、mRNA上のリボソームの位置と量を網羅的に解析するリボソームプロファイリングを行いました。シスプラチン処理により、トリプトファンコドンでリボソームが蓄積(停滞)することがわかりました。(B) 溶媒またはシスプラチンで処理した細胞内のuS3のユビキチン化状態をウェスタンブロット法により調べました。(C) 溶媒またはシスプラチンで処理した細胞内のリボソーム小サブユニットと大サブユニットとの量比をショ糖密度勾配遠心法で解析しました。
本成果は、翻訳動態とリボソーム安定性を結びつける新たな仕組みを提示し、リボソームの異質性や翻訳異常に起因する疾患、さらにシスプラチンをはじめとする薬物作用の理解に貢献することが期待されます。
発表者・研究者等情報
東京大学医科学研究所 基礎医科学部門 RNA制御学分野
稲田 利文 教授
兼:同大学大学院理学研究科 生物科学専攻
李 思涵/LI SIHAN 助教
論文情報
雑誌名:Nature Communications題 名:Collision-induced ribosome degradation driven by ribosome competition and translational perturbations
著者名:Sihan Li*, Okuto Shounai, Misaki Kato, Ken Ikeuchi, Toshifumi Inada*
(*責任著者)
DOI: 10.1038/s41467-025-66026-x
URL: https://doi.org/10.1038/s41467-025-66026-x
研究助成
本研究は、日本医療研究開発機構(AMED-CREST 課題番号:20gm1110010、研究代表者:稲田利文)、日本学術振興会科学研究費助成事業(課題番号:19H05281, 21H05277, 22H00401, 25H00007、稲田利文; 23K19341, 25K18401、LI SIHAN)、武田科学振興財団研究助成金などの支援を受けて行われました。
用語解説
(注1)翻訳細胞内のメッセンジャーRNA (mRNA)の塩基情報配列をもとに、リボソームがアミノ酸をつなげてタンパク質を合成する過程。開始、伸長、終結の三つの段階に分けられる。
(注2)リボソーム
リボソームタンパク質とリボソームRNA (rRNA)から構成され、タンパク質合成(翻訳)を担う分子機械。大小二つのサブユニットからなる。
(注3)(リボソーム)衝突
mRNA配列の異常など、さまざまな要因によってリボソームが翻訳途中で停滞し、同一mRNA上を進む後続のリボソームが先頭のリボソームに追いついて接触する状態。
(注4)コドン解読活性中心
リボソーム小サブユニットにある領域で、mRNAの3塩基ごとの遺伝情報(コドン)を読み取り、対応するアミノ酸を持つトランスファーRNA(tRNA)を正確に選択する重要な役割を果たす。
(注5)シスプラチン
抗がん剤として広く用いられる化学物質で、DNAの鎖を架橋して損傷を与え、細胞分裂を阻害する。RNAにも架橋することが示されている。
(注6)酵母の成長段階
酵母集団が栄養の状態や環境に応じて示す成長の状態。代表的な成長段階には、栄養が十分なときに細胞増殖が活発に行われる対数増殖期と、連続培養などで栄養が不足して増殖が止まる静止期がある。
(注7)リボソームの異質性
細胞内のリボソームは、構成するタンパク質やRNAの変異・修飾の違いなどにより性質が不均一であること。この異質性は、特定の機能を担うリボソームの産生につながる可能性がある一方、ダイアモンド・ブラックファン貧血をはじめとする「リボソーム病」と総称されるさまざまな疾患の原因になることもある。
(注8)uS3の二段階ユビキチン化
uS3に対してユビキチンが順に付加される過程。まず、Mag2によってuS3の212番目のリジンにユビキチンが1分子付加される(モノユビキチン化)。その後、Fap1がこのユビキチンにさらにユビキチン同士を連結しユビキチン鎖を形成する(ポリユビキチン化)。Fap1の代わりにHel2もuS3のポリユビキチン化を触媒できる。
(注9)原核変異型リボソーム
コドン解読活性中心に位置する18S rRNAのhelix 44と呼ばれる領域のうち、生物種間で保存されていない二つの塩基であるG1645とA1754を大腸菌などの原核生物型に置換したリボソーム。
問合せ先
<研究内容について>東京大学医科学研究所 基礎医科学部門 RNA制御学分野
教授 稲田 利文(いなだ としふみ)
<機関窓口>
東京大学医科学研究所 プロジェクトコーディネーター室(広報)
https://www.ims.u-tokyo.ac.jp/

