| 発表のポイント |
|---|
|
概要
東京大学医科学研究所幹細胞分子医学分野の岩間厚志教授と大島基彦講師らの研究グループは、骨髄異形成症候群(MDS:注1)の幹細胞および前駆細胞分画を用いてATAC-seq解析(注2)を行い、正常な造血幹・前駆細胞の分化過程で変化する転写因子ネットワーク(注3)の異常と、それに伴い幹細胞から前駆細胞への分化の階層性が失われることを明らかにしました。さらにクロマチン状態を指標に幹細胞から前駆細胞への分化を定量的に評価する「前駆細胞スコア」を新たに定義することで、このスコアがMDSの予後予測や新たな層別化に寄与することを示しました。本研究成果は2025年 11月28日付で、英国科学雑誌「Nature Communications」オンライン版に公開されました。
発表内容
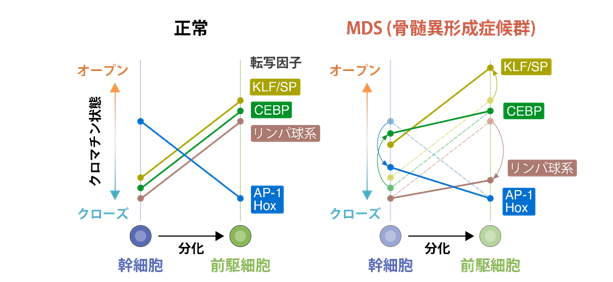
MDSは異常な造血幹細胞のクローンに起因する、多様な病態を含む疾患です。エピジェネティックな変化(注4)は、さまざまながんの分子病態に深く関わっていることが知られていますが、MDSにおいてはいまだに不明な点が多くあります。本研究ではATAC-seq解析を行うことで、MDS幹・前駆細胞の転写ネットワークの変化について詳細に検証しました(図1)。
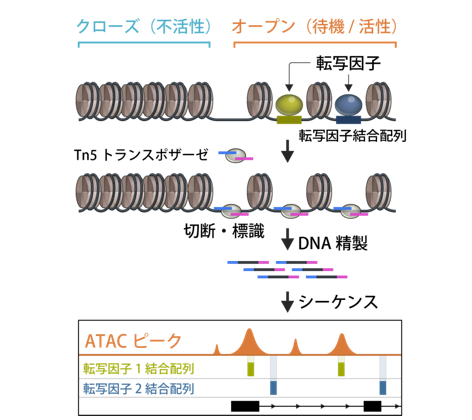
オープンな状態のクロマチン領域では、転写因子が転写因子結合配列を認識して結合し、遺伝子の発現を待機/活性化します。ATAC-seqは、オープンクロマチン領域のDNAを、Tn5トランスポザーゼが特異的に切断・標識して、それをシーケンスすることでオープンクロマチン領域をATACピークとして可視化する技術です。またATACピークにどのような転写因子結合配列があるかを調べることで、転写因子ネットワークの解析をすることが出来ます。
幹細胞、前駆細胞分画それぞれについて、正常群と病態の進展順にCCUS/ICUS、MDS-MLD、MDS-EB、AML-MRC(注5)の各疾患群のATACピークにおいて、転写因子結合配列が同定される頻度を比較したところ、幹細胞では、正常検体で高頻度に同定されるHoxファミリーやGATA、AP1 ファミリー転写因子の結合配列が疾患群で顕著に減少しており、前駆細胞ではリンパ球系の転写因子の結合配列が減少していました。また様々な造血機構に関わるファミリーや骨髄球系の転写因子であるCEBPの結合配列が幹・前駆細胞で増加することがわかりました(図2)。
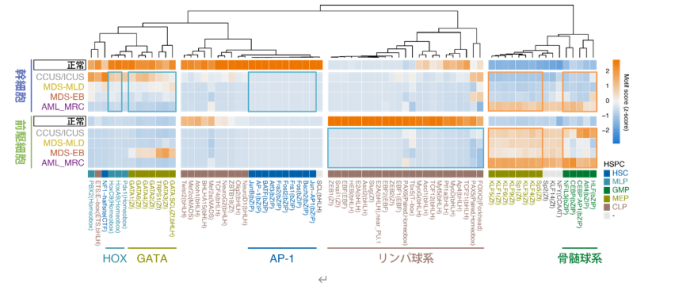
正常群および各疾患群それぞれについて、ATACシグナルの上位15%の領域にどのような転写因子結合配列が同定されるかを示している。ヒートマップのスケールは、群間の同定される頻度の違いを示しており、正の値は相対的に高率に同定され、負の値は同定される頻度が低いことを示している。
MDSの幹・前駆細胞において異常な変動が見られた転写因子の多くは、正常な幹・前駆細胞の分化過程においても変動している転写因子です。各疾患サンプルの分化傾向をより定量的に評価するため、クロマチン状態を指標に正常幹細胞を0、前駆細胞を1とするスケールの「前駆細胞スコア」を定義しました(図3a)。疾患群毎に前駆細胞スコアを比較したところ、病態の進展に伴い幹細胞分画の前駆細胞スコアは増加し、前駆細胞との階層性が失われて行くことがわかりました(図3b)。そこで、現在一般的に使用されているMDS予後予測スコアリングシステムであるIPSS-Mスコア(注6)と比較したところ、前駆細胞と幹細胞のスコアの差分値は、IPSS-Mスコアと顕著な負の相関を示すことが分かりました(図3c)。そこで前駆細胞スコアの差分値を使って、解析に使用した患者検体の生存期間との関係について検証したところ、予想通りIPSS-Mスコアの高値群は低値群と比較して有意な生存期間の短縮が確認されました。また、前駆細胞スコアの差分値(前駆細胞のスコア-幹細胞のスコア)を任意の閾値で高値群と低値群に分けたところ、低値群すなわち幹細胞から前駆細胞の階層性がより失われた群の生存期間が、著しく短縮しているおり、予後とよく相関することが明らかになりました(図3d)。

(a)正常の分化過程で変動し、かつMDSでも変動しているATACピーク領域を用いて、正常幹細胞と前駆細胞のピーク値をそれぞれ0と1に補正し、疾患サンプルのピーク値を正常の0-1スケールに合わせて補正し平均した値を前駆細胞スコアとした。(b)サンプル個別の前駆細胞スコアを疾患群毎に分け、幹-前駆細胞の変化を比較した。(c)MDS前駆細胞のスコアから幹細胞のスコアを差し引いた差分値を用いて、IPSS-Mスコアと比較した。(d)生存期間とIPSS-Mおよび差分値との比較。
同じサンプルで行ったRNA-seq解析(注7)のデータを用いて同様に前駆細胞スコアを計算してみたところ、ATAT-seq解析で見られたような顕著な特徴は示されませんでした。このことから、本研究の成果はクロマチン状態に注目することで初めて得られたものであり、転写因子ネットワークの変化と階層性の喪失というMDS病態の新たな分子基盤の解明は、今後より精度の高いMDSの予後予測や新規治療法の開発につながることが期待されます。
発表者・研究者等情報
東京大学医科学研究所 附属幹細胞治療研究センター 幹細胞分子医学分野
岩間 厚志 教授
大島 基彦 講師
岩間 厚志 教授
大島 基彦 講師
論文情報
雑誌名:Nature Communications題 名:Chromatin accessibility in stem cells unveils progressive transcriptional alterations in myelodysplastic syndrome
著者名: Motohiko Oshima#, Naoya Takayama#, Yaeko Nakajima-Takagi, Daisuke Shinoda, Naoki Itokawa, Shuhei Kurosawa, Satoshi Kaito, Takahiro Kamiya, Yuta Yamada, Shohei Andoh, Kensuke Kayamori, Sudip Kumar Paul, Maria Alejandra Kanashiro, Tomoya Muto, Shokichi Tsukamoto, Emiko Sakaida, Eriko Sato, Nozomi Yusa, Kazuaki Yokoyama, Yasuhito Nannya, Seiya Imoto, Bahityar Rahmutulla, Atsushi Kaneda, Kiyoshi Yamaguchi, Yoichi Furukawa, Noriko Doki, Koji Eto, Kei Nishikawa, Ye Ding, Tomohiro Myojo, Yuka Harada, Hironori Harada, Atsushi Iwama*(#共同筆頭著者、*責任著者)
DOI: 10.1038/s41467-025-65753-5
URL: https://www.nature.com/articles/s41467-025-65753-5
研究助成
本研究は、大島基彦講師に対する日本学術振興会(JSPS)「基盤研究(C)(課題番号:21K08366、24K11554)」、岩間厚志教授に対するJSPS「基盤研究(S)(課題番号:19H05653、24H00066)」、「新学術領域研究(研究領域提案型)(課題番号:19H05746)」、日本医療研究開発機構(AMED)「革新的がん医療実用化研究事業(課題番号:18ck0106401h0001)」、「ムーンショット型研究開発事業(課題番号:21zf0127003h0001)」などの助成金の支援により実施されました。
用語解説
(注1)骨髄異形成症候群(Myelodysplastic syndrome: MDS)骨髄異形成症候群(MDS)は、遺伝子変異などにより生じた異常な造血幹細胞に起因する、多様な病態を含む疾患です。骨髄内で拡大した異常な造血幹細胞クローンは、血球の分化プログラムの破綻により、血球の異形成や無効造血による血球減少を示し、一部の症例では急性骨髄性白血病(AML)に進展することがあります。
(注2)ATAC-seq(Assay for Transposase-Accessible Chromatin with high-throughput sequencing)解析
Tn5トランスポザーゼを用いて、オープンクロマチン領域を切断・標識し、そのDNA断片をシーケンスすることで、ゲノム全体のクロマチン構造の開閉状態を可視化する手法です。転写因子結合部位などの活性領域の開閉状態を網羅的に検証することで、転写因子ネットワークの変化を明らかにすることができます。
(注3)造血系の分化過程で変化する転写因子ネットワーク
赤血球、白血球、血小板などの多様な血液細胞は全て、多能性を持つ造血幹細胞が分化・成熟することで産生されています。この造血系の分化過程では、GATA、RUNX、CEBP、TAL1といった様々な転写因子のネットワークが厳密に制御されながら変化することで、系統特異的な分化が段階的に進行していきます。
(注4)エピジェネティックな変化
エピジェネティックな変化は、DNA配列そのものを変えることなく、遺伝子の発現状態を制御する分子機構で、転写因子ネットワークと協調して働きます。転写因子はクロマチン修飾酵素をリクルートすることでクロマチン構造を変化させ、細胞特異的な遺伝子発現プログラムを形成します。
(注5)CCUS/ICUS、MDS-MLD、MDS-EB、AML-MRC
・CCUS(Clonal Cytopenia of Undetermined Significance):
血球減少を示しつつ、造血幹細胞に体細胞変異が認められる状態で、MDSの診断基準を満たさないクローン性前駆段階です。将来的にMDSなどへ進展するリスクがあります。
・ICUS(Idiopathic Cytopenia of Undetermined Significance):
血球減少が持続しますが、明確な形態異常や遺伝子変異が確認されない状態です。非クローン性であり、原因不明の骨髄低形成や慢性炎症などが背景にある場合もあります。
・MDS-MLD(Myelodysplastic Syndrome with Multilineage Dysplasia):
複数系統(通常は2系統以上)の血球に形態学的異形成を認めるMDSで、芽球増加は軽度です。代表的なMDSの病型で、慢性経過をとることが多いです。
・MDS-EB(Myelodysplastic Syndrome with Excess Blasts):
骨髄または末梢血中に芽球が増加(5~19%)する病型で、急性骨髄性白血病(AML)への移行リスクが高いです。病勢進行期のMDSを反映します。
・AML-MRC(Acute Myeloid Leukemia with Myelodysplasia-Related Changes):
MDS関連変化を伴うAMLで、①既往MDSの存在、②MDS関連染色体異常、③複数系統の異形成のいずれかを満たします。予後不良で、しばしばMDS-EBから連続的に発症します。
病態は、CCUS/ICUS、MDS-MLD、MDS-EB、AML-MRCの順に進展します。
(注6)IPSS-Mスコア
IPSS-M(International Prognostic Scoring System – Molecular)は、MDSの予後を評価するための国際的スコアリングシステムで、従来のRevised IPSS(IPSS-R)における臨床指標(血球数、芽球比率、染色体異常)に加えて、遺伝子変異情報を統合的に評価します。
(注7) RNA-seq解析
細胞内のRNAを網羅的にシーケンスして遺伝子発現量を定量化する手法で、転写産物の全体像を明らかにします。
問合せ先
〈研究内容について〉東京大学医科学研究所 附属幹細胞治療研究センター 幹細胞分子医学分野
教授 岩間 厚志 (いわま あつし)
https://www.ims.u-tokyo.ac.jp/imsut/jp/lab/stemcell/section02.html
東京大学医科学研究所 プロジェクトコーディネーター室(広報)
https://www.ims.u-tokyo.ac.jp/