| 発表のポイント |
|---|
|
発表内容
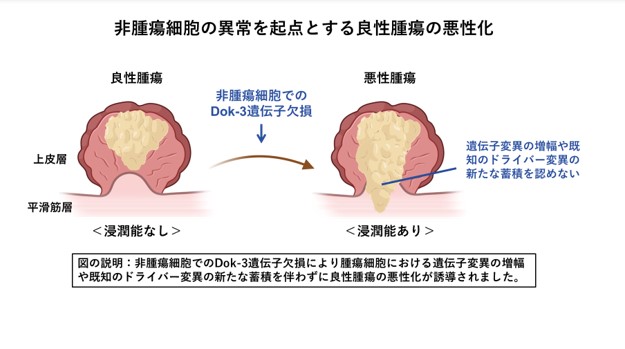
腫瘍形成やその悪性化を誘導する遺伝子変異(ドライバー変異)の蓄積によりがんが発生するという多段階発がん説(注1)が広く認められています。近年の研究から、上皮細胞のドライバー変異は当該細胞の挙動を変化させるだけでなく、非腫瘍細胞(線維芽細胞、内皮細胞、血球系細胞など)にも影響を与えることで腫瘍形成や悪性化を促進することが報告されています。そのような背景の下、非腫瘍細胞に人為的な遺伝子変異を導入することで、良性腫瘍がその遺伝子変異の増幅や既知のドライバー変異の新たな蓄積を伴わずに浸潤能を獲得する、という全く新しい腫瘍悪性化機構を発見しました。さらに、この悪性化はCD4陽性T細胞とCD8陽性T細胞を必要とすることや、炎症性サイトカインの発現誘導等の炎症応答の亢進を伴わないことを見出しました。本研究成果は非腫瘍細胞の異常を起点とする、良性腫瘍の新たな悪性化機構の発見であり、当該分子機構の理解に基づく治療法開発への発展が期待されます。
本研究は、日本学術振興会(JSPS)科学研究費助成事業(18K19470、15H05574)や一般財団法人阪大微生物病研究会(BIKEN財団)の助成を受けて実施されました。
発表内容
① 研究の背景・先行研究における問題点悪性腫瘍(がん)と良性腫瘍の決定的な違いは浸潤能の有無にあります。浸潤能を獲得した悪性腫瘍細胞による基底膜の破壊を介した周囲組織への浸潤は、浸潤-転移カスケード(注2)の第一段階であり、血管内侵襲、血管外流出、遠隔臓器への生着を経て転移が成立します。約90%の癌死の原因が転移であると報告されていることから、浸潤-転移カスケードは癌の治療標的になると考えられていますが、その機構の詳細は十分に理解されていません。
多段階発がんは、ドライバー変異の蓄積により腫瘍形成から悪性化の各段階が誘導されるというモデルであり、大腸がんにおいてよく研究されています。近年の研究により個々のドライバー変異が、非腫瘍細胞を巻き込んだ腫瘍微小環境(注3)の形成を介して腫瘍形成や悪性化を促進することが報告されている一方で、非腫瘍細胞の異常を起点とし、腫瘍細胞における遺伝子変異の増幅やドライバー変異の新たな蓄積を伴わない腫瘍悪性化の報告は知られていません。
② 研究内容
現在までに7種類同定されているDokファミリータンパク質のうち、Dok-1、Dok-2、Dok-3(Dok-1/-2/-3)から成るサブファミリーは、いわゆるアダプター分子として、免疫細胞におけるチロシンキナーゼシグナルを負に制御することが知られています。我々はこれまでにDok-1/-2/-3ががん抑制遺伝子であることをマウスにおいて報告していましたが、それらの腫瘍悪性化における機能は不明でした。
そこで腸管腫瘍の悪性化におけるDok-1/-2/-3の役割を明らかにすべく、良性腫瘍(腸管ポリープ)の自然発症モデルであるApcMin/+マウス(注4)に、Dokファミリー内で最も近縁なDok-1とDok-2の二重欠損、もしくは、Dok-3の単欠損を導入したところ、前者は腫瘍の増生を亢進させるのに対し、後者は腫瘍の増生に影響を与えず腫瘍の浸潤を誘導することが判明しました。興味深いことに、Dok-3の発現は腫瘍上皮細胞では検出されず、また、この浸潤、つまり腫瘍悪性化の誘導は腫瘍細胞における遺伝子変異の増幅や新たなドライバー変異の蓄積を伴わないことが判明しました。さらに、この腫瘍悪性化にはCD4陽性T細胞とCD8陽性T細胞が必須であると共に、異常な非腫瘍細胞であるDok-3欠損骨髄細胞の移植により再現できること、また、血球系細胞の腫瘍内浸潤等の炎症応答の亢進を伴わないことを解明しました。
③ 社会的意義・今後の予定など
本研究の成果は、これまでに報告のない良性腫瘍の悪性化誘導機構を提示するものであり、腫瘍悪性化の新たな分子メカニズムの解明と、その理解に基づく新たな治療法開発の基盤となる点において高い社会的意義を有します。
発表雑誌
雑誌名:「Cancer Research Communications」(2022年11月28日オンライン掲載)論文タイトル:Loss of Dok-3 in non-tumor cells induces malignant transformation of benign epithelial tumor cells of the intestine
著者:Sumimasa Arimura*, Akane Inoue-Yamauchi*, Kotoe Katayama, Tatsuo Kanno, Hiroki Jozawa, Seiya Imoto, and Yuji Yamanashi**
*:共筆頭著者
**:責任著者
DOI: 10.1158/2767-9764.CRC-22-0347
URL: https://doi.org/10.1158/2767-9764.CRC-22-0347
問い合わせ先
<研究に関するお問い合わせ>東京大学医科学研究所腫瘍抑制分野
教授 山梨 裕司(やまなし ゆうじ)
https://www.ims.u-tokyo.ac.jp/imsut/jp/lab/cancerbiology/section03.html
<報道に関するお問い合わせ>
東京大学医科学研究所 国際学術連携室(広報)
https://www.ims.u-tokyo.ac.jp/imsut/jp/
用語解説
(注1)多段階発がん説: 腫瘍形成やその悪性化を誘導する遺伝子の変異(ドライバー変異)の蓄積が腫瘍形成から悪性化の各段階を誘導するという概念。この概念が確立されている大腸がんでは、Apc遺伝子の不活性化により正常上皮細胞から良性腫瘍(腺腫)が発生し、Kras変異や p53変異などが加わることで悪性腫瘍(腺がん)に進展するとされています。(注2)浸潤―転移カスケード:多段階プロセスとしてのがん転移機構を意味する用語であり、がん細胞の原発巣からの離脱と周囲組織への浸潤、近傍の血管内への進入、血流への移行、血管外への流出、遠隔組織(転移組織)での増殖による微小転移巣の形成、肉眼的転移巣の形成が含まれます。がん細胞の周囲組織への浸潤はこの転移過程に必須の極めて重要な初期過程です。
(注3)腫瘍微小環境:腫瘍組織において腫瘍細胞周辺に形成される線維芽細胞、内皮細胞、血球系細胞などの様々な非腫瘍細胞からなる環境の総称。腫瘍微小環境は腫瘍の増生や悪性化に重要な役割を果たすことが知られています。
(注4)ApcMin/+マウス:ApcはWntシグナルに重要なシグナル伝達分子であるb-カテニンの抑制因子であり、Apc遺伝子の機能欠失型変異は散発性のヒト大腸がんの約9割に認められています。ApcMinマウス/+はApc遺伝子の変異をヘテロに有するマウスであり、その対立遺伝子座欠失(loss of heterozygosity: LOH)によりWnt経路が活性化し、100%の個体が小腸及び大腸に良性腫瘍を発生します。