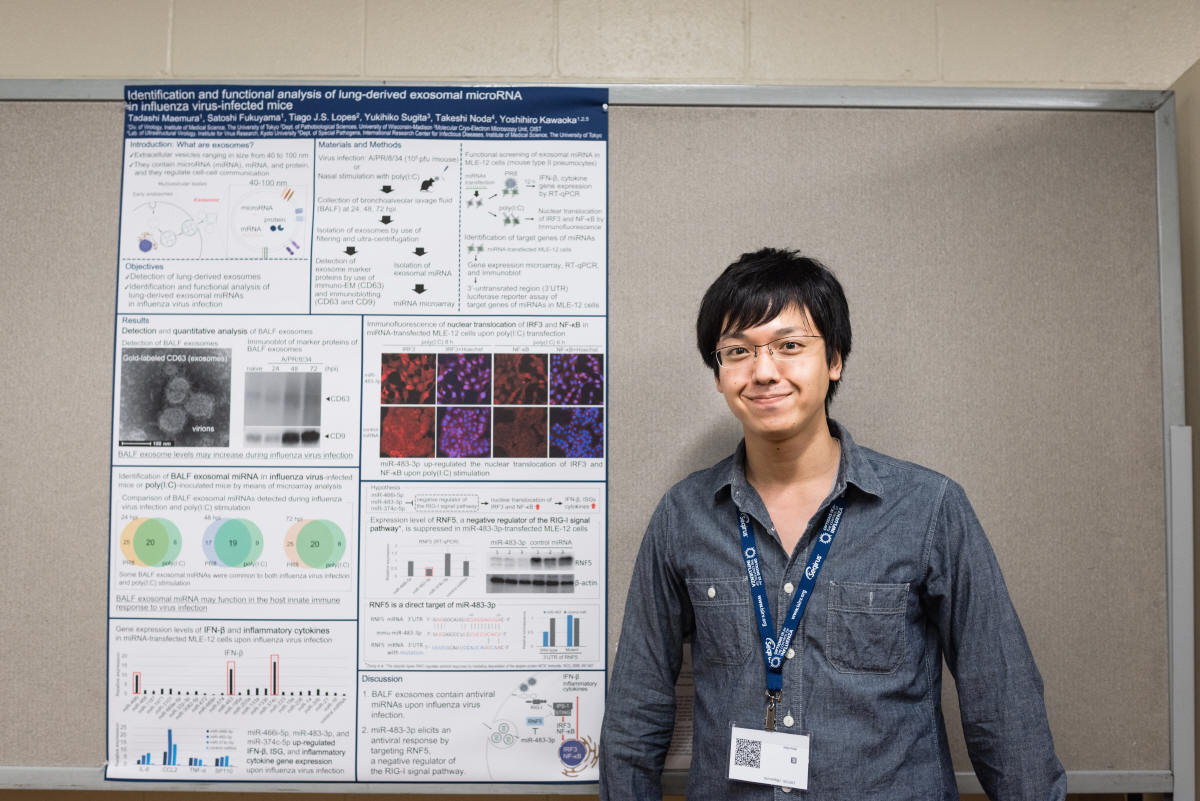
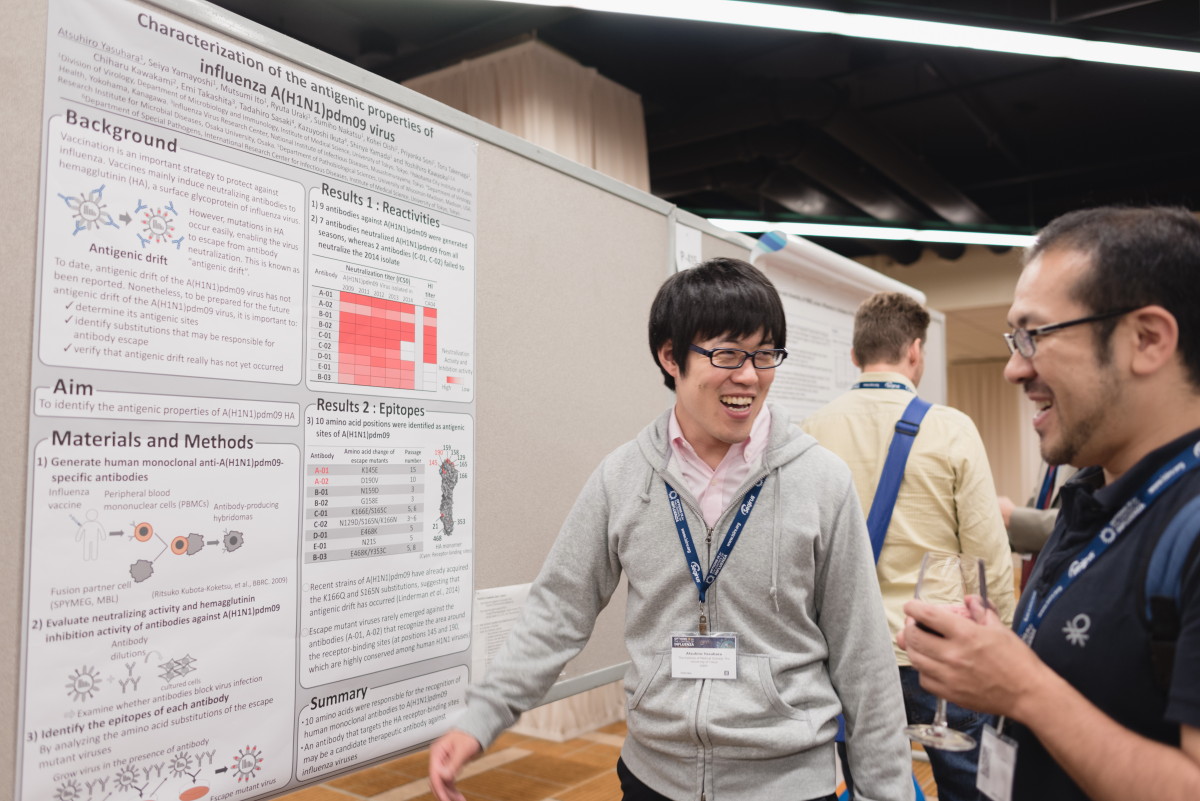
研究活動
学会報告
- Options IX for the control of influenza (2016/8/24-28)
- The fifth ESWI conference @ Rigta, Latvia (2014/9/14-17)
- 獣医学会 (2014/9/9-12)
- IUMS 2014 (2014/7/27-8/1)
- Keystone symposia (2014/1/19-25)
Options IX for the control of influenza (2016/8/24-28)
It’s really a great experience and chance to acquire up-to-date knowledge of influenza virus. I spent most of the time in the Virology & pathogenesis session. I noticed that there are good amount of research on neutrophils and CD8+ T cells, which are very interesting in general. And there are not so many presentations about the genome packaging - I guess that it may be the time when imaging can bring something new to this subject. Following are some presentations that interested me the most:
Talks
- Prof. Peter Palese’s (Mount Sinai) talk on the anti-stalk antibody. I am most amazed by how they link the protection from the specific antibody to the ADCC. Dr. Caitlin Mullarkey from the same institute further elaborates the work by describing the role of ROS in the mechanism. She also showed that IgG induces phagocytosis for protection, while IgA elicits NETs. This talk (O-86) is also very interesting.
- Prof. Anice Lowen (Emory University) showed an interesting approach to study the resassortment of vRNP segments in a global manner. Her results suggest that the vRNP segments interact with each other with certain preferences, which may be very helpful for designing related experiments in molecular virology.
- Dr. Yohei Yamauchi (University of Zurich) presented his working on the uncoating mechanism of IAV, and I’m simply happy to listen to a talk about virus entry. While HDAC6 and ubiquitination play a fundamental role in the uncoating, he also mentioned that HDAC6 may be important for packaging as well.
Poster
- Lakdawala lab from U. Pitts. (LBP-8) presented their work on the role of microtubules (MT) on intracellular assembly of vRNA. Their study doesn’t bring too much to the subject in addition to what Palese lab have published (vRNA assembly is independent of MT). The only new thing is probably that the recruitment of vRNA to Rab11+ endosome is also MT-independent.
- Flethcer lab from UC Berkeley (LBP-28) presented their work in using enzymatic labeling to tag viral proteins (M, NP) and Rab11+ endosome (via tag poly-Ig receptor, which is not really specific though). They use this approach to visualize and study the formation of progeny virion. According to the presenter, they can now use up to 4 or 5 tags simultaneously. The advantage of this approach is that it only introduce one copy of fluorophore to each target protein, therefore minimize the interference to the biological processes. However, this is also a disadvantage in terms of imaging, since highly sensitive and low background microscopy will be mandatory for such an approach. In this case, they are using TIRF and only to observe virions adsorbed on the coverslips or infection events happens at the plasma membrane. Presenter mentions that imaging the apical plasma membrane on TIRF is very difficult so that he only does it when really necessary; and imaging the events in the cytoplasm is probably not possible (due to the high back round). On the same day, Garcia-Sastre lab (O-69) also shows that how they use the same approach to label HA and visualize its intracellular transport upon infection. Their image quality is not as good, but massive amount of HA allows to perform imaging with regular microscopes.
Biology-wise, Fletcher lab’s data suggests that vRNPs arrive plasma membrane in a hand-off way (from Rab11+ endosome to the plasma membrane), instead of via direct fusion between the Rab11+ endosome and the plasma membrane.
ポスドク Jessica IH Wang
初めて国際学会に参加させていただきました。世界中のインフルエンザウイルス研究者が1つの会場に集まり講演を聞いている様子は、インフルエンザウイルスに一丸となって立ち向かっているようにもみえ、’save the world’ に向けて取り組んでいるように感じられ、感激しました。
様々な基礎研究発表に加え、臨床ガイドラインのオーバービューなど、普段聞くことができない内容に触れることができた素晴らしい学会でした。発展途上国で高病原性の鳥インフルエンザウイルスのヒトへの暴露が問題となっているなかで、その国の現状を踏まえたうえでの対策(適切な容器を使用したうえでのニワトリの屠殺、読める文字を用いたポスターによる啓もう活動など)が重要であるとの話には、シエラレオネでとられていたエボラウイルスの拡大防止策にも重なるところがありました。
以下、自身が行っているmiRNAに関与した研究で印象深かった発表についてまとめました。
Dr. Benjamin R. tenOever
「The biology of Influenza Virus non-coding RNAs」
宿主のmiRNAそのものは、ウイルスゲノムにはほとんど直接の影響を与えないことを示したうえで、ウイルスゲノム由来のsmall RNA(svRNA)が、ウイルスの生活環に関与している可能性を提示していた。
このsvRNAは、宿主のDicer非依存的に発現することから、miRNA発現機構とは異なるメカニズムにより産生されるsmall RNAであることが示された。ウイルス感染細胞では各セグメントの3’または5’末のnon-coding領域に由来するsvRNAが産生され、svRNA発現パターンとcRNAの発現量は相関している一方で、vRNAの発現には相関しないことが示されていた。svRNAの配列に変異を導入したウイルスは、各ウイルス蛋白質の発現量には影響を与えないものの、ウイルスの増殖を低下させた。これはインフルエンザウイルスの生活環の制御にウイルス由来のsmall RNAが関与している可能性を示す結果であり、大変興味深かった。
ウイルス自身が産生するsmall RNAがウイルスの増殖をサポートしている現象は、現在でも議論が行われている「哺乳類がウイルスに対する防御メカニズムとしてsiRNAの産生を行っているのか」、という疑問に答えるうえで重要な研究であると感じた。
Dr. Balaji Manicassamy
「Endothelial cell tropism is a determinant of H5N1 pathogenesis in mammalian species」
Dr. Manicassamyは、当研究室で開発したcolor-flu-virusの研究基盤となったNS1-GFP発現PR8を報告した論文 (Manicassamy et al., PNAS, 2010) での筆頭著者で、現在はシカゴ大学でPIである。
今回のDr. Manicassamyの発表内容は、宿主のmiRNAを用いたH5N1ウイルスの病原性解析であった。季節性のインフルエンザウイルスと異なり、高病原性の鳥インフルエンザウイルスは細網内皮系と言われるような血管内皮細胞やマクロファージ、単球、樹状細胞などの免疫細胞に感染する。その結果全身の臓器にウイルスが波及し増殖することで、強力に炎症性サイトカインが誘導され、Immunopathologyといわれる病態を生じる。
発表者らは細網内皮系で増殖しないH5N1高病原性鳥インフルエンザウイルスを作成し、培養細胞、マウスでのウイルスの増殖や免疫応答を解析することで、高病原性鳥インフルエンザウイルスの細網内皮系に与える影響を評価した。
VN1203株のNPセグメントのORFの直後に、microRNA(miR-126, miR-142)の標的配列(T)をタンデムに4つ導入したウイルスを作成した。miR-126は、内皮細胞に特異的に発現するmiRNAで、miR-142は血球系の細胞に特異的に発現するmiRNAである。培養細胞にこれらウイルスを感染させたところ、miR-126Tを持つウイルスは内皮細胞で増えにくく、miR-142Tを持つウイルスは血球系の免疫細胞で増えにくいという結果になった。コントロールのウイルスと比較して、103倍以上ウイルスタイターが抑えられたことに驚いたが、内皮細胞または免疫細胞でのmiRNAの発現量と標的配列をタンデムに4つ配置したことが影響しているのではないかと感じた。マウスにウイルスを感染させたところ、マウスの肺でのこれらmiRNAの標的配列をもつウイルスの増殖は、野生型のウイルスと同様であったが、マウスの体重減少と生存は野生型ウイルスと比較してマイルドで、病原性が低下していた。野生型ウイルスを感染させたマウスと比較して、miRNAの標的配列を持つウイルスを感染させたマウスでは、Immunopathologyの原因である炎症性サイトカインの発現が低下、微小血管の透過性も低下、肺の組織学的損傷レベルも低下していた。
以上から、H5N1高病原性鳥インフルエンザウイルスの病原性が高い原因の一つは、このウイルスが細網内皮系にtropismを有していることであることが示された。今後異なるウイルス(スペイン風邪ウイルス, H7N9高病原性鳥インフルエンザウイルスなど)でも同様の系を用いて病原性を解析することで、それぞれのウイルスのtropismの観点から病原性解析を行うことができる。miRNAは宿主間、細胞腫間で高度に保存されており、細胞特異的に発現しているmiRNAに対する標的配列を付加したウイルスを用いた病原性解析は、非常に効率のいい解析であると感じた。
D4 前村 忠
【全体のまとめ】
オプションでは、個々の発表がClinical science, Public health とVirology & pathogenesisの3つのカテゴリーに分類されており、学会開催中に全てのカテゴリーの話を聞くことができた。
Clinical scienceやpublic healthは普段馴染みがない分野だが、インフルエンザ制圧に向けた多方面からの話を聞くことで、現在のインフルエンザ研究の全体像を把握できたように感じる。
Clinical science
新規抗ウイルス薬であるPA阻害剤の話や、重症化したインフルエンザに対する治療法の話を聞いた。
抗ウイルス薬や治療法の有効性を確認するには、予め、薬や治療が効いたとする評価項目(endpoint)を設定しておく必要がある。しかし、University of Amsterdamのde Jong先生によれば、インフルエンザは採取する検体、部位、ウイルス検出方法や検体を検査する感染後日数など、決めるべき項目が多岐に渡るため、ウイルス学的なendpointの設定がchallengingであるとのことだった。抗ウイルス薬の作用機序や治療法にもよるが、適切なendpointの設定が、薬の安全性や速やかな上市につながると思った。
PA阻害剤について学会で話を聞くのは初めてだったが、University of VirginiaのHayden先生によれば、PA阻害剤はタミフルと比較してウイルス量が劇的に下がる(4 log vs. half~1 log reduction in viral load, 24hpi)とのことだった。
Public health
WHOの方からインフルエンザの治療法や予防法に関する話を、China CDCのShu先生から中国の生鳥市場におけるインフルエンザウイルスの流行・発生状況に関する話を聞いた。国際機関であるWHOはインフルエンザに対する予防法・治療法のスタンダードを確立する必要があるが、中国の生鳥市場のように、文化的背景によって地域ごとにウイルスが流行し得る状況は異なる。さらに、CDCのJernigan先生も言っていたように、インフルエンザ感染者数やサーベイランスが行われている地域にも偏りがある。これら全てを考慮した上でスタンダードを考え、実施していくことの難しさ感じた。
Virology & pathogenicity
Invited talkでは、semi-infectious particlesが多く存在することをFACSで示したJohnathan Yewdell先生と、semi-infectious particlesをhighMOIでモルモットに感染させるとreassortant効率が上がることを示したAnice Lowen先生の話が印象的だった。特にLowen先生の発表では、リアソートメントにバイアスがかかること、二つの株のどのセグメントが取り込まれやすいのかが示されていた。しかし、そのバイアスのメカニズムはまだわかっていない。
以下に、virology & pathogenesisのセクションで聞いた発表で、自分のテーマであるゲノムパッケージングの研究をしていた発表をまとめる。
- The dual roles of the HA segment-specific noncoding nucleotides in the extended duplex region of the influenza A viruses (IAV) RNA promoter.
By Prof. Tao Deng
HAとNA segmentのnon-coding region (NCR)には、subtype-specificな塩基が存在しているが、そのNCRの中には、segment-specificな塩基(3’: 13-14 (CC), 5’: 13’-15’ (GUG))が存在している。
このsegment-specificな塩基の役割を明らかにするため、これらの箇所が異なるmutantを作成し、promoter活性・transcription・replication・ウイルス粒子内へのHA segmentの取り込み効率を比較した。
その結果、3’13と5’14’はvRNAのpromoter活性に、3’14-5’15’はvRNAの合成に関与することがわかった。さらに、3’14がHA segmentのウイルス粒子内への取り込みに重要な役割を果たすことがわかった。
これまでに同じグループから、HA segmentのNCR内にsegment-specificな塩基があることと、3’末端側のNCRがHA segmentの取り込みに関わっていることが報告されている (Zhao et al., J Virol. 2014)。今回の発表では、segment-specificな塩基のひとつひとつが担っている役割が報告された。 - Incorporation of the influenza A virus NA segment does not require homologous non-coding sequences.
By Prof. Sylvie van der Werf A型インフルエンザウイルスゲノムの各セグメントには、それぞれ3’末端と5’末端にnoncoding region (NCR)が存在する。NCRはさらに、全セグメントに共通のconserved regionと、各セグメント特異的なnon-conserved regionに分けることが出来る。これまでにconserved regionの配列はvRNAのtranscription/replicationに必須であること、non-conserved regionと近接するcoding regionの一部はゲノムパッケージングに重要であることが報告されている。
このnon-conserved regionがゲノムパッケージングに与える影響をさらに解析するため、異なるセグメントのNCRを持つNAセグメント(x-NA-x)を作成し、ウイルスの増殖や各NCRを持ったNAセグメントがウイルス粒子内に取り込まれる効率を比較した。
その結果、全てのウイルスをレスキューできたが、各ウイルスのタイターはNAセグメントの取り込み効率に依存していた。各ウイルスをMDCK細胞で継代し、増殖が 増えたものについてDeep-sequencingを行ったところ、M-NA-M, NS-NA-NS, NP-NA-NPでは5’ NCRに1-10塩基のinsertionが見られた。M, NS, NPの5’NCRはNAのNCRよりも短いため、NAセグメントの取り込みには5’末端側の長さが必要なのかもしれない。
さらにPB2-NA-PB2, PB1-NA-PB1, PA-NA-PAでは、NCRにpoint mutationが確認された。
これらのことから、genome同士のネットワーキングにmutationやinsertionが必要である可能性がある。
【その他】
これまでに3回国際学会に参加する機会をいただいたが、今回は特に、演者に対しphilosophicalな質問 (その事象はどのような意味があると思うのか、自分はどう考えているのかetc…)をしている人が多かったように感じた。ただこれは、こういった質問が今回のmeetingで特に多かったわけではなく、自分が質問の内容を理解できるようになったから多く感じたのだと思う。
D3 中津 寿実保
24日から28日までの4日間、シカゴで行われたoptions Ⅸ for the control of influenzaに参加してきました。
会場はSheraton grand hotelで学会のスケージュルは、はじめの3日間は8時から19時半まで、最終日は15時まででした。
名前の通りInfluenza限定の学会にもかかわらず、その規模や参加者数がシエナで開催されたNegative Strand Meetingの数倍で驚きました。開催地がアメリカということもあってか、シエナの時にはお目にかかれなかったアメリカや中国の有名な先生方がたくさんいらしており、最新の研究からこれまでの研究の総括的なお話まで非常に興味深い発表をたくさん聴くことができました。
学会は大きくPublic health 、Clinical Science、Virology and Pathology の3つのセッションにわかれていました。午前中は、初日はClinical Science、2日目はPublic healthといったように日毎にひとつのセッションにフォーカスしたプログラムが組まれており、午後はすべてのセッションがパラレルに進行しているため聞きたい演題を選び移動するというスタイルでした。またポスターセッションは非常に充実しており、3日間で計700ものポスター演題が登録されていました。
私はvirology and pathologyの演題を多く聴いたのですが、Public health のセッションでは、ヨーロッパでワクチンがどのくらい広まっているか、ワクチンの生産コストや妊婦に対する安全性はどうかといった話から中国の鶏市場の現状と今後についての演題が、 Clinical Scienceのセッションでは抗インフルエンザ薬の多剤併用や抗体医療の効果や懸念事項について、これからphaseⅢに入ろうとしている抗インフルエンザ薬の効果についてといった演題から、薬の効果を定量的に比較するためのスタンダードをどのように設定すべきかといった演題までありました。
このように日本のウイルス学会や他の学会では聴くことができないようなインフルエンザに関するマニアックな演題が非常に多く、広く蔓延している病気だけにひとえにインフルエンザの研究をしているといってもこれだけ異なる研究の形があるのだと改めて実感しました。
またNIHやWHOの方の発表では、様々な国においてワクチン接種がどのくらい推し進められているかや、鳥インフルエンザの蔓延を予防するためどういった政策をとっているかといった世界規模の新しいデータも多く引用されており、全世界の研究者たちがインフルエンザに立ち向かっている現状をつぶさに知ることができました。
上述したように、インフルエンザにフォーカスした学会ということでこれまで参加した他の学会とは全く違ったコンセプトの演題が多くあり、とても興味深かったです。また参加者のほとんどがインフルエンザの専門家であり、場合によっては競争相手でもあるため熱のこもったディスカッションも各所で多く見られました。自身や他の学生の研究に応用できそうな知見もあった一方で、他のグループに先を越されていることを実感することも多々あり、良い刺激にもなったと思います。
個人的にはアメリカでは英語が非常に早く、シエナの時と比べても聞き取るのに非常に苦戦しました。また学会の内容とはあまり関係ないですが、発表中にスライドを撮影する人が非常に多いことに驚きました。NSVではそういった光景は見かけなかったのでお国柄なのか、近年の学会の傾向なのかはわかりませんが、小さい字でさらっと出しただけのつもりでもしっかり記録されてしまうため、スライドにのせる情報は漏れても大丈夫なものだけに限るよう気をつけないといけないと思いました。
今回はPublic health 、Clinical Science、Virology and Pathologyの各セッションから、気になった発表について少しですがまとめてみました。
【Public health】
The Market as an influenza Risk Factor: The animal human interface
中国の生鳥市場の現状についての発表が印象的でした。実際の市場や飼育所の写真を見て、高い病原性を示すことからも注目されているH5N1、H7N9高病原性鳥インフルエンザが出現し蔓延する原因として、未だ劣悪と言わざるをえない家畜の飼育環境があることを実感しました。初期のH5N1およびH7N9の感染患者のおよそ半数は市場を訪れ感染したことがわかっており、また市場で働く労働者の多くがH9やH6の鳥インフルエンザに対する抗体を持っていることからも、市場で働く労働者も常にインフルエンザウイルスの脅威にさらされているのだと知りました。こうした中国の内情についての発表後の質疑応答時に、他国の研究者が環境改善を指摘するシーンも見られましたが、発表者である中国の研究者も現状が良くないことはわかっているようで、科学的な理想と経済的な現実のギャップを垣間見ました。
インフルエンザは経済的にも大きな影響を与える感染症であるため、科学的な側面に加え政治的な側面も考慮に入れなければいけないと改めて感じました。
【Clinical science】
S-033188, a Small Molecule Inhibitor of Cap-dependent Endonuclease of Influenza A and B Virus, Leads to Rapid and Profound Viral Load Reduction
S-033447/S-033188, a Small Molecule Inhibitor of Cap-dependent Endonuclease of Influenza A and B Virus: Non Clinical Efficacy against Influenza A and B Virus Infection
様々な薬の効果、耐性ウイルスの発表が多い中、やはりPA-Xの研究をする上で新規抗インフルエンザ薬として開発が進んでいるPAのエンドヌクレアーゼ活性に対する阻害薬の話が興味深かったです。
小耳には挟んでいたのですが、塩野義製薬がPAのエンドヌクレアーゼ活性に対する阻害薬の開発を進めており、現在phaseⅡ、来年にはphaseⅢへと進んでいくそうで、満を持してその効力をポスター及び口頭で発表されていました。
PAのエンドヌクレアーゼ活性に対する阻害薬についての論文は古くから存在しており、特にPAのN末端の結晶構造が解かれた2009年ごろからさらに多く見かけるようになりました。これらのほとんどは、エンドヌクレアーゼ活性に必要なMn2+ないしMg2+の代わりに結合部位にはまりこむことで活性を阻害します。
しかしながら、これまでの化合物は大きな環構造と炭素鎖を有しているため細胞に入ることができず、その結果ウイルスのplaque reductionもできませんでした。そのため、in vitroではIC50=数nMという高い活性阻害効果を持ちながら、主に精製したPAのエンドヌクレアーゼ活性を評価する際の阻害剤として用いられていました。今回、塩野義製薬が同定した化合物S-033188は構造は明らかにされていませんが、細胞に侵入できるほどの低分子化合物であり、高い抗ウイルス効果が期待されます。単独の経口摂取にも関わらず、マウスにおいてIC50=数nMという値を示し、人においても6mgで十分な効果を示すことが確認されているようです。
PA-Xはそのエンドヌクレアーゼ活性によりmRNAを分解し、蛋白質の発現抑制を引き起こします。そのため、S-033188やそれから派生した薬剤がPA-Xの活性を阻害する可能性は十分考えられます。そのような薬剤がみつかると、PA-Xの大量発現・精製が可能になるため解析の幅が格段に広がることが期待されます。新薬の開発はそういった側面でも、研究の役に立つものだと思いました。
【Virology and Pathology】
Genome wide CRISPR/Cas9 screen identifies host factors imperative for Influenza virus replication
CRISPR/Cas9システムを用いたスクリーニングの口頭発表が2つあり、そのうちひとつではうちのラボで行ったスクリーニングとほぼ同じストラテジーでスクリーニングを行っていました。A549にレンチウイルスライブラリーを感染させることでノックアウト細胞ライブライリーを作製し、H5N1を感染させ生残した細胞を解析するというものです。ここまでの過程で大きく異なるのは、Cas9発現A549を作製しそこにgRNA搭載レンチウイルスを感染させていることです。当ラボではレンチウイルスがgRNAおよびCas9を搭載しており、それを感染させることでノックアウトを行おうとしていましたがCas9の発現量が少なくノックアウト効率が悪いことが障害になっていました。Cas9発現A549を作製することで、ノックアウト効率が改善し彼らのグループはスクリーニングがうまくいったのだと思います。その後、様々なウイルス株での増殖効率の低下を確認し、各因子がウイルス生活環のどのステップに関与しているかといった解析まで終わっている因子がいくつかあるようでした。当ラボの解析でポジティブコントロールとして用いているSLC35A1をノックアウトした細胞株がスクリーニングの結果得られていることからも、スクリーニングの信ぴょう性が伺え、他の因子についてもウイルス感染に関与している可能性が高いように思えました。幸い、当ラボでの解析の結果リストに挙がっている因子との重複はなかったため、帰ったら解析を進めます。
D2 大石 康平
Options2016のポスター発表の際に頂いた質問およびコメントと、いくつかの演題を紹介します。ポスター発表はポスターの場所が良かったのと、抗原性の変化というメジャーなトピックを含んでいたこともあってか、多くの方が質問してくださり大変勉強になりました。口頭発表の演題では、政策面や公衆衛生といった普段聞けない話題も聞けたことは大変興味深かったです。ただ、英語が聞き取れないことが多く、理解できないこともあったため、英語の勉強をがんばります。
〈ポスター発表で受けた質問とコメント〉
- モノクローナル抗体を使って抗原性を調べているが、ヒトの血清だと違いは出るのか。
- A(H1N1)pdm09のワクチン株は変えたほうがいいと思うか。
- エスケープミュータントが出現しにくい抗体が認識する145番目のアミノ酸はA(H1N1)pdm09-HAに特徴的なループを形成するのに重要なアミノ酸である。HAの構造を維持するため変異が起こりにくいのかもしれないとのこと。
- (横浜衛生学研究所の川上先生より)日本において2015/2016冬シーズンは、A(H1N1)pdm09が大流行した。その理由は抗原性の変化にあると思うか。
- H3N2においても166番目のアミノ酸は出現後早めに変異している(A(H1N1)pdm09では、166番目に変異をもつアミノ酸は2013-2014冬シーズンから出現し、現在の流行株は変異を有している)。H3N2では166番目のアミノ酸の変異後、大きな抗原性の変化が連続して起きているため、A(H1N1)pdm09でもこれから抗原性の変化が起きてくるのではないか。
また、Trevor Bedford先生が発表されたnextful.orgというサイトがとても便利そうです。HAの系統樹上でHI価を比較したり、変異の頻度を比較したりするのを簡単にできるようです。系統樹見ながらどこにアミノ酸変異が入っているかを一目でわかるだけでもとても便利だと思います。
<演題紹介>
- HA acid stability and the emergence of H1N1 pandemic influenza from swine
Marion Russier (St Jude Children’s Research Hospital)
H1N1pdm09においてHAが強酸性下(pH5.5<)で安定であることが、病原性とフェレットでのトランスミッションに重要であることが示されている。筆者らは、HAが酸性下で安定であることが異種間での感染に重要ではないかと考え、実験を行った。酸性下で不安定になる変異を導入したpH1N1ウイルス(pH1N1-Y17H(pH6.0で活性化する))とWT-pH1N1を用い、ブタとブタのトランミットおよびブタとフェレットのトランミットの実験を行い、HAの酸性安定性が異種間の感染に重要であるか検証した。その結果、ブタ同士だと、酸性において不安定なpH1N1-Y17Hにおいても増殖・トランスミットでき、変異も維持されている。一方で、ブタからフェレットにトランスミットしたpH1N1-Y17Hは、アミノ酸変異(HA1: Y17H+V55I, HA2: R106K+K153E+V192A(すべてステム領域のアミノ酸))を獲得し、酸性下で安定になっていた。
このことから、HAの酸性安定性は宿主への適応に重要である。さらに異種間の感染に酸性安定性が重要であることが考えられ、それらに関与するアミノ酸をモニターすることはヒトでのパンデミックを予測する上で重要であると考えられる。 - Loss of Fitness in Mammalian Cells imposed by the NS1 Protein from Bat Influenza-like Viruses
Teresa A. Aydillo Gomez (Icahn School of Medicine at Mount Sinai)
近年コウモリからHL17NL10とHL18NL11が分離された。いまだHAのレセプターも解明されておらず、ヒトへの感染の可能性も明らかになっていない。筆者らは、感染には宿主応答(特にIFN応答)を回避することが重要であると考え、宿主応答を抑えるNS1タンパク質に着目し、HL17NL10とHL18NL11のNS1タンパク質の機能を明らかにすることを目的として研究を行った。HL17NL10とHL18NL11由来のNS1タンパク質をもつPR8ウイルス(PR8-NS1HL17とPR8-NS1HL18)をリバースジェネティクスにより作製し、マウス肺でのウイルス増殖と病原性をみている。その結果、マウスにおいて、PR8-NS1HL17とPR8-NS1HL18はWTと比べてウイルス力価が低下し、病原性の低下がみられた。そこで、STAT1欠損マウスを用いて同様の実験を行うと、PR8-NS1HL17とPR8-NS1HL18は野生型PR8と同様の増殖を示した。さらに、マウスで継代すると7回と5回目の継代でPB2に変異がみられ、それにより野生型マウスでの病原性を獲得した。
このことから、PR8-NS1HL17とPR8-NS1HL18はNS1タンパク質によるIFN応答の阻害が弱体化しているため、病原性が低下していると考えられる。PB2タンパク質への変異獲得によりマウスでの病原性を獲得することから、HL17NL10とHL18NL11がコウモリ以外の哺乳類でも病原性を獲得する可能性が示唆された。 - Role of Neuraminidase in Influenza A(H7N9) Receptor Binding
Donald Benton (Tne Francis Crick Institute)
H7N9-NAのレセプター結合能を検証していた。精製したN9-NAを用いてα2,3およびα2,6結合したシアル酸に対する結合を確認したところ、secondary haemadsorption siteを介しては、α2,3およびα2,6結合したシアル酸の両方への結合を示したのに対し、sialidase siteを介した場合だとα2,6結合したシアル酸への結合が強いことが明らかとなった。さらに、α2,6結合したシアル酸の切断能が弱いことがヒトでの感染効率を下げているのではないかと考察している。
D1 安原 敦洋