Toll様受容体9のN末端フラグメントは受容体の応答に重要である
Toll様受容体9のN末端フラグメントは受容体の応答に重要である
Toll様受容体9 (TLR9) は病原体由来のDNAを認識する受容体です.宿主および病原体由来のDNAは構造的に類似しているためTLR9は自己と非自己由来の核酸の識別が困難なことが分かっております.宿主由来の自己DNAに対する自己免疫応答を避けるために,TLR9は自己DNAに暴露されにくいエンドリソソームなどの細胞内小器官に局在し,そこでシステインプロテアーゼなどにより細胞外ドメインのN末端フラグメント (TLR9N) が切り離されたC末端側の受容体 (TLR9C) が下流へシグナルを伝達できるとされてきました.すなわちTLR9による自己免疫応答の制御はTLR9の細胞内局在,リガンドの選択的な輸送,細胞内器官でのTLR9の修飾により反応を適切な場に制御することで可能とされてきました.しかし,内因性のTLR9やTLR9Nの役割に対する詳細な検討はされていませんでした.
われわれは,マウスTLR9に対する新規モノクローナル抗体を作成し詳細な解析を行ったところ,主に脾臓由来の樹状細胞の表面にはTLR9が多く発現することが証明されました.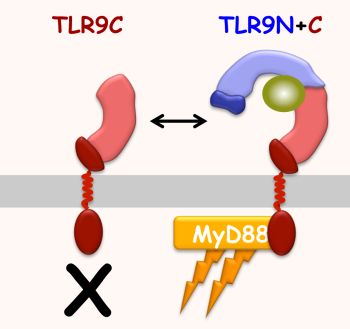 Pro-B細胞株においてTLR9はUnc93B1の発現量に依存して,細胞表面に局在することが分かりました.さらに,共焦点顕微鏡解析によって樹状細胞の内因性TLR9はほとんど小胞体の外に存在し,TLR9は切断された後もTLR9NはTLR9Cと直接結合していることをウェスタンブロットにて証明しました.TLR9Nの機能を解析するためにTLR9を欠損させた樹状細胞にTLR9C単独あるいはTLR9CとTLR9Nを共発現させて,TLR9依存的な応答を解析しました.TLR9C単独では応答せず,TLR9CとTLR9Nを共発現させるとはじめてTLR9のリガンドに応答してサイトカインが産生されました.
Pro-B細胞株においてTLR9はUnc93B1の発現量に依存して,細胞表面に局在することが分かりました.さらに,共焦点顕微鏡解析によって樹状細胞の内因性TLR9はほとんど小胞体の外に存在し,TLR9は切断された後もTLR9NはTLR9Cと直接結合していることをウェスタンブロットにて証明しました.TLR9Nの機能を解析するためにTLR9を欠損させた樹状細胞にTLR9C単独あるいはTLR9CとTLR9Nを共発現させて,TLR9依存的な応答を解析しました.TLR9C単独では応答せず,TLR9CとTLR9Nを共発現させるとはじめてTLR9のリガンドに応答してサイトカインが産生されました.
これらの結果はTLR9が切断された後にTLR9NとTLR9Cが結合した構造体こそがDNAに応答する受容体であることを証明しました.
本研究は、東京大学医科学研究所炎症免疫分野の清野宏教授と同研究室のスタッフ、岡山大学大学院医歯薬総合研究科消化器・肝臓内科学の山本和秀教授らの協力を得て行いました。
