TLR3の阻害が致死的な放射線誘導性腸炎を著しく改善させる
TLR3の阻害が致死的な放射線誘導性腸炎を著しく改善させる
急性放射線症候群は、高線量の電離放射線に曝露後に起こる急性疾患である。急性放射線症候群では、各臓器の放射線に対する感受性に従って様々な症状が出現する。1.5 Gy以上の全身被曝では、体内で最も感受性の高い造血幹細胞が傷害され、血小板や白血球の供給が途絶えるために出血傾向と免疫力低下が誘導される(造血症候群)。5 Gy以上では、腸管傷害が誘導され、下痢、吸収低下、細菌性腸炎によって亜急性に死亡する(消化管症候群)。消化管症候群は、陰窩の上皮幹細胞が細胞死を起こす事によって起こるというのが定説である。電離放射線が、宿主のDNAを傷害すると、癌抑制遺伝子のp53が細胞周期を停止させ、DNA修復を行う。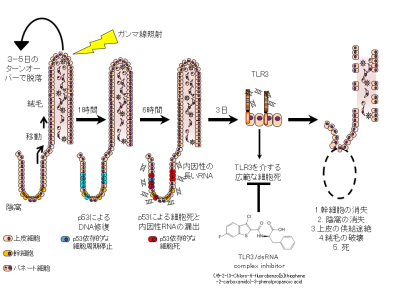 もしDNA傷害が不可逆的ならば、p53はアポトーシスを誘導する。放射線誘導性の細胞死を阻害する薬剤が消化管症候群の治療に効果的だと思われるが、p53阻害剤の治療応用はDNA修復にまで影響を及ぼすため現実的でない。Toll-like receptorファミリーは自然免疫の代表的な受容体で、様々な微生物由来の成分を認識して自然免疫応答を誘導する。我々は、TLR3欠損マウスが急性放射線症候群に抵抗性を示す事を見出した。造血症候群に関しては変化は無かったが、TLR3欠損マウスは致死率、下痢、体重減少といった消化管症候群の症状が有意に軽度であった。放射線で誘導される陰窩の細胞死がTLR3欠損マウスでは抑制されており、そのため生き残った陰窩から上皮が供給されたため絨毛構造は破綻せずに生存できることが明らかになった。興味深いことに、p53による細胞死はTR3欠損マウスでは正常に起こっていた。p53依存的に細胞死を起こした細胞から自己のRNAが漏出しており、それがTLR3を介して広範な陰窩の細胞死を誘導していることが明らかになった.最近TLR3-RNA結合阻害剤((R)-2-(3-chloro-6-fluorobenzo [b] thiophene-2-carboxamido)-3-phenylpropanoic acid)が発売された。この阻害剤は、陰窩の細胞死を抑制し、致死率も顕著に改善した。従って、TLR3の活性化阻害は、GISの新しい治療標的となることが明らかになった。
もしDNA傷害が不可逆的ならば、p53はアポトーシスを誘導する。放射線誘導性の細胞死を阻害する薬剤が消化管症候群の治療に効果的だと思われるが、p53阻害剤の治療応用はDNA修復にまで影響を及ぼすため現実的でない。Toll-like receptorファミリーは自然免疫の代表的な受容体で、様々な微生物由来の成分を認識して自然免疫応答を誘導する。我々は、TLR3欠損マウスが急性放射線症候群に抵抗性を示す事を見出した。造血症候群に関しては変化は無かったが、TLR3欠損マウスは致死率、下痢、体重減少といった消化管症候群の症状が有意に軽度であった。放射線で誘導される陰窩の細胞死がTLR3欠損マウスでは抑制されており、そのため生き残った陰窩から上皮が供給されたため絨毛構造は破綻せずに生存できることが明らかになった。興味深いことに、p53による細胞死はTR3欠損マウスでは正常に起こっていた。p53依存的に細胞死を起こした細胞から自己のRNAが漏出しており、それがTLR3を介して広範な陰窩の細胞死を誘導していることが明らかになった.最近TLR3-RNA結合阻害剤((R)-2-(3-chloro-6-fluorobenzo [b] thiophene-2-carboxamido)-3-phenylpropanoic acid)が発売された。この阻害剤は、陰窩の細胞死を抑制し、致死率も顕著に改善した。従って、TLR3の活性化阻害は、GISの新しい治療標的となることが明らかになった。
