骨格筋におけるグルココルチコイドレセプターの標的遺伝子同定と筋委縮の分子機構解明 -副腎皮質ステロイドホルモンの副作用の仕組みを解明し新しい治療法を開発-
骨格筋におけるグルココルチコイドレセプターの標的遺伝子同定と筋委縮の分子機構解明 -副腎皮質ステロイドホルモンの副作用の仕組みを解明し新しい治療法を開発-
【背景】 骨格筋は身体の40%以上を占める臓器であり、姿勢保持、運動、そして栄養の貯留と供給など、生きていく上で重要な役割を担っています。成人の骨格筋量は主として筋細胞内のタンパク質の合成速度と分解速度のバランスによって調節されています。病気や薬剤などによってそのバランスが破綻すると筋萎縮が起こり、移動能力の低下、転倒骨折リスクの上昇、病臥の長期化とさらなる筋萎縮の進行という負のスパイラル(悪循環)に至ることも稀ではありません。超高齢化社会に向かう現在、筋萎縮の病態解明と治療法開発は喫緊の課題です。
膠原病などの代表的治療薬である副腎皮質ステロイドホルモン-グルココルチコイドーの作用と副作用は不可分であり、しばしば「諸刃の剣」に例えられます。ここで、タンパク代謝に関してグルココルチコイドには異化(分解促進)作用と抗同化(合成抑制)作用が存在することが知られています。その結果、薬理量のグルココルチコイド投与時に筋萎縮・筋力低下が起こることは稀ではありませんが、教科書的には軽微な副作用に分類されていました。しかし、膠原病患者さんを対象とした調査によって、潜在的に筋萎縮と筋力低下に悩む患者さんは決して少なくなく、積極的医療介入対象とはなっていない実態がクローズアップされました。
骨格筋において、他の組織と同様に、グルココルチコイドの作用は細胞内の転写因子であるグルココルチコイドレセプター(GR)と結合することによって発現されます。したがって、GRが様々な遺伝子の発現量を調節した結果として筋萎縮が起こると考えられますが、筋萎縮発症の鍵となるGR標的遺伝子や、タンパク質の分解促進・合成抑制のメカニズムは不明でした。
【研究成果】 今回、GR標的遺伝子の網羅的探索手法を骨格筋に応用して新しいGR標的遺伝子を同定し、国立精神・神経医療研究センター、味の素製薬、慶應義塾大学医学部との共同研究によってグルココルチコイド筋萎縮の分子機構を解明したとともに、新規治療法のプロトタイプとして分岐鎖アミノ酸(BCAA)によるmTORC1活性化療法を開発しました。
第一にGRは複数の標的遺伝子の発現を介して筋萎縮を引き起こすことを解明しました。すなわち、GRは同じく転写因子であるKLF15遺伝子の発現上昇を介して、玉突き式にKLF15が標的とする多くの筋萎縮関連遺伝子発現を増強します。これらの筋萎縮関連遺伝子には、ユビキチンープロテアソーム系を介してタンパク質分解を促進するはたらきを持つものと、BCAA分解を促進するはたらきを持つものが含まれます。細胞内のBCAA濃度の低下は、栄養のセンサーでありタンパク質合成促進の鍵因子でもあるmTORC1の活性低下を引き起こします。一方、GRはmTORC1抑制タンパク質であるREDD1遺伝子をも標的としてその発現を上昇させます。つまり、GRは骨格筋タンパク質の分解亢進と合成低下に関与する多数の遺伝子発現を協調的にコントロールして筋萎縮を引き起こすことがわかったのです。生理的には、栄養の貯蔵と供給も骨格筋の重要なはたらきであることを考えると、飢餓などのストレスを受けた際にGRは骨格筋から重要臓器に栄養を再分配する上できわめて効率的な役割を果たすといえます。
第二に、mTORC1はGRに拮抗してグルココルチコイドによる筋萎縮を抑制することがわかりました。骨格筋が栄養を感知するとmTORC1はタンパク質合成を促進すると同時にGRの働きを抑えて標的遺伝子の発現を転写レベルで低下させ筋萎縮に拮抗するのです。
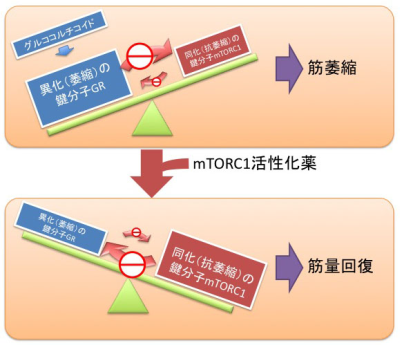
このように、mTORC1とGRという、同化促進と異化亢進という各々相反する性質を持った骨格筋量制御の鍵分子同士が多段階的にお互いの活性を抑制し合うことでバランスをとるという、きわめて巧妙な筋量制御の仕組みを紐解くことができました。グルココルチコイド療法の場合、生理的必要量を遙かに超える量のホルモンが投与されるため、この仕組みが破綻してバランスが異化に傾き、筋萎縮がおこります。私たちは、グルココルチコイド筋萎縮モデルラットにおいて、このバランスを是正するべく、mTORC1活性化作用を有するBCAAを投与しました。すると、mTORC1活性の回復、GRによる遺伝子発現の抑制が確認されたとともに、グルココルチコイドによる筋量減少と筋力低下を防止することができました(図参照)。
【治療への応用・今後の展開】 今回の研究は、骨格筋を例に、GRの標的遺伝子の網羅的探索がグルココルチコイドのはたらきや副作用のメカニズム解明とその治療法確立にきわめて有効な手段であることを示したといえます。今後、この手法が多くの臓器に応用されることによって、グルココルチコイドの副作用が克服されグルココルチコイド療法が進歩することを期待しています。
グルココルチコイドによる筋萎縮は臨床的には軽視される傾向がありますが、膠原病をはじめとしたグルココルチコイド治療を受ける患者さんの日常生活に与える影響は大きく、特に高齢者では骨折や感染などの合併症のリスク因子として重要なことは自明です。私たちの研究成果が臨床応用されることによって患者さんのQOLが改善されるとともにこれらのリスクが回避され、疾患自体の治療にも貢献することを期待します。また、最近、糖尿病などの慢性疾患に伴う筋萎縮、廃用性筋萎縮(潜在患者数は数百万人)においても、GRの関与が示唆されています。したがって、私たちの研究成果とその実用化は多方面に波及効果を有する可能性もあると考えます。新しい治療法の開発が疾患の臨床に変革をもたらすことは骨粗鬆症などの歴史が如実に示しています。今回の成果によって筋萎縮の系統的かつ基礎疾患横断的な研究の進展と臨床への展開が加速化されることを期待します。
現在、BCAAを含有する機能性食品を含む膨大な数の民間療法が筋力増強作用をうたい、一定の市場を形成しています。しかし、そのほとんどが健康人、アスリートを対象にしたものであり、本来筋力を増強されるべき疾患に苦しむ患者さんを対象にしたものではありません。このゆがんだ状況を是正するためにも、一日も早く科学的なエビデンスを有する筋萎縮治療を確立して医療的介入を可能にしなくてはならないと考えます。私たちは今回の研究成果を臨床に橋渡しするべく、東京大学医科学研究所附属病院においてグルココルチコイド筋萎縮患者を対象とした臨床試験を計画しています。
