腫瘍壊死因子ファミリーのレセプターであるRANKとCD40は胸腺髄質の環境と自己免疫寛容を協調して制御する
腫瘍壊死因子ファミリーのレセプターであるRANKとCD40は胸腺髄質の環境と自己免疫寛容を協調して制御する
国民の3人に1人はアレルギーや自己免疫疾患などのいわゆる免疫病に罹患していると言われています。これらの免疫病は、本来は無害な物質に対して免疫反応が起きてしまうことが原因の1つとされています。健康な人間の体には、自分の組織や無害な異物に対して免疫反応が起きないようにする機構(免疫寛容)が備わっており、この免疫寛容に異常が起きた状態を免疫病と考えることができます。そのため、免疫寛容を制御する機構について明らかにすることは、アレルギーや自己免疫疾患の原因解明、治療に重要であると考えられています。
免疫寛容を制御する組織の1つが胸腺です。胸腺はリンパ球の一つであるTリンパ球を産生する器官ですが、その際同時に自分の組織に反応するTリンパ球を除去します(負の選択)。この負の選択を調節している細胞として、胸腺髄質上皮細胞が注目されています。私たちは以前に胸腺髄質上皮細胞の分化がシグナル伝達因子の1つであるTRAF6により制御され、その異常は自己免疫を誘導することを報告しました(Science、 2005、詳細は本サイト内で紹介しています)。TRAF6はTNFレセプターファミリーなど細胞表面レセプターからのシグナルを伝達して、転写因子NF-kBを活性化する因子です。しかしながら胸腺髄質上皮細胞ではどの細胞表面レセプターがTRAF6へシグナルを伝えるのかが不明でした。
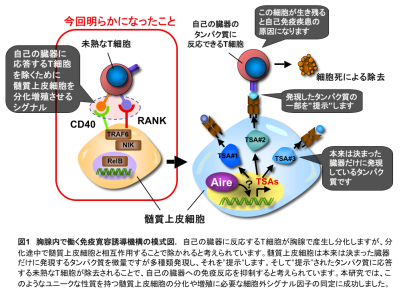 私たちはそのレセプターを同定するために、未熟な胸腺髄質上皮細胞を含む胎仔胸腺ストローマ(胸腺からリンパ球などを除いたもの)に発現するTNFレセプターファミリーの発現を検討し、候補としてReceptor activator of NF-kB (RANK)とCD40に絞りました。次にそれを検証するためにRANKリガンド(RANKL) とCD40の各欠損マウスおよびRANKLとCD40の2重欠損マウスの胸腺を調べました。その結果、RANKL, CD40各欠損マウスでは、成熟した胸腺髄質上皮細胞の分化は部分的に異常であり、両方を欠損するマウスでは分化が全く起きないことを発見しました。さらに組み替えRANKLやCD40Lタンパク質の存在下に胸腺ストローマをin vitro培養すると、成熟した胸腺髄質上皮細胞へ分化することが分かりました。さらにそのin vitro分化には、TRAF6などこれまで胸腺髄質上皮細胞の分化に必要であると考えられていた因子を必要としました。同時に共同研究として、RANKLやCD40Lは未熟なTリンパ球が発現していることも見つけています (Immunity 28, 438)。
私たちの今回の発見で、免疫寛容の誘導に必要な髄質上皮細胞の分化を制御するサイトカインシグナルが明らかとなりました(図)。髄質上皮細胞はいろいろな自己組織抗原を異所的に発現することで、自己免疫寛容を制御すると考えられています。今回の発見は、髄質上皮細胞が持つこの特殊な性質を利用して免疫寛容機構を制御し、免疫病の治療に役立てるための大きな一歩になることが期待されます。(この研究成果は9月29日付け朝日新聞朝刊でも紹介されました)
私たちはそのレセプターを同定するために、未熟な胸腺髄質上皮細胞を含む胎仔胸腺ストローマ(胸腺からリンパ球などを除いたもの)に発現するTNFレセプターファミリーの発現を検討し、候補としてReceptor activator of NF-kB (RANK)とCD40に絞りました。次にそれを検証するためにRANKリガンド(RANKL) とCD40の各欠損マウスおよびRANKLとCD40の2重欠損マウスの胸腺を調べました。その結果、RANKL, CD40各欠損マウスでは、成熟した胸腺髄質上皮細胞の分化は部分的に異常であり、両方を欠損するマウスでは分化が全く起きないことを発見しました。さらに組み替えRANKLやCD40Lタンパク質の存在下に胸腺ストローマをin vitro培養すると、成熟した胸腺髄質上皮細胞へ分化することが分かりました。さらにそのin vitro分化には、TRAF6などこれまで胸腺髄質上皮細胞の分化に必要であると考えられていた因子を必要としました。同時に共同研究として、RANKLやCD40Lは未熟なTリンパ球が発現していることも見つけています (Immunity 28, 438)。
私たちの今回の発見で、免疫寛容の誘導に必要な髄質上皮細胞の分化を制御するサイトカインシグナルが明らかとなりました(図)。髄質上皮細胞はいろいろな自己組織抗原を異所的に発現することで、自己免疫寛容を制御すると考えられています。今回の発見は、髄質上皮細胞が持つこの特殊な性質を利用して免疫寛容機構を制御し、免疫病の治療に役立てるための大きな一歩になることが期待されます。(この研究成果は9月29日付け朝日新聞朝刊でも紹介されました)
