ピロリ菌は、消化管上皮の代謝回転をアポトーシス抑制により遅らせる。-胃で増殖するための細菌の戦略-
ピロリ菌は、消化管上皮の代謝回転をアポトーシス抑制により遅らせる。-胃で増殖するための細菌の戦略-
世界人口の半数以上が感染しているヘリコバクターピロリ菌 (Helicobacter pylori)は、胃粘膜に長期間持続感染して、胃炎、胃潰瘍、胃MALTリンパ腫、胃ガンを誘発する。ピロリ菌が感染する消化管上皮細胞は絶えず新生と死を繰り返し、数日以内で入れ替わる。粘膜病原細菌の感染の足場である上皮細胞の迅速なターンオーバーは、宿主感染防御システムとして重要である。
本研究では、ピロリ菌が胃粘膜上皮細胞内へ分泌するCagAタンパク質が、アポトーシス細胞死の抑制因子であるMCL1タンパク質の発現を促進することにより、胃粘膜の細胞死を抑制し、その結果、上皮細胞のターンオーバーを遅らせることを明らかにした。
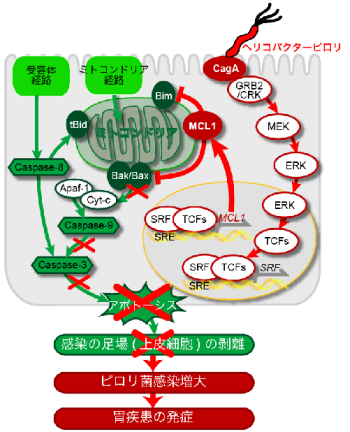 スナネズミにアポトーシス誘導剤を経口投与することで、胃粘膜上皮細胞のターンオーバーを観察しやすくすると、CagAを分泌するピロリ菌が感染したスナネズミでは、アポトーシスが抑制されることを見いだした。分子レベルでの解析の結果、CagAは、宿主のアダプタータンパク質であるGRB2やCRKと結合してERKキナーゼを活性化させることにより、ミトコンドリアに存在してアポトーシス抑制因子として作用するMCL1の発現を促進することが判明した。また、スナネズミの胃に定着した菌数を測定すると、野生型ピロリ菌を投与した場合には、CagAがない菌の場合よりも多数の菌が検出された。つまり、CagAを分泌するピロリ菌は、MCL1の発現を促進することで、胃粘膜感染の足場となる表層上皮細胞のアポトーシスによる剥離を抑制して、長期持続感染を成立させることが明らかになった。
スナネズミにアポトーシス誘導剤を経口投与することで、胃粘膜上皮細胞のターンオーバーを観察しやすくすると、CagAを分泌するピロリ菌が感染したスナネズミでは、アポトーシスが抑制されることを見いだした。分子レベルでの解析の結果、CagAは、宿主のアダプタータンパク質であるGRB2やCRKと結合してERKキナーゼを活性化させることにより、ミトコンドリアに存在してアポトーシス抑制因子として作用するMCL1の発現を促進することが判明した。また、スナネズミの胃に定着した菌数を測定すると、野生型ピロリ菌を投与した場合には、CagAがない菌の場合よりも多数の菌が検出された。つまり、CagAを分泌するピロリ菌は、MCL1の発現を促進することで、胃粘膜感染の足場となる表層上皮細胞のアポトーシスによる剥離を抑制して、長期持続感染を成立させることが明らかになった。
写真:スナネズミ胃粘膜上皮細胞のアポトーシス
(左)アポトーシス誘導剤を投与しない場合は、胃表層の上皮細胞に、緑色で示すアポトーシスを起こした細胞が見られる。
(右)アポトーシス誘導剤であるエトポシドを経口投与すると、胃表層の多くの細胞がアポトーシスを起こし(緑色)、剥離する。
