がん細胞の浸潤性転換を制御するPI3K-PKCaphaシグナルの解明
がん細胞の浸潤性転換を制御するPI3K-PKCaphaシグナルの解明
がん細胞は周辺組織に浸潤する能力が亢進しており、その結果として遠隔臓器に転移する。転移したがんの治療は困難であり、がん死の主たる原因となっている。がん細胞は、生体内ではコラーゲンを中心とした細胞外基質と呼ばれる生体高分子が構成するマトリックス中に埋もれた状態で存在している。このような環境の中で、がん細胞が増殖し、浸潤するためには細胞外基質に接着するとともに、それを壊す能力が必要とされる。安定な細胞接着は浸潤を困難にするが、接着能の適度な低下と細胞外基質分解活性の亢進はがん細胞の浸潤を促進する。細胞の細胞外基質への接着には、接着斑と呼ばれる構造体形成が知られてる。一方で、浸潤の際には細胞外基質分解酵素を持つ浸潤突起形成が特徴的に観察される。
今回の研究では、接着斑と浸潤突起形成に関与する因子および制御シグナルの部分的類似性に着目して、がん細胞には安定した細胞接着から動的な浸潤への転換を促進する仕組みがあると推定して、浸潤スイッチとして機能する新しいシグナル系の同定を試みた。まず、文献情報およびタンパク質間相互作用情報に基づくオントロジー解析の新規手法の構築と解析により、浸潤制御に関与するシグナル系を推定した(図1)。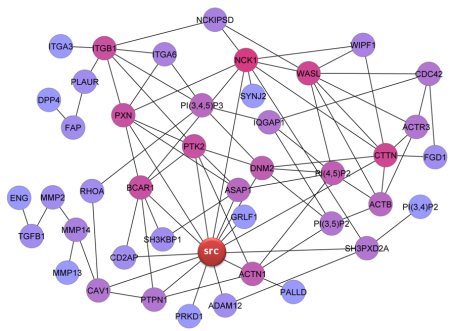 さらには、頭頸部がんの転移巣を原発巣の臨床材料を用いたリン酸化タンパク質に対するシグナルアレイ解析を行って、PI3K-highとPKCa-lowの状態が浸潤性・転移性と相関することを見出した。がん細胞株を用いて、PI3KとPKCaの細胞レベルを操作することにより、実際にがん細胞の浸潤突起形成と接着斑形成が制御されることを証明した。PI3K経路の亢進によってがん細胞の浸潤が亢進する一方で、PKCaからはPI3Kのリン酸化を介してフィードバック制御がかかることも明らかにした(図2)。
さらには、頭頸部がんの転移巣を原発巣の臨床材料を用いたリン酸化タンパク質に対するシグナルアレイ解析を行って、PI3K-highとPKCa-lowの状態が浸潤性・転移性と相関することを見出した。がん細胞株を用いて、PI3KとPKCaの細胞レベルを操作することにより、実際にがん細胞の浸潤突起形成と接着斑形成が制御されることを証明した。PI3K経路の亢進によってがん細胞の浸潤が亢進する一方で、PKCaからはPI3Kのリン酸化を介してフィードバック制御がかかることも明らかにした(図2)。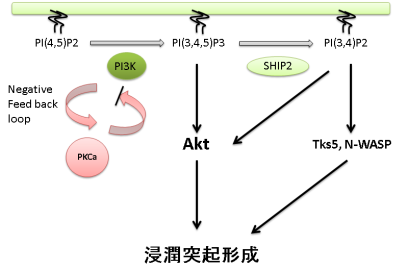 また、がん細胞はPI3Kの経路にしばしば遺伝子異常を持つことが知られている。このPI3K経路の遺伝子異常の有無により、PKCaからのフィードバック制御が異なる効果を与えることも見出した。この発見に基づいて、PI3K/PKCa経路の阻害剤をがん治療に応用するに際しては、単に分子標的を点としてとらえるだけでは不十分であり、がんシステム制御の観点から治療戦略を構築する必要があることを提唱した。
また、がん細胞はPI3Kの経路にしばしば遺伝子異常を持つことが知られている。このPI3K経路の遺伝子異常の有無により、PKCaからのフィードバック制御が異なる効果を与えることも見出した。この発見に基づいて、PI3K/PKCa経路の阻害剤をがん治療に応用するに際しては、単に分子標的を点としてとらえるだけでは不十分であり、がんシステム制御の観点から治療戦略を構築する必要があることを提唱した。
筆頭著者の星野大輔助教は、H23年度の日本学術振興会「組織的な若手研究者等海外派遣プログラム」による支援でヴァンダービルド大学に5か月間滞在し、今回の共同研究がスタートした。
