概要
理化学研究所(理研)生命医科学研究センター基盤技術開発研究チームの笹川甫研究パートタイマーI(研究当時、現研修生、現秋田大学大学院医学系研究科腎泌尿器科学講座大学院生)、桃沢幸秀チームディレクター(生命医科学研究センター副センター長)、東京大学医科学研究所附属ヒトゲノム解析センターシークエンス技術開発分野の松田浩一特任教授(同大学大学院新領域創成科学研究科メディカル情報生命専攻クリニカルシークエンス分野教授)、秋田大学大学院医学系研究科医学専攻腎泌尿器科学講座の羽渕友則教授(研究当時)、日本医科大学先端医学研究所分子生物学部門の村上善則特命教授、愛知県がんセンターがん予防研究分野の松尾恵太郎分野長らの国際共同研究グループは、乳がんや卵巣がんの発症リスクを高めることで知られるBRCA1とBRCA2(BRCA1/2)遺伝子における病的バリアント[1]が甲状腺がん、膀胱(ぼうこう)がん、頭頸部(とうけいぶ)がん、皮膚がんの発症リスクも上昇させることを明らかにしました。本研究成果により、BRCA1/2遺伝子のゲノム情報を用いたがん個別化医療がより幅広い形で進展することが期待されます。
今回、国際共同研究グループはBRCA1/2遺伝子について、バイオバンク・ジャパン[2]が保有している日本人集団におけるこれまで未解析である9種のがんについて、合計4万人以上を対象に、がん種横断的ゲノム解析を行いました。
本研究は、科学雑誌『ESMO Open』オンライン版(4月8日付)に掲載されました。
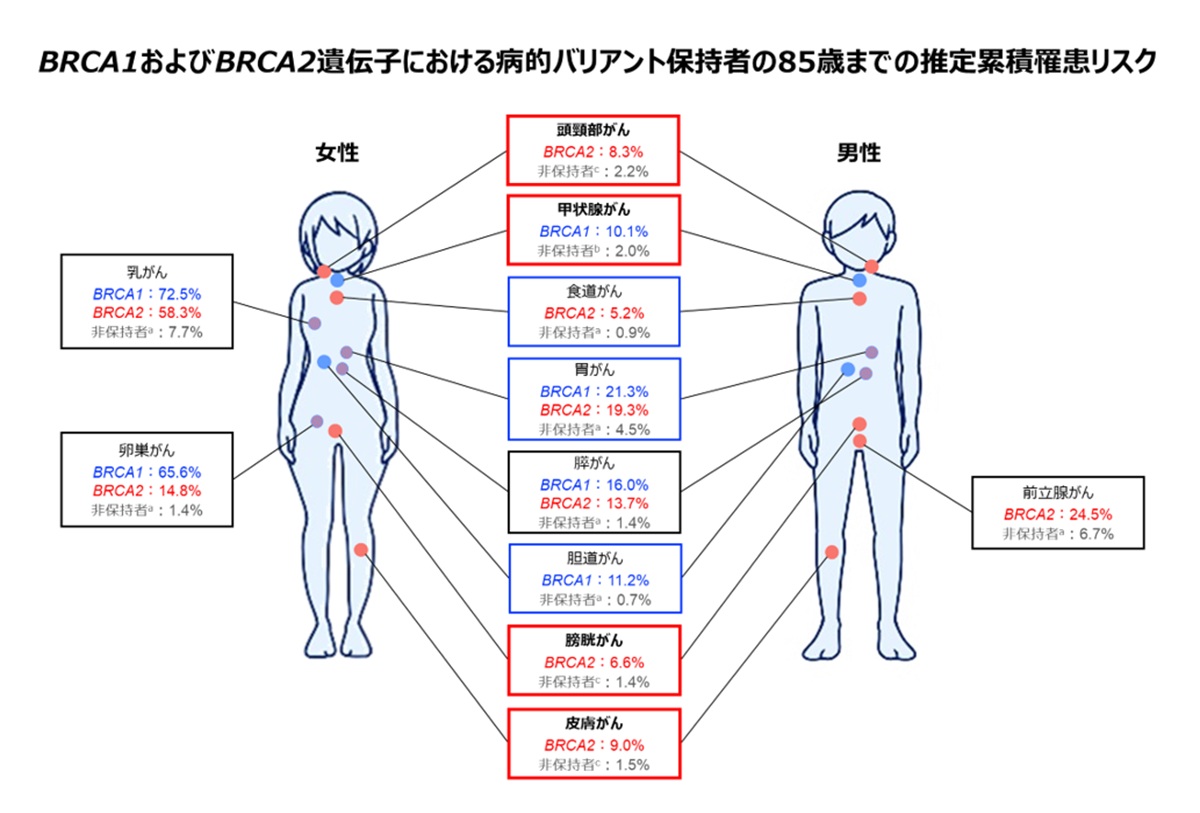
黒枠は本研究発表時点において、ゲノム情報を用いた医療が保険医療の対象となっているがん種、青枠は2022年の研究(Momozawa et al.JAMA Oncol 2022)で新たに関連を報告したがん種、赤枠は今回の研究で新たに関連を報告したがん種を示しています。累積罹患リスクは、すべてバイオバンク・ジャパンのデータをもとに算出した推定値であり、各個人の発症確率を直接示すものではありません。また、統計学的に有意な関連が報告されているがん種と遺伝子の組み合わせのみを示しています。そのため、記載がないがん種および遺伝子について、リスクがないことを意味するものではありません。病的バリアント非保持者の定義については、aBRCA1およびBRCA2の病的バリアント非保持者、bBRCA1の病的バリアント非保持者、cBRCA2の病的バリアント非保持者と、研究ごとに異なります。
背景
がんは遺伝と環境の両要因により発症すると考えられていますが、一部のがんはゲノム配列上のたった1カ所の配列の違い(遺伝的バリアント)により発症リスクが大きく上昇することが知られています。その代表的な原因遺伝子としてBRCA1とBRCA2(BRCA1/2)があり、これらの遺伝子に病気の原因となる病的バリアントが存在すると、乳がんや卵巣がんなどを発症しやすくなります。BRCA1/2遺伝子に病的バリアントを持つ乳がん患者と卵巣がん患者には、分子標的薬であるPARP阻害薬[3]の治療効果が高いことが分かっており、この治療は保険適用となっています。さらにその適用は、前立腺がんや膵(すい)がんにも拡大しています。2022年に、桃沢チームディレクターらはBRCA1/2遺伝子がこれらのがんに加えて、食道がん、胆道がん、胃がんの発症リスクと関連することを明らかにしました注1)。病的バリアントに基づいて一人一人に適した治療を行うがん個別化医療において、保険適用範囲をさらに拡大させるためには、より多くのがん種における遺伝情報を明らかにすることが必要です。これは、治療選択肢が限られているまれながん種においても、さらなる治療戦略の発展につながります。
そこで、国際共同研究グループはバイオバンク・ジャパンが保有しているDNAサンプルを用いて、新たに9種のがんについて、BRCA1/2遺伝子のゲノム解析を行いました。
注1)2022年4月15日プレスリリース「10万人以上を対象としたBRCA1/2遺伝子の14種のがんを横断的解析」
https://www.riken.jp/press/2022/20220415_1/index.html
研究手法と成果
理研が独自に開発したターゲットシークエンス法[4]を用いて、BRCA1/2遺伝子のタンパク質への翻訳に影響が大きいとされる翻訳領域およびその周辺2塩基の合計16,111塩基の配列を、42,331人について調べました。その結果、41,742人(約98.6%)の十分なシークエンスデータが取得でき、994個の遺伝的バリアントを同定しました。さらに、世界標準とされるENIGMAコンソーシアム[5]における基準を用いて、これらの遺伝的バリアントから105個の病的バリアントを同定しました。ほとんどの病的バリアントは、タンパク質合成がその変異箇所で停止することなどで機能が低下する機能欠失バリアントでした。
病的バリアントの保持率について症例群と対照群を比較することで、どのがんになりやすいかの「疾患リスク」を計算することができます。統計学的な検定を行った結果(表1)、BRCA1遺伝子の病的バリアントと有意な関連を示したがんは、甲状腺がんでした。また、BRCA2遺伝子の病的バリアントと有意な関連を示したがんは、膀胱がん、頭頸部がん、皮膚がんでした。
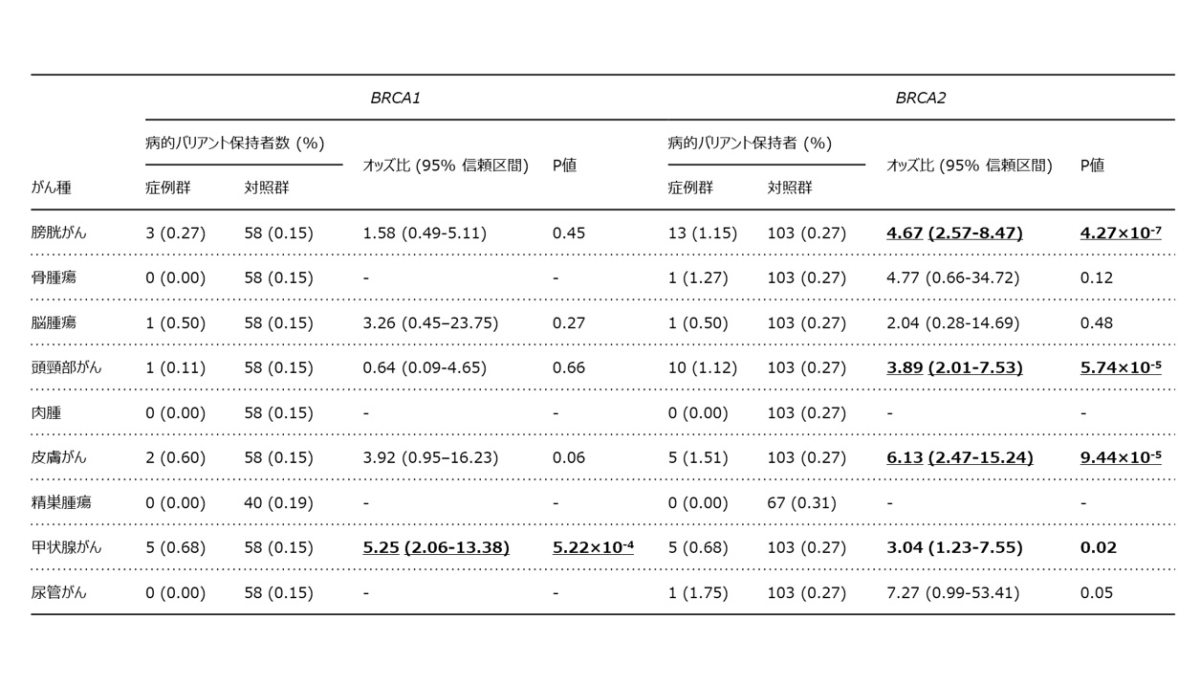
各がん種における病的バリアント保持者数(%)、対照群と比較することで算出される疾患リスク(オッズ比:「ある事象の起こりやすさ」を表す)、その95%信頼区間、P値(偶然にそのようなことが起こる確率)を示す。P<0.05のものは太字で示し、本研究におけるP値の基準(P=2.78x10-3)を下回ったがん種には、さらに下線も示した。また、サンプル数不足により計算できなかったがん種は、ハイフン(‐)で示した。BRCA1遺伝子では甲状腺がんが、BRCA2遺伝子では膀胱がんと頭頸部がんと皮膚がんが関連することが分かった。さらに、P<0.05ではBRCA2遺伝子で甲状腺がんとの関連が認められた。
発症リスクに性別による違いがあるとされている甲状腺がんや膀胱がん、頭頸部がんについて、性別ごとに疾患リスクを算出しました(図1)。膀胱がんにおいては、女性で23.6倍(95%信頼区間9.8~57.2)、男性で2.4倍(95%信頼区間1.0~5.5)と男女間の差について統計学的に有意な違いを認めました(P=2.15×10-4)。
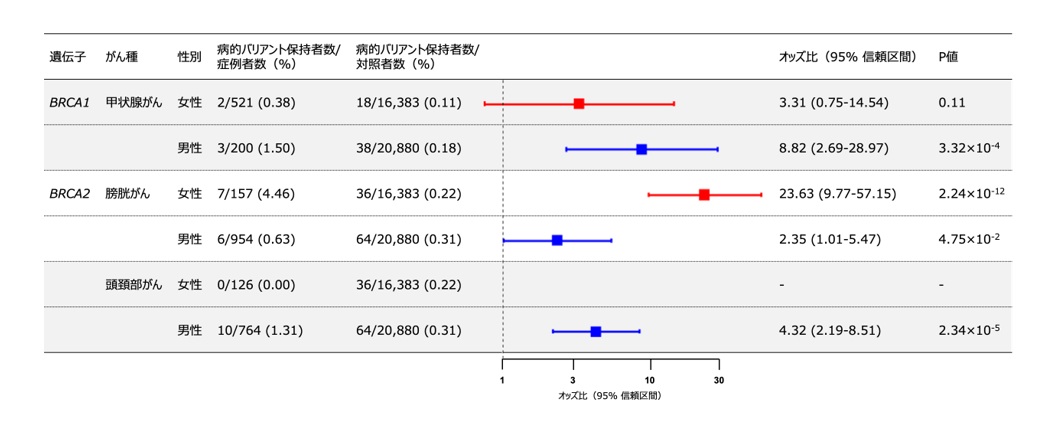
本研究でBRCA1/2遺伝子と関連を認めたがん種のうち、発症リスクに性別による違いがあるとされているがん種について性別ごとに疾患リスクを算出した。また、サンプル数不足により計算できなかったがん種は、ハイフン(‐)で示した。膀胱がんにおいては、女性で23.6倍(95%信頼区間9.8~57.2)、男性で2.4倍(95%信頼区間1.0~5.5)と男女間の差について統計学的に有意な違いを認めた(P=2.15×10-4)。
何歳までにどのくらいの確率でがんを発症する可能性があるかを示す累積リスク[6]は、実際の診療において、非常に重要な情報です。そこで、国立がん研究センターがん情報サービス「がん統計」(全国がん登録)を基に、本研究で新たに関連を同定した甲状腺がん、膀胱がん、頭頸部がん、皮膚がんについて85歳までの累積リスクを算出しました。
BRCA1/2遺伝子に病的バリアントを持たない場合の累積リスクは、5%未満でした。BRCA1遺伝子に病的バリアントを持つ場合の累積リスクは、甲状腺がんで10.1%でした(図2A)。BRCA2遺伝子に病的バリアントを持つ場合の累積リスクは、膀胱がんで6.6%、頭頸部がんで8.3%(図2B)、皮膚がんで9.0%(図2C)でした。
また、膀胱がんの性別ごとの累積リスクは、女性で12.8%(図2D)、男性で5.6%(図2E)でした。
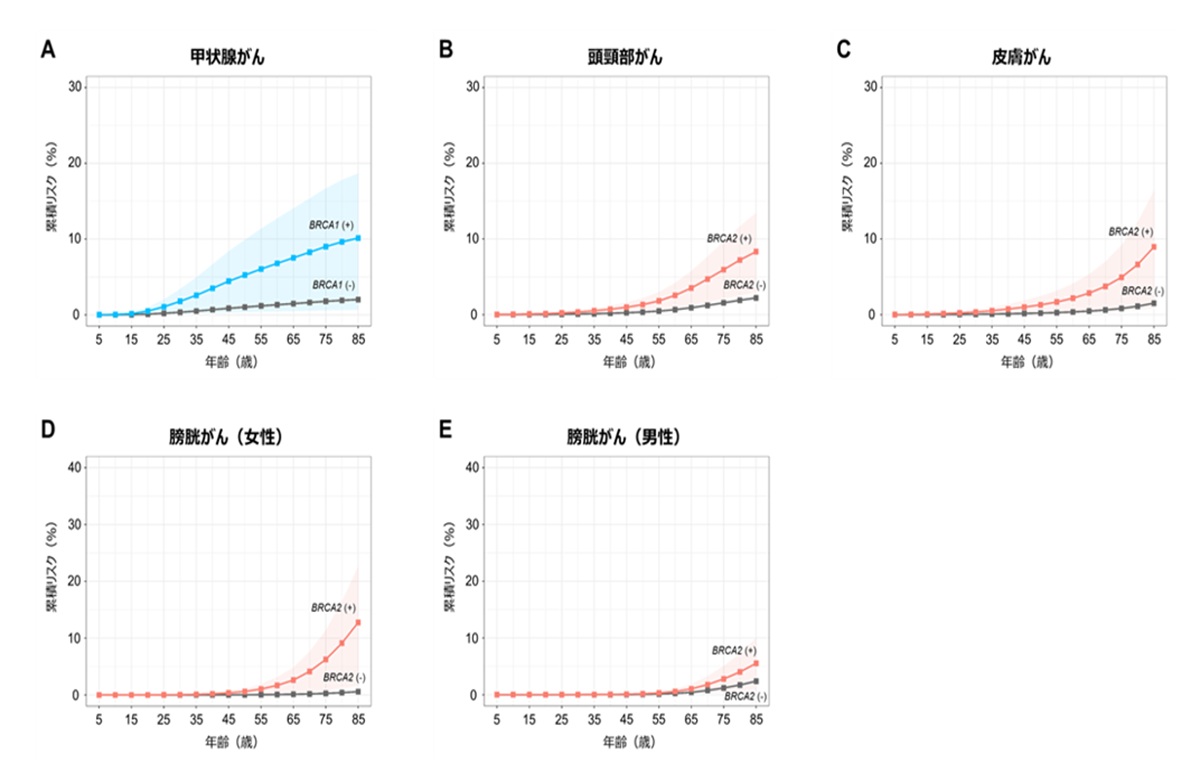
本研究でBRCA1/2遺伝子の病的バリアントと関連が認められたがん種について、各年齢までに発症するリスクを示した。BRCA1(-)はBRCA1遺伝子に病的バリアントを持たない人(灰色線)、BRCA2(-)はBRCA2遺伝子に病的バリアントを持たない人(灰色線)、BRCA1(+)はBRCA1遺伝子に病的バリアントを持つ人(青線)、BRCA2(+)はBRCA2遺伝子に病的バリアントを持つ人を示す(赤線)。
今後の期待
本研究では、9種のがんについて、BRCA1/2遺伝子のゲノム解析を行いました。今回の研究成果により、BRCA1遺伝子の病的バリアントが甲状腺がん、BRCA2遺伝子の病的バリアントが膀胱がん、頭頸部がん、皮膚がんの発症と関連していることが新たに明らかになりました。本研究成果は、これらのがん種に対するPARP阻害薬の適用拡大につながるような重要なエビデンスとなり、今後このようなデータが蓄積されることで、個別化医療のさらなる発展が期待されます。
患者・市民の皆さまへ
我々の研究では、BRCA1/2遺伝子の病的バリアントが乳がん、卵巣がん、前立腺がん、膵がんの4種のがんに加えて、胃がん、食道がん、胆道がんの3種のがんの発症リスクとの関連を2022年に明らかにしました。本研究は、これまで解析されていなかった9種のがんを対象に新たに解析を行い、甲状腺がん、膀胱がん、頭頸部がん、皮膚がんの発症リスクとの関連も明らかにしました。これらの結果は、バイオバンク・ジャパンにより収集された方々のデータを統計的に解析したものであるため、本結果だけを根拠に、これらのがん種注2)に対して新たに積極的なスクリーニング(サーベイランス、定期検査)やその他の治療などを行うことを推奨するものではありません。今後は、「どの方を対象に」、「どのタイミングで」、「どのような検査や治療が適切なのか」といった、より良質かつ適切な個別化医療について研究データを積み重ねるとともに、慎重に議論していく必要があります。
また、遺伝性乳がん卵巣がん症候群におけるがん未発症で家族歴のある方を対象とした遺伝学的検査やそれに伴う医学的管理が、2026年度の診療報酬改定において保険適用となる見込みです。これにより、将来の発症リスクを予測し、適切なスクリーニングや経過観察および医療提供体制の強化が期待されるとともに、本研究の成果も、このようなリスクに応じた適切な医療の実現に向けた基盤として、患者さんや一般の方々の健康に貢献するものと考えられます。
注2)各がん種についての情報は、以下のがん情報サービスリンクより参照してください。
https://ganjoho.jp/public/cancer/index.html
謝辞
本プレスリリースは、特定非営利活動法人クラヴィスアルクスの太宰牧子理事長、東京大学大学院新領域創成科学研究科の永井亜貴子特任助教、東京大学医科学研究所の河田純一特任研究員、理研生命医科学研究センター生命医科学倫理とコ・デザイン研究チームの佐藤桃子特別研究員、武藤香織チームディレクター(東京大学医科学研究所教授)からいただいたご意見も踏まえて作成いたしました。研究成果の適切な発信にご協力いただきましたことに、心より感謝申し上げます。
論文情報
<タイトル>BRCA1 and BRCA2 pathogenic variants increase the risk of four less common cancer types
<著者名>
Hajime Sasagawa, Mikiko Endo, Yusuke Iwasaki, Yoshiaki Usui, Yuriko N. Koyanagi, Giovanni Innella, Johanna Hadler, Michael T. Parsons, Kazuyuki Numakura, Yoichiro Kamatani, Yoshinori Murakami, Keitaro Matsuo, Koichi Matsuda, Amanda B. Spurdle, Tomonori Habuchi, Yukihide Momozawa
<雑誌>
ESMO Open
<DOI>
10.1016/j.esmoop.2026.106900
<URL>
https://www.sciencedirect.com/science/article/pii/S2059702926008422?via%3Dihub
補足説明
[1] 病的バリアント遺伝子の塩基配列の違いを指す遺伝的バリアントのうち疾患発症の原因となるものを病的バリアントという。
[2] バイオバンク・ジャパン
日本全国の約27万人から提供を受けた、世界最大級の疾患バイオバンク。オーダーメイド医療の実現プログラムを通じて実施され、ゲノムDNAや血清サンプルを臨床情報と共に収集し、研究者へ提供している。2003年から東京大学医科学研究所内に設置されている。
[3] PARP阻害薬
DNAの相同組換え修復機構が機能していないがん細胞に、特異的に細胞死を誘導する新しい分子標的薬のこと。PARPはPoly (ADP-ribose) polymeraseの略。
[4] ターゲットシークエンス法
全ゲノム領域のうち標的ゲノム領域のみを解析する方法。多くの場合は標的遺伝子を選定して領域を設定するが、ある疾患領域に関連する全ての遺伝子を解析するなど、疾患と関連するイントロン領域や調節領域などの非翻訳領域も組み入れ、標的を拡大して解析する場合もある。
[5] ENIGMAコンソーシアム
主にBRCA1/BRCA2遺伝的バリアントを解析・評価する国際コンソーシアム。ENIGMAはEvidence-based Network for the Interpretation of Germline Mutant Allelesの略。
[6] 累積リスク
属する集団がある年齢までにある病気に罹患(りかん)する確率をいう。本研究では、国立がん研究センターのウェブサイト「がん情報サービス」の2019年における日本の年齢階級別のがん罹患率と年齢階級別の人口割合(https://ganjoho.jp/reg_stat/statistics/data/dl/index.html#a14)と今回の解析結果を基に算出している。
