| 発表のポイント |
|---|
|
概要
東京大学医科学研究所ワクチン科学分野の石井健教授らと、塩野義製薬株式会社の共同研究グループは、スクアレンベースアジュバント(油中水型エマルション: 注1)をモデルとして、免疫原性(immunogenicity:注2)を高める仕組みと副反応が生じる仕組みを解析しました。その結果、インターロイキン1(IL-1)シグナルが、免疫原性と副反応をそれぞれ異なる細胞種・経路を通じて制御していることを明らかにしました。ワクチンは、体内に病原体に対する免疫をつくり出すことで感染症を防ぎます。その効果を高めるために用いられるのがアジュバント(注3)です。アジュバントは免疫原性を高める一方で、注射部位の腫れや痛み、発熱といった副反応(reactogenicity:注4)を伴うことがあります。これまで、免疫原性と副反応は同じ炎症反応に由来する「切り離せないもの」と考えられてきました。
本研究は、ワクチンの効果と安全性を両立させるための新たなワクチン設計指針を示すものです。
本研究成果は2026年3月30日(英国夏時間)付で、Nature Portfolioの国際学術誌「npj Vaccines」に掲載されました。
発表内容
ワクチンに含まれるアジュバントは、抗原に対する免疫応答を増強する一方で、接種部位の腫れや痛み、発熱といった副反応を伴うことがあります。特にスクアレンベースアジュバントは高い免疫原性を示し、実用ワクチンにも広く用いられていますが、免疫原性と副反応が同一の炎症反応に由来するのか、あるいはどこで分岐するのかは十分に理解されていませんでした。本研究では、α-トコフェロール(注5)含有スクアレンベースアジュバント(A-910823、AddaS03(AS03 mimic))をモデルとして、免疫原性と副反応の双方を同一実験系で体系的に解析しました。抗原(SARS-CoV-2スパイクタンパク質)をマウスへ筋肉内投与後、投与部位筋および排液リンパ節(腸骨リンパ節)を回収し、遺伝子発現を包括的に解析したところ、投与後4時間で炎症性サイトカイン・ケモカイン遺伝子(Il1b、Il6、Csf3など)が誘導され、特にリンパ節においてIL-1シグナル関連遺伝子の誘導が顕著でした。この初期応答は、α-トコフェロールを欠く対照製剤(A-910823 w/o α-Toc)では大きく減弱しており、α-トコフェロールが自然免疫応答の誘導に重要であることが示されました。
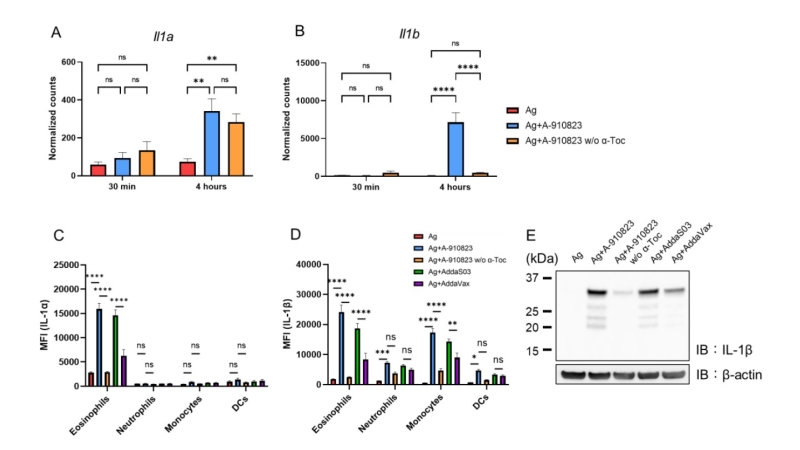
次に、リンパ節内で誘導されるIL-1ファミリー分子を細胞レベルで解析しました。リンパ節組織全体のRNAレベルでは投与後4時間にIl1aおよびIl1bの発現上昇が認められました(図1A-B)。タンパク質レベルの細胞種別解析の結果、IL-1α(注6)は主に好酸球で誘導される一方、IL-1β(注7)は好酸球、単球、樹状細胞(DC:注8)など複数の骨髄系細胞で広く誘導されました(図1C-D)。また、IL-1βはカスパーゼ1による切断を受けた活性型として検出され、これらのIL-1誘導はいずれもα-トコフェロール依存的でした(図1E)。
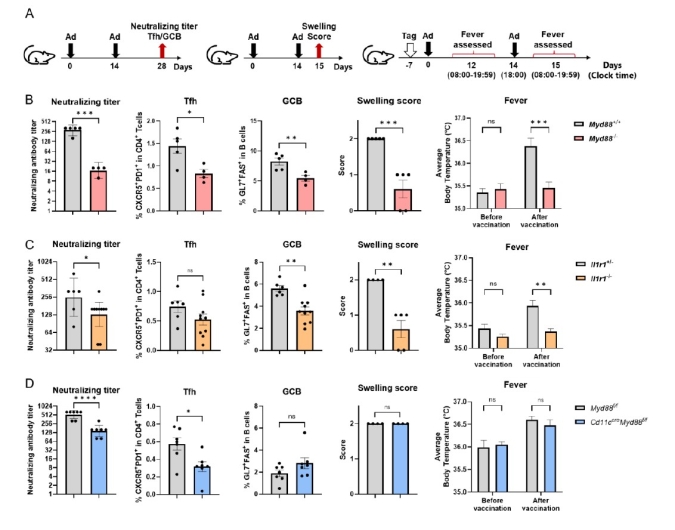
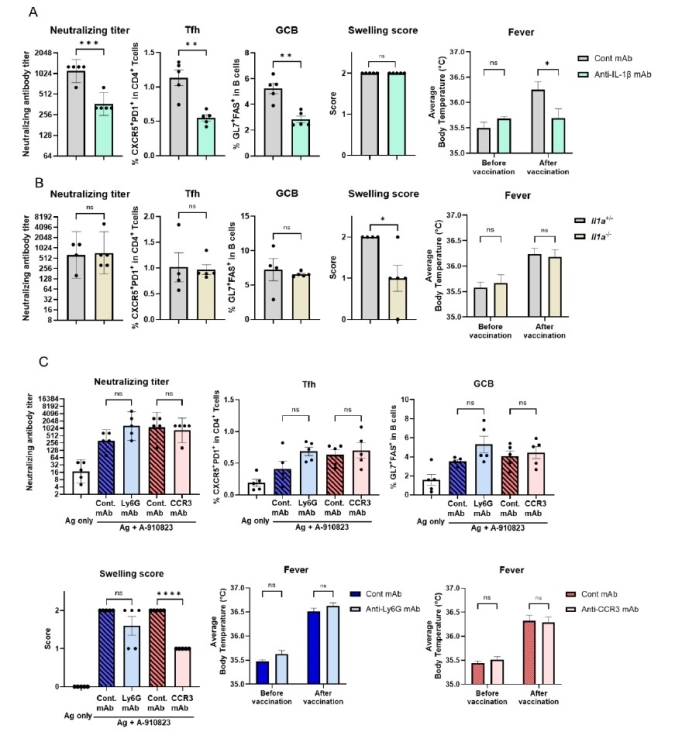
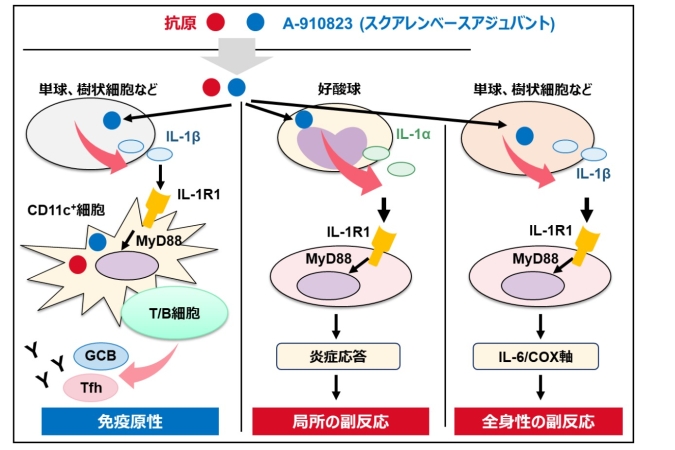
以上より、本研究は、スクアレンベースアジュバントにおいて、免疫原性(主にIL-1β/CD11c+細胞/IL-1R1/MyD88軸)と、副反応(局所:好酸球由来IL-1α軸、全身:IL-1β–IL-6–COX-2軸)が、異なる細胞種・分子経路によって制御されることを実験的に示しました。
なお、本研究は、東京大学医科学研究所における動物実験委員会の審査を受け、東京大学が定めた動物実験実施規則等(承認番号:S19017D)に則り実施されました
発表者・研究者等情報
東京大学
医科学研究所
感染・免疫部門 ワクチン科学分野
石井 健 教授
兼 同大学同研究所 国際ワクチンデザインセンター
兼 同大学国際高等研究所 新世代感染症センター(UTOPIA)
小檜山 康司 准教授(研究当時)
林 智哉 助教
感染・免疫部門 マラリア免疫学分野
Cevayir Coban 教授
塩野義製薬株式会社
吉岡 佑弥
吉岡-西中 杏里
木谷 友次朗
柳田 洋翼
笠原 淳平
辻井 謙一郎
浅岡 由次
黒田 典一
釘宮 啓
大澤 弘明
吉村 彰真
大西 元康
中川 貴之
石田 暁
大本 真也
柳樂 盛男
論文情報
雑誌名: npj Vaccines題 名:IL-1 delineates squalene-based adjuvant efficacy and reactogenicity in a cell-type-specific manner
著者名:Yuya Yoshioka#, Anri Nishinaka-Yoshioka#, Kouji Kobiyama, Tomoya Hayashi, Yujiro Kidani, Yosuke Yanagida, Junpei Kasahara, Kenichiro Tsujii, Yoshiji Asaoka, Norikazu Kuroda, Akira Kugimiya, Hiroaki Osawa, Akimasa Yoshimura, Motoyasu Onishi, Takayuki Nakagawa, Satoru Ishida, Shinya Omoto, Morio Nagira, Cevayir Coban, Ken J. Ishii*
#:共同筆頭著者、*:責任著者
DOI: 10.1038/s41541-026-01420-0
URL:https://doi.org/10.1038/s41541-026-01420-0
研究助成
本研究は、日本医療研究開発機構(AMED)先進的研究開発戦略センター(SCARDA)の支援「ワクチン・新規モダリティ研究開発事業(100日でワクチンを提供可能にする革新的ワクチン評価システムの構築)、(革新的アジュバント・ワクチンキャリアの開発と技術支援ならびにデータベースの構築)」、「ワクチン開発のための世界トップレベル研究開発拠点の形成事業(ワクチン開発のための世界トップレベル研究開発拠点群東京フラッグシップキャンパス(東京大学新世代感染症センター))」を受けるとともに、塩野義製薬株式会社の支援のもとで実施されました。
用語解説
(注1)スクアレンベースアジュバント(油中水型エマルション)スクアレンなどの油成分を、界面活性剤によって微細な油滴として水相中に分散させたエマルション(乳化物)型のアジュバント。
(注2)免疫原性(immunogenicity)
抗体産生やT細胞応答など、抗原特異的な免疫応答を誘導する性質。
(注3)アジュバント
ワクチン抗原に加えて投与し、免疫応答(主に獲得免疫)の誘導を増強する補助成分。
(注4)副反応(reactogenicity)
ワクチン接種後にみられる腫脹、疼痛、発熱など、炎症反応として現れる望ましくない反応の総称。
(注5)α-トコフェロール
ビタミンEの一種。本研究ではスクアレンベース製剤に含まれる成分として解析対象とした。
(注6)IL-1α
炎症反応に関与するサイトカインで、細胞外に放出されると炎症を促進する。
(注7)IL-1β
炎症反応に関与するサイトカインで、細胞内で不活性な前駆体(プロ体)として産生された後、特定の酵素による切断を受けて活性型となり、生理作用を発揮する。
(注8)樹状細胞(DC)
抗原を提示し、T細胞応答の誘導に重要な免疫細胞。
(注9)Tfh細胞
胚中心におけるB細胞の抗体産生・成熟を助けるヘルパーT細胞集団。
(注10)胚中心B細胞(GCB)
リンパ節などの胚中心で増殖し、高親和性抗体の選択・成熟に関与するB細胞。
(注11)IL-1受容体(IL-1R1)
IL-1α/IL-1βを受容し、下流の炎症・免疫活性化シグナルを開始する受容体。
(注12)MyD88
複数の自然免疫受容体やIL-1受容体の下流で働くアダプター分子。
(注13)IL-6
炎症や発熱反応に関与するサイトカイン。
(注14)COX-2
炎症時に誘導され、発熱などに関与するプロスタグランジン産生に関わる酵素。
問合せ先
<研究内容について>東京大学医科学研究所 感染・免疫部門 ワクチン科学分野
石井 健 教授
https://www.ims.u-tokyo.ac.jp/imsut/jp/lab/microbiologyimmunology/section04.html
<機関窓口>
東京大学医科学研究所 プロジェクトコーディネーター室(広報)
https://www.ims.u-tokyo.ac.jp/