| 発表のポイント |
|---|
|
発表概要
東京大学医科学研究所システムウイルス学分野の佐藤佳教授が主宰する研究コンソーシアム「The Genotype to Phenotype Japan (G2P-Japan)」(注1)は、2023年9月20日より接種が開始されたオミクロンXBB.1.5株対応1価ワクチン(注2)によるオミクロン亜株に対する感染中和効果を実験的に検証しました。その結果、接種前と比較して、オミクロンXBB.1.5株対応1価ワクチンによってさまざまなオミクロン亜株に対して効果的な中和抗体(注3)が誘導されることが分かりました。また、SARS-CoV-2の感染歴の有無に関わらずワクチン接種によって中和活性は上昇するが、感染歴の無い人に比べて、オミクロンXBB子孫株に感染歴のある人の方が、中和活性がより高いことも分かりました。本研究成果は2024年1月8日、英国科学雑誌「The Lancet Infectious Diseases」オンライン版で公開されました。
発表内容
新型コロナウイルス(SARS-CoV-2)は、2023年11月現在、全世界において7.7億人以上が感染し、700万人近くを死に至らしめています。これまでにワクチン接種が進み、世界的にも感染者数や死亡者数は減少傾向にあるものの、現在も種々の変異株の出現が相次いでおり、2019年末に突如出現したこのウイルスの収束の兆しは未だ見えていません。2021年末に南アフリカで出現した新型コロナウイルス「オミクロン株(B.1.1.529系統およびBA系統)」は、同年11月26日に命名されて以降、またたく間に全世界に伝播しました。しかし、2022年1月から世界各国で、オミクロン亜株の1つであるオミクロンBA.2株が検出され、日本を含めた世界の多数の国々に拡がり、オミクロンBA.2株が主流行株となりました。その後、オミクロンBA.2株は急速に多様化し、オミクロンXBB株を含む複数のオミクロン亜株が相次ぎ出現してきました。そして現在、オミクロンXBB子孫株であるオミクロンXBB.1.5株、XBB.1.16株、XBB.2.3株、EG.5.1株(別名:XBB.1.9.2.5.1)、HK.3株(オミクロンEG.5.1株の子孫株)が世界中で流行しています。加えて、2023年7月にはオミクロンXBB系統とは大きく異なるオミクロンBA.2.86株が新たに出現し、その割合は増加傾向にあります。世界保健機関(WHO)はオミクロンXBB.1.5株、XBB.1.16株、EG.5.1株およびBA.2.86株を注目すべき変異株(variants of interest, VOI)(注4)に、オミクロンXBB.1.9株、XBB.2.3株を監視下の変異株(variants under monitoring, VUM)(注5)にそれぞれ指定しています。
オミクロン亜株の多くは、中和抗体の効果が減弱することが懸念されています。これらの変異株に対しても有効な免疫を備えるために、2023年9月20日からオミクロンXBB.1.5株対応1価mRNAワクチンが接種可能となりました。
本研究ではオミクロンXBB.1.5株対応1価ワクチン接種によって誘導される中和抗体のオミクロン亜株に対する中和効果を明らかにするため、①ワクチン接種前にSARS-CoV-2の感染歴がない人(感染歴がない群)(図1)、②ワクチン接種前にオミクロンXBB子孫株の感染歴がある人(オミクロンXBB子孫株に感染歴のある群)(図2)の二つの群を対象に、オミクロンXBB.1.5株対応1価ワクチン接種前(Pre)と接種3-4週間後(Post)に採血したヒト血清を用いて、解析を行いました。
その結果、感染歴が無い群(図1)およびオミクロンXBB子孫株に感染歴のある群(図2)いずれにおいても、オミクロンXBB.1.5株対応1価ワクチン接種によって、オミクロン亜株に対する中和活性が上昇することがわかりました。また、中和活性の上昇倍率は、感染歴が無い群で2.1-3.9倍(図1)、オミクロンXBB子孫株に感染歴のある群で1.8-3.6倍(図2)であり、二つの群の間で大きな差はありませんでした。この結果は、オミクロンXBB.1.5株対応1価ワクチン接種の接種により、感染歴の有無によらずオミクロン亜株に対する液性免疫(注6)が誘導されることを示しています。
現在、研究コンソーシアム「The Genotype to Phenotype Japan (G2P-Japan)」では、出現が続くさまざまな変異株について、ウイルス学的特性の解析や、中和抗体や治療薬への感受性の評価、病原性についての研究に取り組んでいます。G2P-Japanコンソーシアムでは、今後も、新型コロナウイルスの変異(genotype)の早期捕捉と、その変異がヒトの免疫やウイルスの病原性・複製に与える影響(phenotype)を明らかにするための研究を推進します。

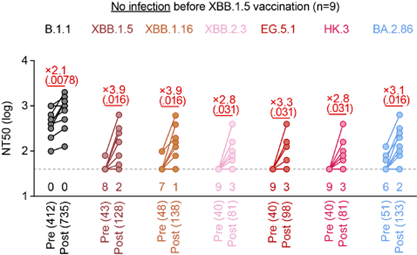
図1. 感染歴が無い群におけるオミクロンXBB.1.5株対応1価ワクチンの中和抗体誘導効果
感染歴が無い群における、オミクロンXBB.1.5株対応1価ワクチンの接種によって誘導される中和抗体の感染中和活性を評価した。ウイルスには6種類のオミクロン亜株および従来株(B.1.1株)を使用した。縦軸はウイルス感染を50%阻害する中和抗体の感染中和活性(NT50)を示し、値が大きいほど中和活性が高いことを指す。括弧内の数字は各ウイルスに対するNT50の幾何平均をそれぞれ示している。点線下の数字は各ウイルスについてNT50が検出限界以下だった血清数を指している。Preはワクチン接種前、Postはワクチン接種3-4週間後にそれぞれ採血した血清を示す。各ウイルスのワクチン接種前に対するワクチン接種3-4週間後の中和活性の上昇倍率は、括弧内の統計検定結果のP値と共に赤字で示している。

図2. オミクロンXBB子孫株に感染歴のある群におけるオミクロンXBB.1.5株対応1価ワクチンの中和抗体誘導効果
オミクロンXBB子孫株に感染歴のある群における、オミクロンXBB.1.5株対応1価ワクチンの接種によって誘導される中和抗体の感染中和活性を評価した。ウイルスには6種類のオミクロン亜株および従来株(B.1.1株)を使用した。縦軸はウイルス感染を50%阻害する中和抗体の感染中和活性(NT50)を示し、値が大きいほど中和活性が高いことを指す。括弧内の数字は各ウイルスに対するNT50の幾何平均をそれぞれ示している。点線下の数字は感染歴が無い群と比較した、オミクロンXBB子孫株に感染歴のある群におけるワクチン接種前の各ウイルスに対するNT50の比を示している。Preはワクチン接種前、Postはワクチン接種3-4週間後にそれぞれ採血した血清を指す。各ウイルスのワクチン接種前に対するワクチン接種3-4週間後の中和活性の上昇倍率は、括弧内の統計検定結果のP値と共に赤字で示している。
発表者
東京大学医科学研究所 システムウイルス学分野佐藤 佳(教授、一般社団法人G2P-Japan 代表理事)
小杉 優介(日本学術振興会特別研究員、大学院生)
郭 悠(特任助教)
Alfredo Hinay, Jr(特任研究員)
郭 子毅 (特任研究員)
瓜生 慧也(日本学術振興会特別研究員、大学院生)
研究コンソーシアム「The Genotype to Phenotype Japan (G2P-Japan)」
論文情報
〈雑誌〉The Lancet Infectious Diseases〈題名〉Antiviral humoral immunity against SARS-CoV-2 Omicron subvariants induced by XBB.1.5 monovalent vaccine in infection-naïve and XBB-infected individuals
〈著者〉小杉 優介, 郭 悠, Alfredo Hinay, Jr, 郭 子毅, 瓜生 慧也, 木原 実, 斎藤 史武, 上箕 義典, 倉持 仁, 白川 康太郎, 高折 晃史, The Genotype to Phenotype Japan (G2P-Japan) Consortium,佐藤 佳*.
(*Corresponding author)
〈DOI〉10.1016/S1473-3099(23)00784-3
〈URL〉https://www.thelancet.com/journals/laninf/article/PIIS1473-3099(23)00784-3/fulltext
研究助成
本研究は、佐藤 佳教授に対する日本医療研究開発機構(AMED)「新興・再興感染症に対する革新的医薬品等開発推進研究事業(JP22fk0108146, JP21fk0108494, JP21fk0108425, JP21fk0108432)」、AMED 先進的研究開発戦略センター(SCARDA)「ワクチン開発のための世界トップレベル研究開発拠点の形成事業(UTOPIA, JP223fa627001)、AMED SCARDA「ワクチン・新規モダリティ研究開発事業(JP223fa727002)」、科学技術振興機構(JST) CREST(JPMJCR20H4)、佐藤 佳教授およびG2P-Japanに対する日本学術振興会(JSPS) KAKENHI Fund for the Promotion of Joint International Research (International Leading Research)(JP23K20041)、伊東 潤平助教に対するJSTさきがけ(JPMJPR22R1)などの支援の下で実施されました。
用語解説
(注1)研究コンソーシアム「The Genotype to Phenotype Japan (G2P-Japan)」東京大学医科学研究所 システムウイルス学分野の佐藤佳教授が主宰する研究チーム。日本国内の複数の若手研究者・研究室が参画し、研究の加速化のために共同で研究を推進している。現在では、イギリスを中心とした諸外国の研究チーム・コンソーシアムとの国際連携も進めている。
(注2)オミクロンXBB.1.5株対応1価ワクチン
オミクロンXBB.1.5株のスパイクタンパク質の設計図となるメッセンジャーRNA(mRNA)を有効成分とする1価ワクチン。
(注3)中和抗体
獲得免疫応答のひとつ。B細胞によって産生される抗体でSARS-CoV-2のスパイクタンパク質を中和する作用がある。
(注4)注目すべき変異株(VOI:variants of interest)
新型コロナウイルスの流行拡大によって出現した、顕著な変異を有する変異株のことであり、今後感染者の増加が懸念される変異株。
(注5)監視下の変異株(variants under monitoring, VUM)
新型コロナウイルスの変異株のうち、世界保健機関(WHO)が指定する今後流行拡大の可能性が懸念される変異株。
(注6)液性免疫
獲得免疫応答のうち、B細胞から産生される抗体が主体となるもの。抗体は細胞外の異物に結合し、中和やマクロファージによる貪食の誘導などにより異物を排除する。
問合せ先
東京大学医科学研究所 感染・免疫部門 システムウイルス学分野
教授 佐藤 佳(さとう けい)
https://www.ims.u-tokyo.ac.jp/imsut/jp/lab/ggclink/section04.html
〈報道に関する問合せ〉
東京大学医科学研究所 プロジェクトコーディネーター室(広報)
https://www.ims.u-tokyo.ac.jp/