| 発表のポイント |
|---|
|
発表内容
東京大学国際高等研究所 新世代感染症センター 河岡義裕 機構長らの研究グループは、新型コロナウイルス変異株・オミクロン株XBB.1.5系統の飛沫伝播のしやすさ、および同変異株に対する再感染のリスクについて、ハムスターモデルを用いて調べました。新型コロナウイルス変異株・オミクロン株の流行は、現在も続いています。2023年6月現在、日本を含む多くの国々で、BA.2系統から派生したXBB.1.5系統(注)が流行の主流となっています。しかし、XBB.1.5系統が飛沫伝播しやすくなっているのか、また、初期のオミクロン株に感染した場合のXBB.1.5系統に対する再感染のリスクについては明らかになっていませんでした。
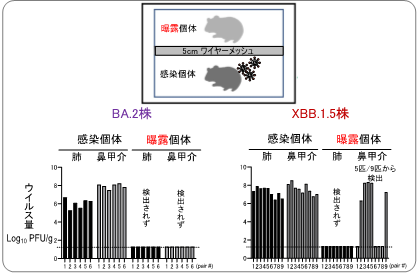
臨床検体から分離されたXBB.1.5系統の株(XBB.1.5株)に感染した個体と非感染個体の間で飛沫を介した感染伝播が起こるかどうかについて調べました。XBB.1.5株を感染させ(感染個体)、感染個体のケージから、直接接触が起こらない飼育環境下(飼育ケージ内を二重の金網の柵で仕切り、お互いに5 cm以上近づくことができないようにした)で、感染歴のないハムスター(曝露個体)を72時間飼育しました。XBB.1.5株に感染したハムスターでは感染後の肺や鼻でウイルスが効率よく増殖し、さらに曝露個体9匹中5匹からウイルスが検出されました。オミクロン株BA.2系統の株(BA.2株)を感染させた場合は、感染個体ではXBB.1.5株と同様に感染後の肺や鼻でウイルスが効率よく増殖しましたが、どの曝露個体からもウイルスは検出されませんでした。これらの結果から、少なくともハムスターにおいて、BA.2系統よりもXBB.1.5系統の飛沫伝播効率が良いことが明らかとなりました。
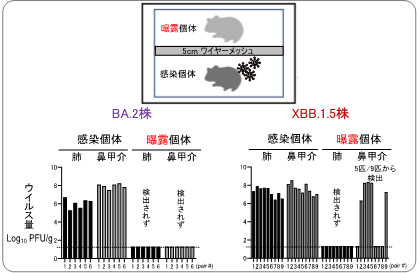
ハムスターに、BA.2株あるいはXBB.1.5株を播種した(感染個体)。一日後に、非感染個体(曝露個体)を入れたケージを5 cm距離を離して隣接させ、飛沫による感染伝播が起こるか調べた(左図)。BA.2株では、曝露3日後には伝播が見られなかったが、XBB.1.5株では、曝露3日後に9ペア中5ペアで伝播していた(右図)。
続いて、初期のオミクロン株の感染によって誘導された免疫応答がXBB.1.5株に対して有効であるかどうかを検証しました。オミクロン株BA.1系統の株(BA.1株)による初感染から10ヶ月間経過したハムスターにBA.1株またはXBB.1.5株を再感染させました。その結果、BA.1株に再感染したハムスターの鼻から検出されるウイルス量は、感染歴を持たないハムスターと比べて大幅に低く、再感染個体の肺からはウイルスは全く検出されませんでした。一方、XBB.1.5株に再感染したハムスターの肺から検出されるウイルス量は、感染歴を持たないハムスターと比べて大幅に低いものの、すべての個体の肺からウイルスが検出されました。また、XBB.1.5株に再感染したハムスターの鼻から検出されるウイルス量は感染歴を持たないハムスターと比べてやや少なくなる程度でした。

(A)BA.1株の初感染から10ヶ月間経過したハムスターの鼻腔内にBA.1株またはXBB.1.5株を再び接種した。(B)BA.1株またはXBB.1.5株を初めて感染させたハムスターの鼻甲介および肺からは大量のウイルスが検出された。一方、再感染させたハムスターでは、再感染後3日目の鼻甲介においてBA.1株接種群では3匹中2匹からウイルスが検出されたものの、肺からはどの個体からもウイルスが検出されなかった。また、XBB.1.5株接種群では肺、鼻におけるウイルス量は初感染のハムスターと比べると減っているが、全個体からウイルスが検出された。
本研究は6月21日、 英国医学誌「eBioMedicine」(オンライン版)に公表されました。
なお、ヒトで世界的に流行したBA.2系統がハムスターでは飛沫伝播を起こさないため、「ハムスターにおいてXBB.1.5系統の方が伝播しやすい」という今回の結果が必ずしもヒトに当てはまるわけではありません。今後もオミクロン系統の飛沫伝播に関する継続的な検証が待たれます。
発表者
東京大学国際高等研究所 新世代感染症センター 機構長東京大学医科学研究所 ウイルス感染部門 特任教授
河岡 義裕
<国立国際医療研究センター 研究所 国際ウイルス感染症研究センター長>
論文情報
〈雑誌〉eBioMedicine(6月21日オンライン版)〈題名〉Transmission and re-infection of Omicron variant XBB.1.5 in hamsters
〈著者〉Peter J. Halfmann*, Ryuta Uraki*, Makoto Kuroda, Kiyoko Iwatsuki-Horimoto, Seiya Yamayoshi, Mutsumi Ito, Yoshihiro Kawaoka¶
*:筆頭著者 ¶:責任著者
〈DOI〉10.1016/j.ebiom.2023.104677
〈URL〉https://www.thelancet.com/journals/ebiom/article/PIIS2352-3964(23)00242-6/fulltext
研究助成
本研究は、東京大学国際高等研究所 新世代感染症センター、東京大学医科学研究所、国立国際医療研究センター、米国ウィスコンシン大学が共同で実施し、日本医療研究開発機構(AMED)新興・再興感染症に対する革新的医薬品等開発推進研究事業(動物モデルと患者検体を用いた新型コロナウイルス感染症(COVID-19)の病態メカニズムの解明II、 愛玩動物由来人獣共通感染症の対策を目指した総合研究)、創薬支援推進事業(新型コロナウイルス感染症(COVID-19)に対する弱毒生ワクチンの開発 II)、新興・再興感染症研究基盤創生事業 (中国拠点を基軸とした新興・再興および輸入感染症制御に向けた基盤研究)ならびに、ワクチン開発のための世界トップレベル研究開発拠点の形成事業 (ワクチン開発のための世界トップレベル研究開発拠点群 東京フラッグシップキャンパス(東京大学新世代感染症センター))の一環として行われました。用語解説
(注)オミクロン株XBB.1.5系統ウイルス感染は、コロナウイルス粒子表面に存在するスパイク蛋白質を介してウイルス粒子が宿主細胞表面の受容体蛋白質に結合することで始まる。実用化されたあるいは開発中のCOVID-19に対する抗体薬は、このスパイク蛋白質を標的としており、その機能を失わせる(中和する)ことを目的としている。BA.2系統は、そのスパイク蛋白質に少なくとも31ヶ所の変異を有する。XBB.1.5系統のスパイク蛋白質は、BA.2系統と共通する30ヶ所の変異に加えて、14ヶ所の変異を有する。
問合せ先
〈研究に関する問合せ〉東京大学国際高等研究所 新世代感染症センター 機構長
東京大学医科学研究所 ウイルス感染部門 特任教授
河岡 義裕(かわおか よしひろ)
https://www.ims.u-tokyo.ac.jp/imsut/jp/lab/dstngprof/page_00174.html
〈報道に関する問合せ〉
東京大学医科学研究所 プロジェクトコーディネーター室(広報)
https://www.ims.u-tokyo.ac.jp/imsut/jp/
国立国際医療研究センター 企画戦略局 広報企画室
https://www.ncgm.go.jp/