| 発表の概要 |
|---|
造血幹細胞は、赤血球・白血球・血小板といったさまざまな血液細胞へ分化する能力を持っており、難治性血液疾患に対して行われる造血幹細胞移植では、移植後の造血および免疫の再構築において重要な役割を担います。しかし、造血幹細胞は非常に数が少なく、特に臍帯血移植においては、移植のリスクが増したり、ドナー選択が制限される可能性があることから、生体外増幅技術の確立が求められています。 これまで、生体外での造血幹細胞の維持には、血清アルブミンとサイトカインを組み合わせた培地が不可欠とされてきましたが、実際には、短期間の造血幹細胞維持はできるものの、その増幅作用は限定的でした。 2019年に日米英独共同研究グループは、ポリビニルアルコール培地にサイトカインを加えると、血清アルブミンを用いずに、長期に安定してマウス造血幹細胞を増幅できることを報告しています。これに基づき、今回、アルブミンとサイトカインを、それぞれ高分子ポリマーと特定の化合物に置き換えた培地を用いて、ヒト造血幹細胞の生体外での長期増幅を可能とする新規の培養技術を開発しました。これにより、臍帯血に含まれるヒト造血幹細胞を1か月間にわたって増幅することができます。さらに、単一細胞RNAシークエンス解析により、既存の培養技術と比較しても、造血幹細胞が選択的に増幅されることが示唆されました。 今後、この培養技術をヒト造血幹細胞の基礎研究ツールとして提供するとともに、より安全な造血幹細胞移植の実現とドナー不足の解消に向けた臨床応用を目指します。 |
研究代表者
筑波大学医学医療系/東京大学医科学研究所 幹細胞生物学分野山﨑 聡 教授/特任准教授
慶應義塾大学医学部 内科学教室(血液)
櫻井 政寿 専任講師
研究の背景
造血幹細胞は、骨髄中に存在し、赤血球・白血球・血小板といったさまざまな血液細胞へ分化する能力を持つ細胞です。血液疾患の治療に広く用いられており、化学療法だけでは治らない白血病や悪性リンパ腫などの難治性血液がん、あるいは再生不良性貧血などの造血不全をきたす疾患に対して、健常人ドナーから採取した造血幹細胞を移植する造血幹細胞移植が広く行われています。しかしながら、この造血幹細胞は非常に稀な細胞であり、特に国内で広く用いられている臍帯血移植では、含まれる造血幹細胞の数が少ないために、生着注1が遅れて感染症のリスクが増したり、ドナー選択が制限される可能性が示唆されています。そのため、より安全な造血幹細胞移植の実現には、とりわけ臍帯血に含まれる造血幹細胞の生体外増幅を行うことが重要です。また近年は、鎌状赤血球貧血や先天性免疫不全症などの遺伝性血液疾患に対して、患者自身の造血幹細胞を採取・培養し、異常な遺伝子を修復した後に再び体内に戻して正常な造血を回復させる遺伝子治療法の開発も進められています。
このようなヒト造血幹細胞の増幅においては、これまで、血清アルブミン注2とサイトカイン注3を組み合わせた培地が、生体外での維持には不可欠であると考えられてきました。しかし実際には、造血幹細胞の短期間の維持は可能ですが、その増幅作用は限定的でした。
日米英独共同の本研究グループ注4は、マウス造血幹細胞について、ポリビニルアルコール(PVA)注5にstem cell factor(SCF)とトロンボポエチン(TPO)の2種類のサイトカインを加えることによって、血清アルブミンを用いずに、長期に安定して増幅できる培養技術を報告しています。そこで今回、これに基づき、血清アルブミンやサイトカインを用いることなく、化合物で構成された培地を用いて、長期に安定したヒト造血幹細胞の増幅技術の開発を目指しました。
研究内容と成果
PVAにSCFとTPOを加えた培地条件では、マウスと異なり、ヒト造血前駆細胞の増幅は限定的でした。そこで、マウスとヒトの造血前駆細胞の違いを調べるために、培養中の主要なシグナル伝達経路のリン酸化状態を分析したところ、ヒトではホスファチジルイノシトール3-キナーゼ(PI3K)/AKTの有意な減少が観察されました(図1)。そこで、PI3K-AKTシグナルを活性化させるため、740Y-P(PI3Kを活性化させる化合物)を加えたところ、7日目時点ではヒト造血前駆細胞の増幅率が改善しました。さらに、740Y-Pを加えるとSCFが不要であること、またTPO受容体作動薬注6であるブチザミドを用いるとTPOも不要になることを見出しました。これらの結果から、PVAに740Y-Pとブチザミドを加えた培地(2a培地)では、サイトカインを用いずともヒト造血前駆細胞を7日間培養可能であることを確認しました。しかし、この方法では、14日間経過すると巨核球(血小板をつくる細胞)に分化してしまうことも分かりました。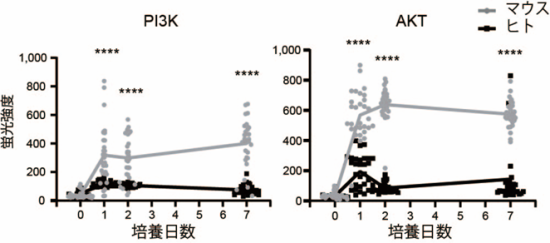
図1 マウスおよびヒトの造血前駆細胞におけるPI3K/AKTリン酸化
SCFとTPOを含むPVA培地で培養した場合、ヒト造血前駆細胞におけるPI3KとAKTのリン酸化状態はマウス造血前駆細胞と比較し、有意に低かった。****P < 0.0001.
長期に安定化した培養を実現するため、造血幹細胞の分化を防ぐ化合物を探索し、ピリミドインドール誘導体UM171を2a培地に加えた3a培地注7では、30日間安定してヒト造血前駆細胞が培養可能になることを見いだしました。この培地で培養後の細胞を放射線照射した免疫不全マウスに移植することによって、造血を再構築する能力の維持を確認しました。
また、増殖効率のさらなる向上を目指し、PVAよりも優れたポリマーの探索を行いました。スクリーニングの結果、ポリビニルカプロラクタム-ポリ酢酸ビニル-ポリエチレングリコールグラフトコポリマー(PCL-PVAc-PEG)注8が著しい細胞増殖能を有することを発見しました(図2)。PVAの代わりにPCL-PVAc-PEGを基盤とし、740Y-P、ブチザミド、UM171注9を添加した培地を用いると、ヒト造血前駆細胞の増殖能がさらに改善しました(図3)。この培地中で培養した細胞も、同様に、造血を再構築する能力を維持していました。
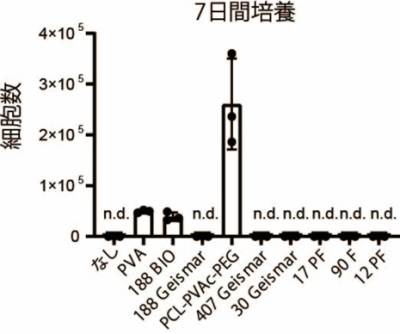
図2 3a培地における合成ポリマーのスクリーニング
ヒト臍帯血由来造血前駆細胞をさまざまな合成ポリマーを含む3a培地で7日間培養した後に生じた全細胞数の比較。PCL-PVAc-PEGは著しく高い細胞増殖能を有する。
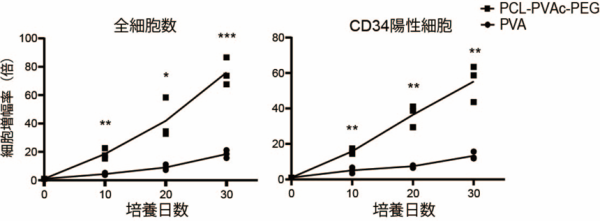
図3 PVAまたはPCL-PVAc-PEGを含む3a培地で30日間培養した際の全細胞数とCD34陽性細胞数(CD34は造血前駆細胞のマーカー)
PCL-PVAc-PEGを基盤とした3a培地では、PVAを含む培地に比べ、30日間の培養で全細胞が約75倍、CD34陽性細胞が約55倍に増加し、より長期的な細胞増殖の促進が確認された。*P < 0.05; **P < 0.01; ***P < 0.001.
次に、PCL-PVAc-PEGを基盤とした3a培地で培養した細胞の特性を調べるために、単一細胞RNAシークエンス解析注10を行ったところ、造血幹細胞に特異的な遺伝子を発現した細胞が多くを占めており、これは近年すでに臨床試験が実施された、UM171あるいはSR-1注9を用いたヒト造血幹細胞の培養技術と比較しても高い傾向にあることが分かりました(図4)。以上より、PCL-PVAc-PEGを基盤とした3a培地は、造血幹細胞を選択的に増幅することが示唆されました。
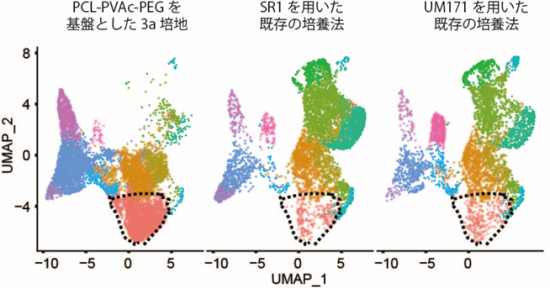
図4 各培養法で10日間培養した細胞における単一細胞RNAシークエンス
PCL-PVAc-PEGを基盤とした3a培地では、造血幹細胞に特異的な遺伝子を発現する細胞(黒点線で囲まれた部分)が既存の培養法よりも、多く含まれていた。
今後の展開
本研究チームは、今回得られた知見をもとに、ヒト造血幹細胞の培養技術のさらなる改良を続けます。これらの培養技術を、ヒト造血幹細胞の基礎研究ツールとして提供するとともに、より安全な造血幹細胞移植の実現とドナー不足の解消に向けて、臨床応用に取り組んでいく予定です。
用語解説
研究資金
掲載論文
問合わせ先
【取材・報道に関すること】
