| 発表のポイント |
|---|
|
発表内容
- 2021年末から始まった新型コロナウイルス変異株・オミクロン株の流行は、現在も続いています。2022年6月現在、オミクロン株は、少なくとも5つの系統 (BA.1、BA.2、BA.3、BA.4、BA.5)に分類されます。2022年1月から3月にかけて国内で流行したオミクロン株の主流はBA.1系統でしたが、その後BA.2系統への置き換わりが進み、現在は、BA.2系統が流行の主流になっています。東京大学医科学研究所ウイルス感染部門の河岡義裕特任教授らの研究グループは、COVID-19動物モデルのハムスターを用いて、BA.1株に対する抗ウイルス薬の効果および耐性ウイルスが出現するリスクについて検証しました。また、BA.1株とBA.1.1株に対する抗体薬の効果を検証しました。
本研究グループは、BA.1株を感染させたハムスターを用いて、抗ウイルス薬2種類 (モルヌピラビル、臨床試験中のS-217622)の効果を検証しました。どちらの薬剤も、肺におけるウイルス増殖を大幅に抑制しました。また、鼻での増殖もやや抑制することがわかりました (図1)。
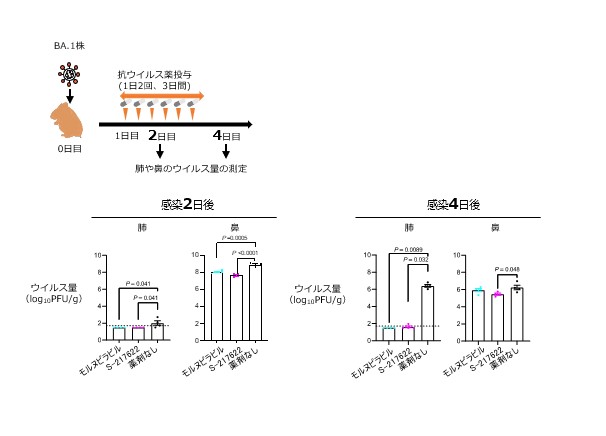
図1:野生型ハムスターにおける抗ウイルス薬の効果の検証
オミクロン/BA.1株をハムスターの鼻腔内に接種し、接種1日後から 抗ウイルス薬(3日間) を投与した。ウイルス接種2日後および4日後の肺と鼻におけるウイルス量を測定した。モルヌピラビル、臨床試験中のS-217622は、いずれも肺におけるウイルス増殖を有意に抑えた。また、鼻での増殖もやや抑制した。
- ウイルス排除に必要な免疫が十分に誘導されない免疫抑制状態のCOVID-19患者に抗ウイルス剤を使用すると、その体内で耐性ウイルスが発生する可能性があります。そこで、耐性ウイルスが出現するリスクについて検証するために、免疫抑制剤のシクロホスファミドをハムスターに投与し、ウイルスが長期間排除されない動物モデルを作出しました。
- BA.1株を感染させた野生型ハムスターでは、感染7日後の肺でウイルスがほとんど検出されなかったのに対して、免疫抑制剤投与ハムスターでは、感染7日後の肺で多くのウイルスが検出されました (図2)。この免疫抑制状態のハムスターにBA.1株を感染させた後、モルヌピラビルまたはS-217622を5日間投与しました。投薬終了後2日目 (感染7日後)の時点では、モルヌピラビルとS-217622投与群いずれにおいても、コントロール群と比べて、肺でのウイルス量は有意に少ないことがわかりました。
しかし、投薬終了後9日目 (感染14日後)の時点では、コントロール群と同程度でした (図2)。これらの結果は、免疫抑制状態の患者にモルヌピラビルまたはS-217622を投与しても、5日間程度の短い投与期間では、体内からウイルスを完全に排除できない可能性があることを示唆しています。 -
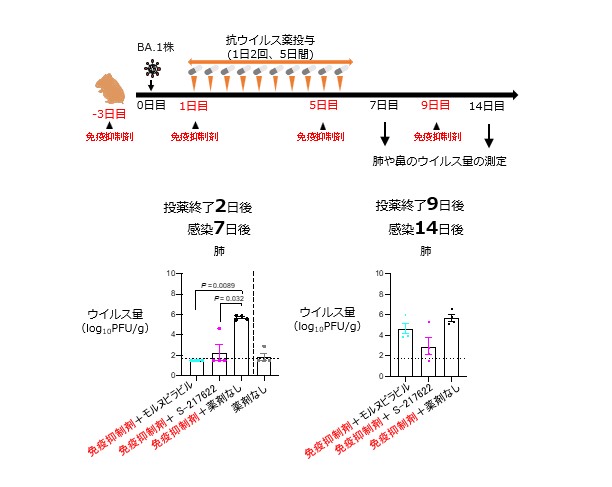
図2:免疫抑制状態のハムスターにおける抗ウイルス薬の効果の検証
免疫抑制剤 (シクロホスファミド)を投与して、免疫抑制状態のハムスターを作出した。このハムスターにBA.1株を接種し、接種1日後から 抗ウイルス薬(5日間) を投与した。
投薬終了後2日目 (感染後 7日目)および投薬終了後9日目 (感染後 14日目)の肺と鼻におけるウイルス量を測定した。投薬終了後 2日目 (感染後 7日目)では、両薬剤で肺におけるウイルスの増殖抑制効果が見られたが、投薬終了後 9日目 (感染後 14日目)では、その抑制効果は見られなかった。 - 一方で、投薬終了後9日目 (感染14日後)にハムスターの肺から分離したウイルスは、モルヌピラビルまたはS-217622に対して高い感受性を示しました。このことは、これらの薬剤を投与した免疫抑制状態の患者体内において、耐性ウイルスが出現し、それが優勢になるリスクは低いことを示唆しています。
- スパイク蛋白質を標的としないモルヌピラビルとS-217622は、オミクロン株のようなスパイク蛋白質に多数の変異を持つウイルスに対して有効であることが示されました。今後、新たな変異株が出現しても、これらの薬剤は、その新規変異株感染患者の重症化防止に大きく寄与すると考えられます。
- また、抗体薬 (カシリビマブ・イムデビマブ、チキサゲビマブ・シルガビマブ、あるいはソトロビマブ)の効果についても検証を行いました。抗体薬は新型コロナウイルス のスパイク蛋白質を標的にしています。抗体薬のチキサゲビマブ・シルガビマブは、BA.1株を感染させた野生型ハムスターの肺でのウイルス増殖を抑制したものの、BA.1.1株に対しては、その効果は見られませんでした (図3)。BA.1.1株のもつR346K (注4)の変異がチキサゲビマブ・シルガビマブの効果に影響したと考えられます。
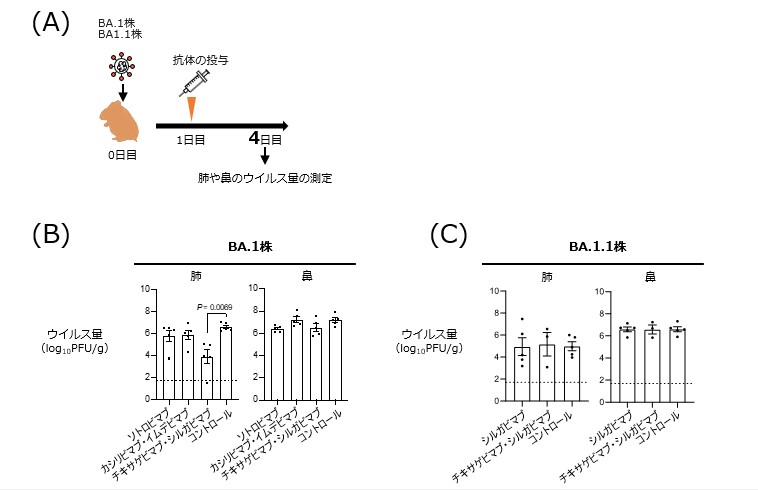
図3:野生型ハムスターにおける抗体薬の効果の検証
(A) 実験のスケジュール:BA.1株または、BA.1.1株をハムスターの鼻腔内に接種し、接種1日後に抗体薬を投与し、ウイルス接種4日後の肺と鼻におけるウイルス量を測定した。
(B) チキサゲビマブ・シルガビマブのみが、BA.1株の肺におけるウイルス増殖を抑えた。一方で、鼻での増殖を抑えなかった。
(C) シルガビマブ単剤、チキサゲビマブ・シルガビマブは、BA.1.1株の肺・鼻におけるウイルス増殖を抑えなかった。
- 本研究を通して得られた成果は、医療現場における適切なCOVID-19治療薬の選択に役立つだけでなく、オミクロン株のリスク評価など行政機関が今後の新型コロナウイルス感染症対策計画を策定、実施する上で、重要な情報となります。本研究成果は、2022年6月15日 (英国夏時間:15日午前10時)、英国科学雑誌「Nature Microbiology」オンライン速報版で公開されました。
- なお、本研究は、東京大学、国立感染症研究所、国立国際医療研究センター、米国ウィスコンシン大学が共同で行ったものです。また、本研究は、日本医療研究開発機構(AMED)新興・再興感染症に対する革新的医薬品等開発推進研究事業並びに厚生労働科学研究費補助金新興・再興感染症及び予防接種政策推進研究事業の一環として行われました。
-
発表雑誌
雑誌名: 「Nature Microbiology 」 6月15日オンライン版
論文タイトル: Therapeutic efficacy of monoclonal antibodies and antivirals against SARS-CoV-2 Omicron BA.1 in Syrian hamsters
著者: Ryuta Uraki*, Maki Kiso*, Masaki Imai*, Seiya Yamayoshi, Mutsumi Ito, Seiichiro Fujisaki, Emi Takashita, Michiko Ujie, Yuri Furusawa, Atsuhiro Yasuhara, Kiyoko Iwatsuki-Horimoto, Yuko Sakai-Tagawa, Shinji Watanabe, Hideki Hasegawa, and Yoshihiro Kawaoka¶
*:筆頭著者
¶:責任著者
DOI:10.1038/s41564-022-01170-4
URL:https://www.nature.com/articles/s41564-022-01170-4
論文タイトル: Therapeutic efficacy of monoclonal antibodies and antivirals against SARS-CoV-2 Omicron BA.1 in Syrian hamsters
著者: Ryuta Uraki*, Maki Kiso*, Masaki Imai*, Seiya Yamayoshi, Mutsumi Ito, Seiichiro Fujisaki, Emi Takashita, Michiko Ujie, Yuri Furusawa, Atsuhiro Yasuhara, Kiyoko Iwatsuki-Horimoto, Yuko Sakai-Tagawa, Shinji Watanabe, Hideki Hasegawa, and Yoshihiro Kawaoka¶
*:筆頭著者
¶:責任著者
DOI:10.1038/s41564-022-01170-4
URL:https://www.nature.com/articles/s41564-022-01170-4
問い合わせ先
<研究に関するお問い合わせ>
東京大学医科学研究所 ウイルス感染部門
特任教授 河岡 義裕 (かわおか よしひろ)
https://www.ims.u-tokyo.ac.jp/imsut/jp/lab/dstngprof/page_00174.html
<報道に関するお問い合わせ>
東京大学医科学研究所 国際学術連携室(広報)
https://www.ims.u-tokyo.ac.jp/imsut/jp/
国立国際医療研究センター 企画戦略局 広報企画室
https://www.ncgm.go.jp/
東京大学医科学研究所 ウイルス感染部門
特任教授 河岡 義裕 (かわおか よしひろ)
https://www.ims.u-tokyo.ac.jp/imsut/jp/lab/dstngprof/page_00174.html
<報道に関するお問い合わせ>
東京大学医科学研究所 国際学術連携室(広報)
https://www.ims.u-tokyo.ac.jp/imsut/jp/
国立国際医療研究センター 企画戦略局 広報企画室
https://www.ncgm.go.jp/
用語解説
(注1) 抗ウイルス薬:
レムデシビル (販売名:ベクルリー点滴静注液)は令和2年5月7日に特例承認を受けた。モ ルヌピラビル (販売名:ラゲブリオ)は令和3年12月24日に特例承認を受けた。ニルマトレ ルビル・リトナビル (販売名:パキロビッドパック)は令和4年2月10日に特例承認を受けた。S-217622は臨床試験中。https://www.mhlw.go.jp/content/10900000/000938454.pdfを参照。
(注2) オミクロン/BA.1変異株:
新型コロナウイルスは、ウイルス粒子表面に存在するスパイク蛋白質を使って、宿主細胞表面のウイルス受容体に結合することで、標的細胞への感染を開始する。BA.1変異株は、従来株と比較して、そのスパイク蛋白質に30カ所以上のアミノ酸変異を有している。これらのスパイク蛋白質におけるアミノ酸変異は、抗体薬の効果を減弱させる可能性がある。
(注3) 抗体薬:
カシリビマブ・イムデビマブ (販売名:ロナプリーブ注射液セット)は令和 3 年 7 月 19 日に特例承認を受けた。ソトロビマブ (販売名:ゼビュディ点滴静注液)は令和 3 年 9 月 27 日に特例 承認を受けた。チキサゲビマブ・シルガビマブ (開発コード:AZD7442)は臨床試験中。 https://www.mhlw.go.jp/content/10900000/000938454.pdfを参照。
(注4) オミクロン/BA.1.1変異株
BA.1の亜系統であるBA.1.1株は、BA.1株が持つ30カ所以上の変異に加えて、スパイク蛋白質346番目のアミノ酸の、アルギニン (R)からリジン (K)への変異(R346K)持っている。オミクロン株が出現する以前に、変異株の中で従来株から抗原性が最も変化した株であったミュー株もR346K変異を有していた。抗体が持つウイルスの細胞への感染を阻害する機能 (中和活性)をさらに低下させる可能性が示唆されていた。
レムデシビル (販売名:ベクルリー点滴静注液)は令和2年5月7日に特例承認を受けた。モ ルヌピラビル (販売名:ラゲブリオ)は令和3年12月24日に特例承認を受けた。ニルマトレ ルビル・リトナビル (販売名:パキロビッドパック)は令和4年2月10日に特例承認を受けた。S-217622は臨床試験中。https://www.mhlw.go.jp/content/10900000/000938454.pdfを参照。
(注2) オミクロン/BA.1変異株:
新型コロナウイルスは、ウイルス粒子表面に存在するスパイク蛋白質を使って、宿主細胞表面のウイルス受容体に結合することで、標的細胞への感染を開始する。BA.1変異株は、従来株と比較して、そのスパイク蛋白質に30カ所以上のアミノ酸変異を有している。これらのスパイク蛋白質におけるアミノ酸変異は、抗体薬の効果を減弱させる可能性がある。
(注3) 抗体薬:
カシリビマブ・イムデビマブ (販売名:ロナプリーブ注射液セット)は令和 3 年 7 月 19 日に特例承認を受けた。ソトロビマブ (販売名:ゼビュディ点滴静注液)は令和 3 年 9 月 27 日に特例 承認を受けた。チキサゲビマブ・シルガビマブ (開発コード:AZD7442)は臨床試験中。 https://www.mhlw.go.jp/content/10900000/000938454.pdfを参照。
(注4) オミクロン/BA.1.1変異株
BA.1の亜系統であるBA.1.1株は、BA.1株が持つ30カ所以上の変異に加えて、スパイク蛋白質346番目のアミノ酸の、アルギニン (R)からリジン (K)への変異(R346K)持っている。オミクロン株が出現する以前に、変異株の中で従来株から抗原性が最も変化した株であったミュー株もR346K変異を有していた。抗体が持つウイルスの細胞への感染を阻害する機能 (中和活性)をさらに低下させる可能性が示唆されていた。
