| 発表のポイント |
|---|
|
研究の背景
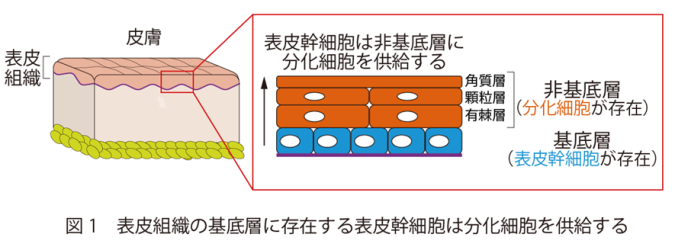
哺乳類の多くの組織には組織幹細胞が存在し、日々失われる細胞を自己複製や分化を介して補充することで、組織の恒常性を維持しています。DNAに損傷をひきおこす遺伝毒性ストレス(ゲノムストレス)※1は幹細胞から生じる子孫細胞全体へと影響を及ぼし恒常性の破綻へと繋がるため、受精卵から成体組織に至るまで、幹細胞のゲノム完全性の維持は生命にとって極めて重要です。一般的に、DNA二本鎖切断(DSB)※2などの細胞毒性の強いゲノムストレスが致死量に至ると細胞死を誘導する一方で、非致死的な場合にDNA損傷応答を経て細胞周期を不可逆的に停止する“細胞老化”(cellular senescence)※3に至ったり、最終的にがん化に至ったりすると考えられています。しかし、紫外線など日常的に経験するようなDNA二本鎖切断(DSB)を受けた細胞が、生体内で実際にどのような運命を辿っているのかについては、明らかにされていませんでした。皮膚の最外層に位置する表皮組織の最下層(基底層)には表皮幹細胞が存在し、自己複製しながら分化細胞を非基底層に供給することで外界との境界面でバリアとして働いています (図1)。表皮幹細胞は紫外線などのゲノムストレスに日々暴露されていますが、健常な若い個体の皮膚では、日焼けしても急激な老化やがん化は生じません。そこで、本研究グループは表皮組織ではゲノムストレスを受けた幹細胞を選択的に処理する未知の仕組みが存在する可能性を想定し、研究を行いました。
研究成果の概要
本グループは、マウスの皮膚が薄く赤くなる程度の紫外線量では、有意にアポトーシスを誘導しないことを確認したうえで、紫外線1回照射後の表皮組織の変化を経時的に観察しました。先行研究の結果通り、紫外線照射後は表皮幹細胞の増殖が亢進し、表皮の厚みが増す一方で、表皮幹細胞の数は変化しませんでした。また、DNA二本鎖切断(DSB)によるDNA損傷応答に伴うフォーカス形成が表皮幹細胞の存在する基底層に多く誘導された後に、分化細胞の存在する非基底層へと分布が変化する像を見出しました。これらの結果より、ゲノムストレスを受けた表皮幹細胞は基底層から非基底層へ移動し、最終的に組織から消失している可能性が示唆されました。
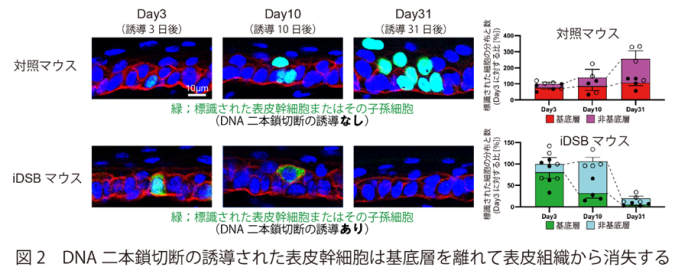
さらに、一部の表皮基底層にのみDSBを誘導し、かつ、その細胞の運命を遺伝学的に追跡※4可能なマウス(iDSBマウス)を用いた、ゲノムストレスを受けた細胞の追跡システムを新たに構築し、それらの細胞の運命を解析しました。その結果、DSBを誘導された表皮幹細胞は、分裂せずに基底層を離れて非基底層へと移動し、1ヶ月以内に表皮組織から消失することが明らかになりました(図2)。
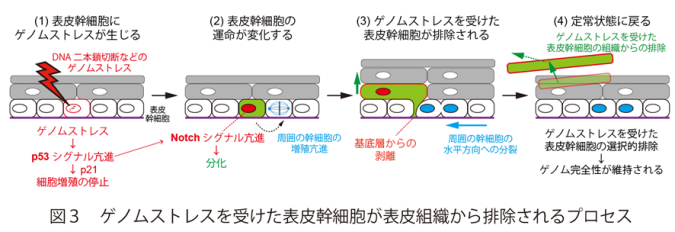
また、DSBを誘導した直後(該当の細胞が基底層に存在しているタイミング)に解析を行った結果、DSB誘導によりp53の発現およびリン酸化が誘導され、表皮幹細胞の分化を促進するNotchシグナルが亢進すること、および細胞増殖の停止に関与するp21の発現が亢進することを示しました。
さらに、一部の表皮基底層にのみDSBを誘導し、かつ、その細胞の運命を遺伝学的に追跡※4可能なマウス(iDSBマウス)を用いた、ゲノムストレスを受けた細胞の追跡システムを新たに構築し、それらの細胞の運命を解析しました。その結果、DSBを誘導された表皮幹細胞は、分裂せずに基底層を離れて非基底層へと移動し、1ヶ月以内に表皮組織から消失することが明らかになりました(図2)。
また、DSBを誘導した直後(該当の細胞が基底層に存在しているタイミング)に解析を行った結果、DSB誘導によりp53の発現およびリン酸化が誘導され、表皮幹細胞の分化を促進するNotchシグナルが亢進すること、および細胞増殖の停止に関与するp21の発現が亢進することを示しました。
研究成果の意義
過去の研究では、ゲノムストレスを受けた細胞を特異的に可視化し追跡することができなかったため、それらの細胞は①アポトーシスなどによる細胞死とその貪食により処理されるか、②不可逆的に増殖を停止して(細胞老化(senescence))組織に残るか、③DNA損傷修復を受ける際に変異を獲得してがんの発生源になると考えられてきました。本研究では、新たに開発した、DNA損傷を受けた表皮幹細胞の追跡システムを用いた解析の結果、これらの細胞は細胞周期を停止し最終分化へとコミットし(老化分化と命名)組織から排除されることを明らかにしました。このことから、上皮が自律的に幹細胞を選択し、そのゲノム品質を管理する機構を備えており、上皮自身が早期の老化や癌化を防いでいることが明らかになりました。本研究において細胞毒性の強いDNA二本鎖切断(DSB)を受けた幹細胞はp53-Notch-p21シグナルを介して老化分化することが判明しましたが、加齢した皮膚ではp53やNotchの変異クローンが定着しやすいことから、上記機構の回避により癌化リスクを亢進させていると考えられます。今回発見した選択機構が哺乳類の表皮に限らず種や系譜を超えて広く多細胞生命のゲノム品質管理を担っているのか、普遍性の検証が待たれます。また、加齢関連疾患の予防や治療への応用が期待されます。
用語解説
※1ゲノム(DNA全体の遺伝情報)がストレスを受けると、遺伝情報が変化したり失われたりする。その結果、がん化や老化などの、恒常性の破綻に繋がることが知られている。※2DNAは二重らせん構造を取っていますが、その両方の鎖が切断されることをDNA二本鎖切断と呼ぶ。DNA二本鎖切断はゲノムストレスの中でも、最も重大な影響を及ぼすものの一つとして知られている。
※3細胞増殖が非可逆的に停止した状態を細胞老化(senescence:セネッセンス)と呼ぶ。がん(細胞の異常増殖)に対する防御機構として働くほか、老化細胞が出す分泌因子等により組織の老化の一因になると考えられている。
※4遺伝子組換えによって特定の細胞に標識を行い、該当細胞および、その細胞から生み出される細胞の運命を追跡することが可能になる。今回の研究で用いたiDSBマウスでは、DNA二本鎖切断が生じた細胞、およびその細胞から生み出された細胞特異的に、特定の配列のペプチド(HAタグ)および蛍光タンパク質(GFP)が発現するよう標識されている。
論文情報
掲載誌: Developmental Cell論文タイトル: Dynamic stem cell selection safeguards the genomic integrity of the epidermis
著者: Tomoki Kato, Nan Liu, Hironobu Morinaga, Kyosuke Asakawa, Taichi Muraguchi, Yuko Muroyama, Mariko Shimokawa, Hiroyuki Matsumura, Yuriko Nishimori, Li Jing Tan, Motoshi Hayano, David A. Sinclair, Yasuaki Mohri, and Emi K. Nishimura.
DOI: 10.1016/j.devcel.2021.11.018
【研究者プロフィール】
加藤 智起(カトウ トモキ) Tomoki Kato
東京医科歯科大学 難治疾患研究所 幹細胞医学分野 大学院生
・研究領域 幹細胞生物学、皮膚科学など
西村 栄美 (ニシムラ エミ) Emi K. Nishimura
東京大学医科学研究所 老化再生生物学分野 教授
東京医科歯科大学 難治疾患研究所 幹細胞医学分野 教授
・研究領域 幹細胞生物学、老化・再生生物学、皮膚科学、実験病理学など
問い合わせ先
<研究に関すること>東京大学医科学研究所 老化再生生物学分野
東京医科歯科大学 難治疾患研究所 幹細胞医学分野
西村 栄美(ニシムラ エミ)
https://www.ims.u-tokyo.ac.jp/imsut/jp/lab/cancerbiology/page_00158.html
<報道に関すること>
東京医科歯科大学 総務部総務秘書課広報係
https://www.tmd.ac.jp/outline/contact/
東京大学医科学研究所 国際学術連携室(広報)
https://www.ims.u-tokyo.ac.jp/imsut/jp/
