| 発表のポイント |
|---|
|
発表概要
東京大学医科学研究所 東京大学特任教授部門 粘膜免疫学部門/千葉大学国際粘膜免疫・アレルギー治療学拠点の清野宏特任教授、東京大学医科学研究所 附属国際粘膜ワクチン開発研究センターの幸義和特任研究員、附属病院アレルギー免疫科の田中廣壽教授(研究当時)、先端医療開発推進分野の長村文孝教授、健康医療インテリジェンス分野の井元清哉教授、および大阪市立大学大学院医学研究科 ゲノム免疫学の植松智教授(東京大学医科学研究所 附属国際粘膜ワクチン研究開発センター 自然免疫制御分野 特任教授 兼務)らのグループは、コレラ毒素(CT)のBサブユニット(CTB)をワクチン抗原として、イネ種子に発現させたコメ型経口ワクチン「ムコライス」(MucoRice-CTB、IMSUT-MR1501)の健康成人を対象とした医師主導第I相試験において有効性(免疫原性)と安全性、忍容性を確認しました(図1)。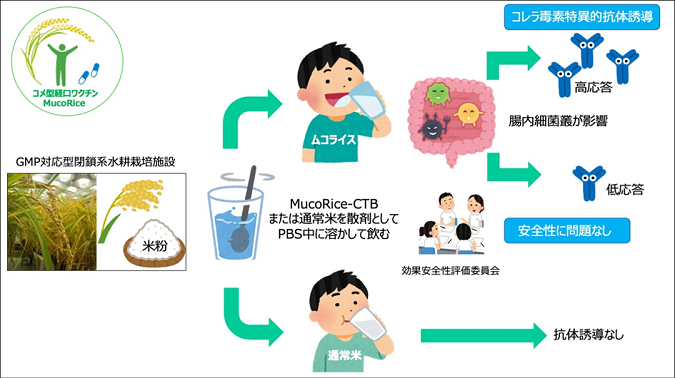
コレラ菌感染による下痢症は発展途上国では未だに大きな問題であり、年間約130-400万人の感染者とそれに起因する2−14万人の死者が出ています。また、毒素原性大腸菌感染による下痢症は、年間約260万人の患者数が報告されています。
「ムコライス」(MucoRice-CTB)の下痢症予防ワクチンとしての有効性は、実験動物レベルでは確認されていましたが、ヒトに投与したときの有効性(免疫原性)と安全性を今回、新たに確認することができました(図1、図2、図3)。また、ワクチンに対する免疫応答は被験者の腸内細菌叢と深い関わりがあることが明らかになりました(図1、図4)。「ムコライス」(MucoRice-CTB)はコレラ毒素(CT)による下痢症だけではなく、毒素原性大腸菌由来易熱性毒素(LT)による下痢症にも効果のある可能性が示されました。
これらの成果は、発展途上国におけるCTによる下痢症のみならずLTや志賀毒素(注3)が原因の旅行者下痢症の予防に役立つと考えられます。「ムコライス」(MucoRice-CTB)は常温保存が可能であり、コールドチェーン(低温物流)不要の世界的規模の安価なワクチンを供給できる可能性があります。
本研究成果は2021年6月25日(英国夏時間)、英国科学雑誌「The Lancet Microbe」オンライン版で公開されました。
本研究成果は、文部科学省(MEXT)/国立研究開発法人日本医療研究開発機構(AMED)の橋渡し研究加速ネットワークプログラムにより2014年度、2015年度の支援を受け、地球規模課題対応国際科学技術協力プログラム(SATREPS 15jm0110012h0101, 17jm0110012h0003, 18jm0110012h0004, 19jm0110012h0005, 20jm0110012h0006)の一環として得られました。
また、日本学術振興会(JSPS)、科学研究費助成事業(B16K16144,18K18148)の支援も受けました。
発表内容
コレラ菌感染症が蔓延している発展途上国におけるワクチン接種の現場・フィールドでの課題・ニーズを考慮すると、ワクチンの冷蔵保存及びコールドチェーンの必要なく、感染性医療廃棄物となる使い捨て注射器・針も出ないワクチン開発が必要となります。これらの条件をクリアする目的で、粘膜ワクチンの開発が進められてきました。近年、コレラ菌や毒素原性大腸菌感染に起因する下痢症を予防する目的で、3種類(Shanchol, Euvichol, Dukoral)の不活化経口ワクチンが開発、上市されましたが、冷蔵保存が基本でした。また、健康成人に加え、幼児、子供や高齢者にワクチンを投与することを考えると、死菌・不活化ではなく安全性が高いリコンビナント精製ワクチン抗原によるサブユニットタイプの経口ワクチンが理想でした。
そこで、清野宏特任教授らの研究グループは、ワクチンの長期常温保存性、経口安定性、低コスト生産性という観点から、組換え植物の技術を用いてイネ種子にワクチン抗原遺伝子(CTB)を組み込むワクチン発現米「ムコライス」(MucoRice-CTB)を開発しました。これを経口ワクチンとして投与することにより、マウスや実験用大動物であるブタ、ヒトにより近い霊長類で、抗原特異的抗体を誘導できることを証明しました(図2)。さらに、「ムコライス」(MucoRice-CTB)経口ワクチンはコレラ毒素による下痢症だけではなく、旅行者下痢症の原因の一つである毒素原性大腸菌由来易熱性毒素による下痢症にも効果のある可能性が示されました。
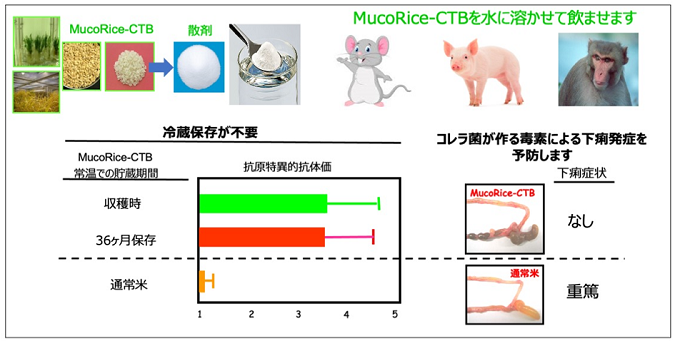
研究グループでは、「ムコライス」(MucoRice-CTB)のヒトでの概念実証(Proof of Concept: POC)を目指しGMP(注4)対応型完全閉鎖系MucoRice水耕栽培システムの構築を進めてきました。このシステムのもとで栽培されたGMP規格の「ムコライス」(MucoRice-CTB)を用いて医師主導型第I相試験を東京大学医科学研究所附属病院にて二重盲検、プラセボ対照、ランダム化比較試験にて実施しました(臨床治験登録番号:UMIN000018001)。
被験者は海外渡航歴と下痢症の関連がない健康成人男子(20−40歳)計60人を無作為に選択し、3つのコホートでの用量漸増試験を行いました。それぞれのコホートは「ムコライス」(MucoRice-CTB)投与群(10人)とプラセボ群(10人)で構成され、ワクチン投与群は、PBS(リン酸緩衝生理食塩水)に懸濁した1g、3g、または6gの「ムコライス」(MucoRice-CTB)散剤を、プラセボ群も同量の野生米を、2週間おきに4回経口摂取しました。最終経口投与より2か月後をエンドポイントとし、この間にスケジュールに沿った血清と糞便サンプルを採取しました。血清は、ELISA法にてCTB特異的抗体価を測定し、糞便サンプルからは細菌のDNAを抽出して次世代シーケンサーを用いて腸内細菌叢のメタゲノム解析を行いました。
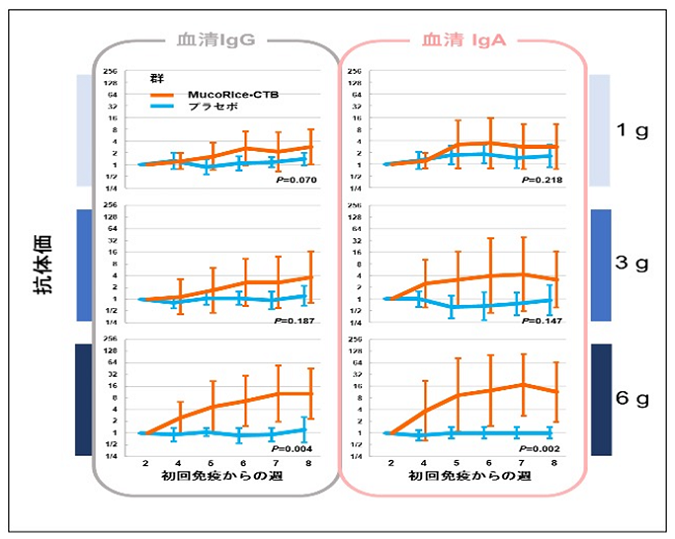
医科学研究所内に設置された第三者専門家から構成される「効果安全性評価委員会」により同試験を通じ重篤な有害事象は認められず、「ムコライス」(MucoRice-CTB)経口投与群ではプラセボ群と比較して、投与用量に依存して顕著にCTB特異的な血清IgGとIgA抗体の上昇が認められました(図3)。これらのCTB特異的抗体には類似抗原であるLTBとも交叉反応する事が明らかになりました。したがって、「ムコライス」(MucoRice-CTB)経口投与で誘導された抗体には毒素(CT,LT注1,2)が粘膜上皮細胞上のGM1レセプターに結合するのを阻害し、それぞれの毒素に対する中和活性がある事が試験管レベルで明らかになりました。
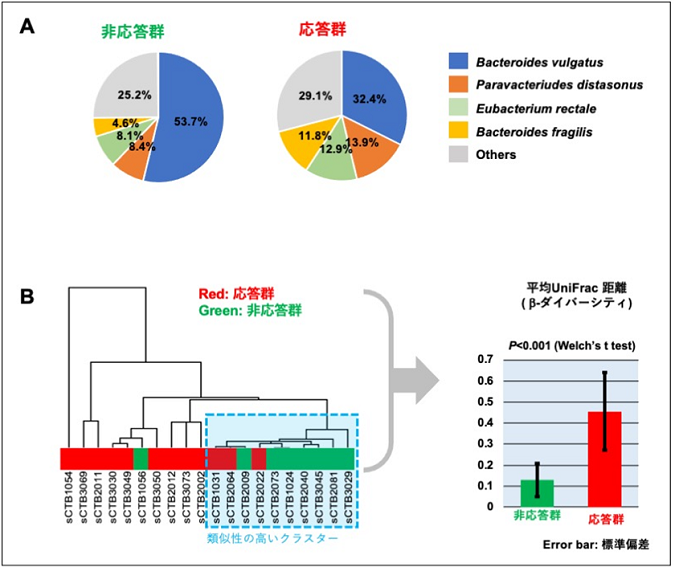
さらに、近年注目されている腸内細菌叢が、「ムコライス」(MucoRice-CTB)経口ワクチンの免疫応答と関わっていることも分かってきました。糞便サンプル中細菌DNAのメタゲノム解析を行ったところ、コメ型経口ワクチン「ムコライス」(MucoRice-CTB)応答群では非応答群に比べて、腸内細菌叢の多様性(注5)が有意に高く(図4A)、クラスター分析(注6)で完全に両群の分別が可能でした(図4B)。また応答群には大腸菌や赤痢菌等のDNAが有意に多く、Bacteroidesが有意に少なく検出される特徴がある事が明らかになりました。
対象者を拡大して実施される臨床試験および製品化に向け、LEDなど最新の光源システムを応用し低コストかつ大量安定供給ができる「ムコライス」(MucoRice-CTB)栽培システムの確立を目指しており、千葉大学大学院園芸学研究科で植物工場に関する研究を行っている後藤英司教授をはじめとする植物系・工学系研究者や、イネ遺伝子改変・発現を専門とした農学系研究者そして空調・設備・機器企業の朝日工業社などとの異分野融合研究を継続的に取り組んでいます。
発表雑誌
雑誌名:The Lancet Microbe(オンライン版)論文タイトル:Oral MucoRice-CTB vaccine for the safety and microbiota-dependent immunogenicity in humans: A Phase 1 Randomized Trial
著者:Yoshikazu Yuki, Masanori Nojima, Osamu Hosono, Hirotoshi Tanaka, YasumasaKimura, Takeshi Satoh, Seiya Imoto, Satoshi Uematsu, Shiho Kurokawa, Koji Kashima, Mio Mejima, Rika Nakahashi-Ouchida, Yohei Uchida, Takanori Marui, Noritada Yoshikawa, Fumitaka Nagamura, Kohtaro Fujihashi, Hiroshi Kiyono*
(*責任著者)
DOI:10.1016/S2666-5247(20)30196-8
URL:https://doi.org/10.1016/S2666-5247(20)30196-8
用語解説
(注1)コレラ毒素(CT)1分子のAサブユニットと5分子のB サブユニットからなるコレラ菌が産生する毒素。B サブユニット5量体(CTB)は無毒で、その受容体である宿主が有する糖脂質GM1ガングリオシドと結合します。Aサブユニットは毒素本体でありADPリボシルトランスフェラーゼ活性を持ちます。
(注2)毒素原性大腸菌由来易熱性毒素(LT)
コレラ毒素と同様の1分子のAサブユニットと5分子のB サブユニットからなる毒素原性大腸菌が産生する毒素です。AサブユニットとB サブユニット(LTB)はコレラ毒素と同様の活性があり、特にLTBは無毒でありCTBとアミノ酸レベルで高い相同性を示します。
(注3)志賀毒素
赤痢菌、及び腸管出血性大腸菌(例O157)が産生する毒素で1分子のAサブユニットと5分子のB サブユニットで構成されています。CTやLT同様、Aサブユニットは毒素本体、B サブユニットは宿主の受容体(Gb3)と結合します。腸管などの微小血管に作用し、出血を引き起こします。
(注4)GMP
Good Manufacturing Practiceの略。医薬品及び医薬部外品の製造管理と品質管理の基準を示したもの。
(注5)多様性
サンプルの種の多さの指標で、値が大きいほど種の多様性が高いことを示します。いくつかの指標がありますが、βダイバーシティは異なったサンプル間の種の多様性(相違)を表します。2サンプル間の距離として表現される指標(ここではUniFrac距離)が大きくなるほど、2 つのサンプルの組成が異なり多様性が大きいと評価されます。
(注6)クラスター分析
数量的な分析結果を基に、サンプルの類似度を評価してクラスターを作成し分類を行う方法のこと。
問い合わせ先
〈研究に関すること〉東京大学医科学研究所 東京大学特任教授部門 粘膜免疫学部門
特任教授 清野 宏(きよの ひろし)
https://www.ims.u-tokyo.ac.jp/imsut/jp/lab/dstngprof/section02.html
〈報道に関すること〉
東京大学医科学研究所 国際学術連携室(広報)
https://www.ims.u-tokyo.ac.jp/imsut/jp/
