研究分野紹介

採取から提供まで、細胞製品製造を支援!
教授:長村 登紀子 附属病院セルプロセッシング・輸血部
医科研には、3種類の細胞調製室がある(まとめて「医科研CPF」という)。医科研病院のセルプロセッシング・輸血部においては、アフェレーシス等細胞原料の採取や最小限の採取や移植前の細胞調製を行う「細胞処理室」と細胞培養加工施設「東大医科研細胞リソースセンター(IMSUT-CRC)」(届出番号;FC3150141)が稼働している。IMSUT-CRCクリーンルームでは、これまで東京臍帯血バンク(現在、日赤バンクに統合)の細胞調製、樹状細胞療法や骨髄由来間葉系細胞(MSC)を用いた歯槽骨再生医療や国内初の腎がん遺伝子治療等が行われてきた。また、研究所には共通施設として、製造所・製造業許可を取得している製造所「IMSUT-HLCセルプロセッシング施設(IMSUT-HLC-CPF)」(許可番号;第13FZ11008号)が稼働している。一方で、同種細胞治療には、その元となる細胞ソースが必要である。長村らは、ドナーに侵襲なく採取できる臍帯血と臍帯に着目し、東大医科研臍帯血・臍帯バンクを立上げた。これまで、急性GVHDに対する医師主導治験、新型コロナ感染症関連ARDSや脳性麻痺に対する企業治験用に臍帯由来MSCを製造・提供した引き続き、医科研CPFにて、原料細胞の提供や細胞調製等によりTRを支援する。

基礎研究から臨床応用までを支援する
教授:長村 文孝 先端医療研究センター先端医療開発推進分野
遺伝子治療や再生医療においても医薬品と同じような開発の過程を経て市販を目指しています。基礎研究の成果を基に産業化を念頭に特許を出願し、細胞や動物を用いた有効性・安全性に関する検討、人に投与できる品質を有しながら治験を行うことのできる大量製造の確立、人で有効性と安全性を検討する治験などの臨床試験の実施が開発の過程です。実際には、どの法律、どのガイドラインに従って実施するのか、それぞれの段階をどのように効率良く実施するのか検討することは難しい問題で、特に遺伝子治療や再生医療は前例に乏しいため難渋することが多いです。臨床試験では、人に初めて投与する量を安全性を考えどのように設定するのか、初回投与量に加えてどれくらいの投与量を試せばよいのか、1つの投与量で何人に投与すれば信頼性のあるデータが得られるのか、有効性と安全性を検討するためには何を調べれば良いのか、等々多くの検討事項があります。特許出願を目指す基礎研究の段階から臨床試験に至るまで、どのようにすれば迅速で効率的に開発を進めることができるのかを科学的に検討し、また研究者と共同して答えを出そうとしています。
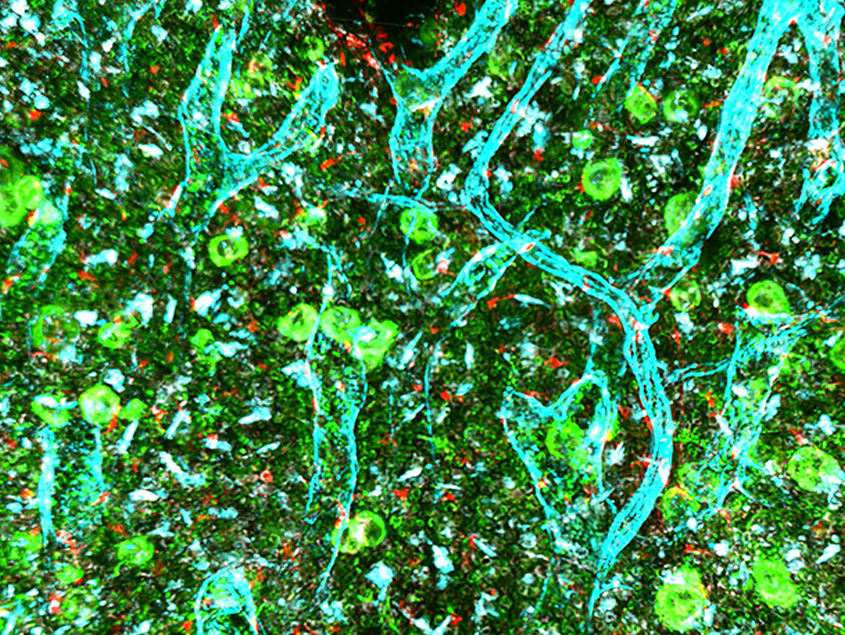
造血幹細胞を分子レベルで理解し、応用する
教授:岩間 厚志 幹細胞治療研究センター幹細胞分子医学分野
造血幹細胞は自己を複製する能力(自己複製能)および多様な細胞に変化する能力(分化多能性)の両方を有する細胞であり、個体の発生・維持において基幹となる細胞です。当研究室では、造血幹細胞の自己複製機構と分化の分子基盤を明らかにすることを主題とし、「幹細胞生物学」の真髄となる真理の探究とともに、造血幹細胞やその骨髄ニッチ細胞の操作を行う先端医療の確立に貢献する研究を目指しています。また、造血幹細胞制御機構の破綻が多くの造血器腫瘍につながることが明らかになり、その理解も重要なテーマとして取り組んでいます。特に、エピジェネティック制御機構の破綻が、白血病を始めとして様々な腫瘍で確認されており、その実態の解明とともにエピジェネティック治療法の開発についても重要なテーマとして研究を進めていきます。これらの研究から得られる知見を、再生医療・がん治療につなげることが最終的な目標です。
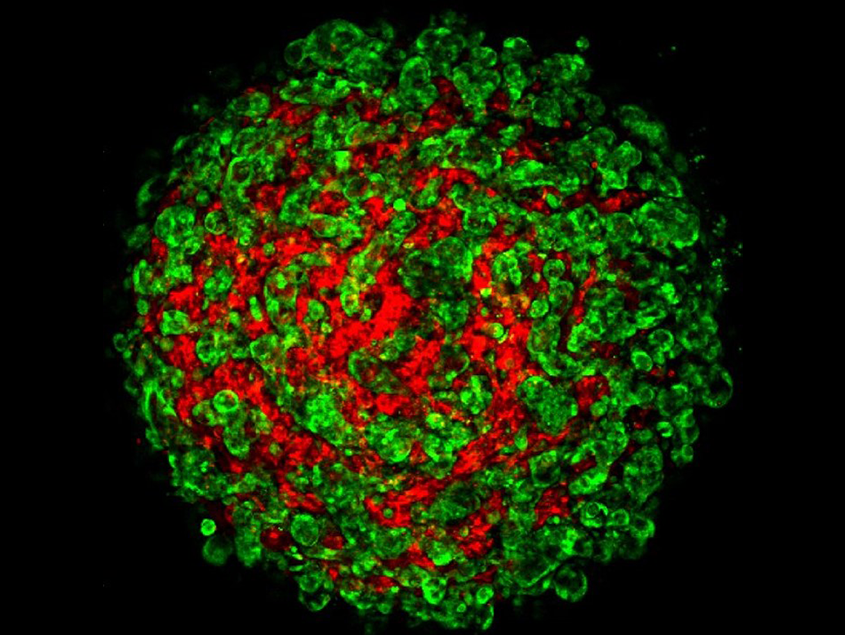
ヒトiPS細胞操作技術を駆使した再生医療の実現化
教授:谷口 英樹 幹細胞治療研究センター再生医学分野
「再生医学(Regenerative Medicine)」は、急速に解明の進みつつある発生生物学や幹細胞生物学の新知見を、臨床医学へ応用することを目指す挑戦的な学問領域です。現在、末期臓器不全症に対して臓器移植が有効な治療法として実施されていますが、年々、増大する移植ニーズと比較してドナー臓器の供給量は絶対的に不足しており、再生医療への期待が世界的に高まっています。当研究室では、ヒト多能性幹細胞(iPS細胞)等からヒト臓器を創出するためのオルガノイド培養技術や移植技術を開発し、臓器移植の代替となる新たな治療法を開発する研究を行っています。また、iPS細胞研究において確立した様々な細胞操作技術を「がん研究(Cancer Biology)」に応用し、がん特異的な微小環境を伴うヒト難治癌組織(癌オルガノイド)を人為的に再構成する手法を確立しています。この技術をもとに、癌の再発や転移を抑制するための創薬開発に繋げる研究を展開しています。
・再生医学分野HPのURL
http://re-medicine.stemcell-imsut.org/
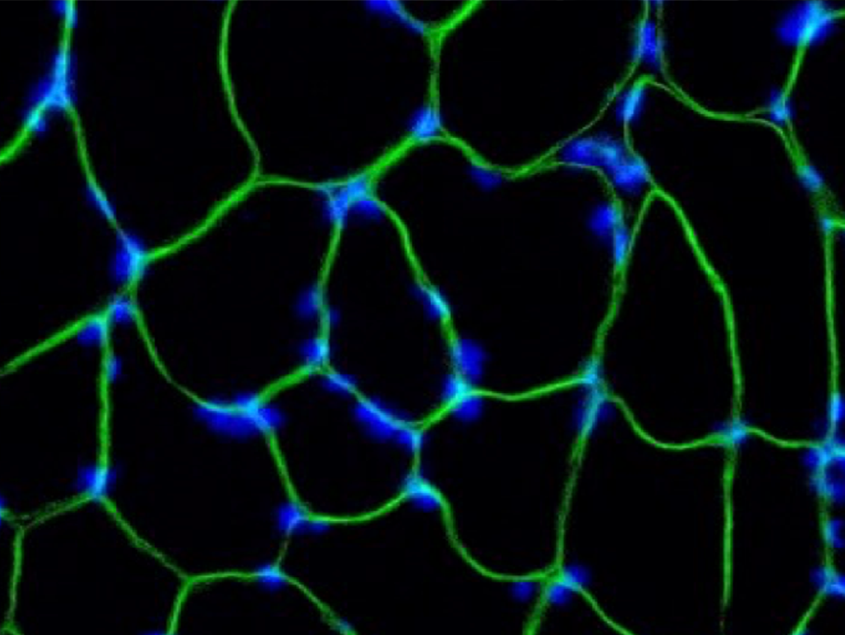
難治性神経筋疾患の分子病態解析と遺伝子細胞治療
教授:岡田 尚巳 遺伝子・細胞治療センター分子遺伝医学分野
難治性遺伝性神経筋疾患の分子病態解析、遺伝子・細胞治療の基盤技術開発、臨床的課題の解決を推進し、個別化ゲノム医療の包括的トランスレーショナルリサーチを目指しています。遺伝性疾患に対する遺伝子治療用製品として、治療遺伝子を組織に送達するウイルスベクターの開発は、分子病態に基づく明確な作用機序と臨床的効果から高い注目を集めています。特に神経筋疾患の治療において、アデノ随伴ウイルス(AAV)ベクターは優れた特性を有していますが、全身大量投与においては臓器障害の懸念も指摘されています。そこで私たちは、本格的な普及に向けベクターの安全性や生産性に関わる製造・分析の基盤技術開発に加え、間葉系細胞を用いた免疫調節によるベクター投与量の低減等、安全性・有効性やコストの優れた治療技術の開発を展開しています。また、探索研究における均質性や、非臨床試験薬・治験薬製造と製品製造における一貫性、同等性を考慮し、Quality by Designの考え方に基づいた製造プロセスの検証を推進しています。さらにこれらの取り組みを通じて、様々な領域で求められる教育・産業人材の育成を行い、将来の遺伝子細胞治療を支えることを目標としています。
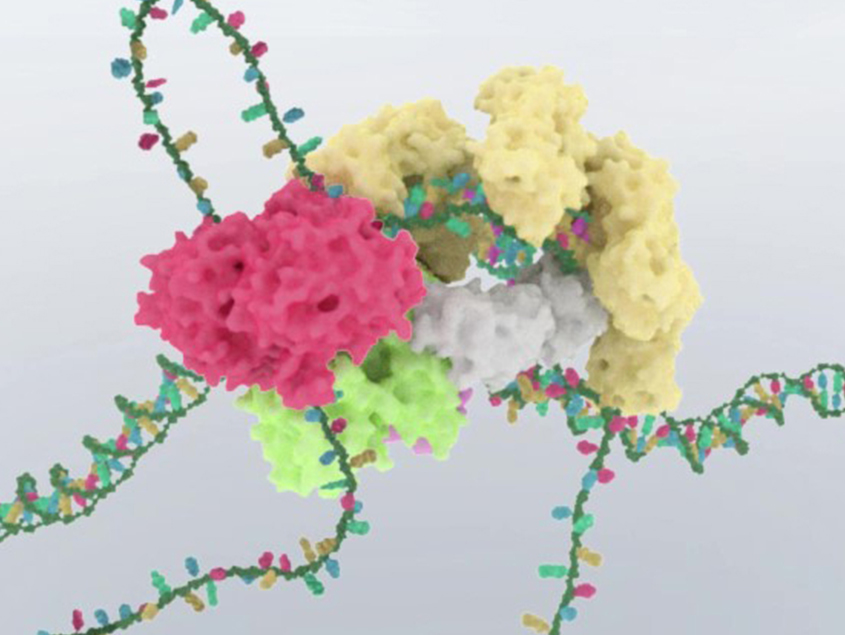
CRISPR-Cas3ゲノム編集による遺伝子治療の開発
教授:真下 知士 システム疾患モデル研究センターゲノム編集研究分野
ゲノム編集CRISPR-Cas9は、特定の遺伝子を狙って改変したり、機能を調節する革新的な技術です。私たちはCas9とは異なる日本発CRISPR-Cas3によるゲノム編集を開発しました。この技術は、再生医療でのヒトiPS細胞の編集、造血幹細胞での遺伝子編集による希少疾患治療、免疫T細胞を用いたがん治療などの「ex vivo遺伝子治療」に利用できます。さらに、AAVベクターやLNPデリバリー技術による「in vivo遺伝子治療法」を可能にします。また、CRISPR遺伝子発現調整やCRISPRライブラリを使用した基礎研究、創薬シーズの探索研究にも利用されています。さらに、感染症診断や遺伝子診断としてCRISPR-Dxも開発されています。様々な分野の共同研究者の方々と一緒に、このゲノム編集技術を利用した新しい治療薬、診断薬、ドラッグシーズの開発を目指します。
研究室のHP:
https://www.ims.u-tokyo.ac.jp/animal-genetics/index.html
造血幹細胞増幅を用いた遺伝子治療への臨床応用
教授:山崎 聡 システム疾患モデル研究センター 細胞制御研究分野
遺伝性血液疾患は、血液細胞の機能に重要な役割を果たす遺伝子の単一または複数の遺伝的変異によって引き起こされ、これまでに多種多様な疾患が報告されています。造血系の頂点に位置する造血幹細胞(HSC)はこれらの遺伝性血液疾患の原因となる変異を保有していることから、同種幹細胞移植が唯一の根本的治療法であると考えられています。一方で、同種幹細胞移植は人体の負担が大きく、複数の懸念点がある治療方法でもあります。この問題を払拭するために、我々のグループでは自己の疾患HSCにおける原因遺伝子をHSC体外増幅システムとゲノム編集及び遺伝子導入法との融合により編集、補完することで疾患HSCから正常HSCへと変換する、遺伝子治療システムを目指しています。








