自己免疫抑制のネガティブフィードバック制御―自己免疫疾患の発症抑制と癌免疫誘導のトレードオフ
自己免疫抑制のネガティブフィードバック制御―自己免疫疾患の発症抑制と癌免疫誘導のトレードオフ
私たちの体には、病原体など外来異物を排除する免疫機能が備えられています。免疫機能に重要なT細胞は胸腺で作られますが、自分の組織に応答する有害なT細胞は選択的に除かれ、自己免疫疾患の発症が抑制されます。これを自己免疫寛容と呼んでいます。最近、胸腺を構成する細胞の一群である髄質上皮細胞が、自己免疫寛容に必須であることが分かってきました。髄質上皮細胞は組織特異的に発現するタンパク質を多種類にわたって異所的に発現し、抗原提示します。それら自己抗原を認識するT細胞は細胞死により除去され、結果として自己組織タンパク質に対する自己免疫寛容が成立します。これまでに私たちのグループは、TNF受容体スーパーファミリーRANKのシグナルが胸腺髄質上皮細胞の分化を誘導し、自己免疫寛容に重要なことを報告しました。しかし、RANKのシグナルから髄質上皮細胞が分化するまでの過程において細胞内で起こる現象は不明でした。
今回、RANKシグナルが髄質上皮細胞でETSファミリー転写因子Spi-Bの発現を誘導することを発見しました。Spi-Bは組織特異抗原の一部や、T細胞の選択に必要な分子(CD80やCD86)に加えて、RANKシグナルを阻害するタンパク質OPGの発現を誘導していました。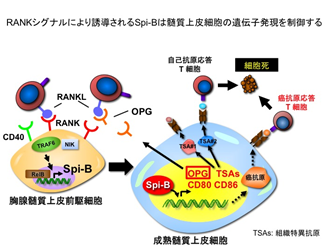 そしてSpi-BはOPGの発現を介して、RANKシグナルによって誘導される髄質上皮細胞の分化を抑制するという、ネガティブフィードバック機構を制御します(図)。
そしてSpi-BはOPGの発現を介して、RANKシグナルによって誘導される髄質上皮細胞の分化を抑制するという、ネガティブフィードバック機構を制御します(図)。
髄質上皮細胞は自己免疫疾患の発症抑制に必須です。にもかかわらず、髄質上皮細胞の分化を“抑制”する機構が、なぜ存在するのでしょうか?ネガティブフィードバック制御機構が働かないOPG欠損マウスでは、免疫応答を抑制する制御性T細胞が増加していました。興味深いことに、OPGを欠損する胸腺を持つマウスでは、癌細胞に対する免疫応答が弱まっていました。つまり、このネガティブフィードバック機構は、“有用な”自己組織と“有害な”自己組織である癌、に対する免疫応答の微妙なバランスを調整していると考えられます。
本研究の成果は、癌免疫寛容の誘導と自己免疫疾患の発症抑制機構の解明への貢献や、癌や自己免疫疾患の新しい治療法を開発する研究への展開が期待されます。
