血液線溶系の活性化は骨髄組織再生と造血系細胞分化増殖を促進する
血液線溶系の活性化は骨髄組織再生と造血系細胞分化増殖を促進する
我々はこれまで金属要求性蛋白分解酵素の一つであるマトリックスメタロプロテイナーゼ(MMP)、特にMMP-9が組織幹細胞の分化増殖また末梢組織の再生に重要な役割を担っていることを報告してきた(Cell 2002, Nat Med. 2002, Nat Med 2006)。これらの研究過程においてMMPの活性化が骨髄中の幹細胞因子(Kit-ligand)のプロセシングを誘導し、骨随組織幹細胞及びその前駆細胞の分化増殖あるいはその再生を促進することが明らかとなっている。近年、血液中の血栓形成等に関与する線維素溶解系因子プラスミンは、生体内潜在酵素であるproMMPをMMPへと活性化する作用を有することが解明された。生体内では、プラスミンはプラスミノーゲンアクチベーター(PA)の作用により、その前駆体プラスミノーゲン(Plg)から迅速に活性化され、生成することが広く知られている。
我々はPlg遺伝子欠損マウス(Plg-/-)とその野生型(Plg+/+)との間で、細胞周期特異性抗癌剤5-フルオロウラシル(5-FU) 250mg/kgの投与により骨随組織傷害を誘導したところ、Plg+/+はほぼ一ヶ月以内に骨髄細胞数、白血球数も回復し、100%生存したのに対し、Plg-/-は著しい骨髄組織傷害、造血機能低下が継続し、二週間以内に全てのマウスが死亡した。免疫特殊染色法で、Plg+/+では、5-FU投与後2-3日の間、骨芽細胞ニッチ付近で、プラスミノーゲン及びプラスミンの活性化を認め、さらに骨髄細胞の細胞表面マーカー、細胞周期解析により、Plg-/-では骨随細胞の分化障害が存在することが解った。
またこの原因について精査したところ、Plg-/-では、MMP(-2及び9)の活性化及びKit-ligand産生の有意な障害が存在することが明らかとなった。そこで我々はKit-ligandを、Plg-/-に投与したところ、5-FUによる骨随組織傷害からの再生機能が回復し、生存率も有意な改善を認めたことから、Kit-ligandを介した骨随組織再生機構におけるプラスミンの重要性を確信した。また骨随中の幹細胞ニッチを構成するストローマ細胞にtPAを供給する機能があることも見出した。
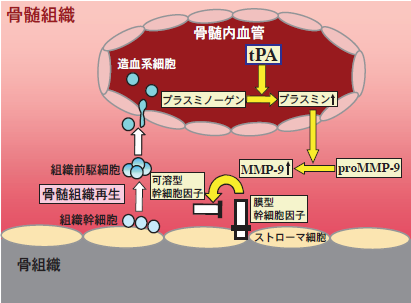 組織型PA(tPA)をPlg+/+、Plg-/-、MMP-9-/-加えてKit-ligandの遺伝子が欠落したSl/Sldマウスに投与したところ、まずPlg+/+についてのみ、Kit-ligand産生の増加とこれに伴う骨髄細胞の有意な増加が認められ、さらにPlg+/+においてtPAは、細胞表面マーカー及び細胞周期解析により骨髄組織幹細胞(骨随中のSca-1陽性c-Kit陽性細胞分化抗原陰性分画、長期培養開始細胞: long-term culture-initiating cell)の分化増殖を促進することが判明した。
そこで我々は5-FUによる骨随組織傷害をPlg+/+、Plg-/-、MMP-9-/-に誘導し、tPAを前述のプロトコールで投与したところ、Plg+/+では、骨随組織再生、さらに骨髄細胞の成熟分化が有意に促進され、かつ5-FU投与後の生存率にも有意な向上が認められた。本研究成果は、組織再生の新機構と、これを活用した再生医療の新たな可能性について提示したものであり、特に倫理面、免疫反応の点で安全性の高い組織幹細胞を使用していること、tPAが、既に臨床に普及した薬剤であること等の理由から、本研究成果は臨床応用への至近距離に位置づけられるものと考えられる。
組織型PA(tPA)をPlg+/+、Plg-/-、MMP-9-/-加えてKit-ligandの遺伝子が欠落したSl/Sldマウスに投与したところ、まずPlg+/+についてのみ、Kit-ligand産生の増加とこれに伴う骨髄細胞の有意な増加が認められ、さらにPlg+/+においてtPAは、細胞表面マーカー及び細胞周期解析により骨髄組織幹細胞(骨随中のSca-1陽性c-Kit陽性細胞分化抗原陰性分画、長期培養開始細胞: long-term culture-initiating cell)の分化増殖を促進することが判明した。
そこで我々は5-FUによる骨随組織傷害をPlg+/+、Plg-/-、MMP-9-/-に誘導し、tPAを前述のプロトコールで投与したところ、Plg+/+では、骨随組織再生、さらに骨髄細胞の成熟分化が有意に促進され、かつ5-FU投与後の生存率にも有意な向上が認められた。本研究成果は、組織再生の新機構と、これを活用した再生医療の新たな可能性について提示したものであり、特に倫理面、免疫反応の点で安全性の高い組織幹細胞を使用していること、tPAが、既に臨床に普及した薬剤であること等の理由から、本研究成果は臨床応用への至近距離に位置づけられるものと考えられる。
