酵母の浸透圧センサーの発見と高浸透圧を感知する仕組みの解明
酵母の浸透圧センサーの発見と高浸透圧を感知する仕組みの解明
生物が生きていくためには外的環境に適応することが必要であり、浸透圧の変化に対する適応反応も生物の生存に極めて重要です。細胞が高浸透圧環境に適応するためには、まず高浸透圧環境を細胞が感知する必要がありますが、物理化学的刺激である浸透圧を何がどのように感知するのかについてはよくわかっていません。本研究で私たちは、モデル生物の出芽酵母において高浸透圧を感知するセンサータンパク質を発見し、高浸透圧感知の作用機作を分子レベルで明らかにしました。
出芽酵母は高浸透圧環境に曝されると、Hog1キナーゼをリン酸化・活性化して細胞内のグリセロール濃度を上昇させ、細胞内外の浸透圧差を解消することで高浸透圧環境に適応します。Hog1のリン酸化には上流のキナーゼであるSte20、Ste11、Pbs2が順次リン酸化・活性化することが必要ですが、これらのキナーゼはHkr1, Opy2, Sho1という膜タンパク質とそれぞれ複合体を形成しているため、細胞膜が一連のリン酸化反応の場となります。本研究では、高浸透圧に応答した一連のリン酸化反応は4回膜貫通タンパク質のSho1による高浸透圧の感知が引き金になって誘起される、いいかえればSho1こそが高浸透圧センサーであることを明らかにしました。まず、Sho1は高浸透圧刺激によって構造変化をおこし、細胞内アダプタータンパク質のSte50と結合するようになることを見いだしました(図A)。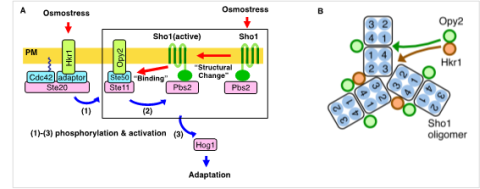 Ste50はOpy2膜アンカー及びSte11 MAPKKキナーゼと結合し、Sho1はPbs2 MAPKキナーゼと結合することから、高浸透圧下、Sho1とSte50との結合が誘導されると、Ste11→Pbs2へのリン酸化・活性化がひきおこされることになります。高浸透圧条件下にも関わらず構造変化をおこさない変異型Sho1では、高浸透圧によるSte50との結合誘導及びHog1のリン酸化が起きないこと、Hkr1やOpy2など他の膜タンパク質の存在なしでもSho1の構造変化は起きることなどから、Sho1は高浸透圧を感知しその構造変化を介して細胞内に活性化シグナルを伝達する自立的な浸透圧センサーであると考えられます。
Ste50はOpy2膜アンカー及びSte11 MAPKKキナーゼと結合し、Sho1はPbs2 MAPKキナーゼと結合することから、高浸透圧下、Sho1とSte50との結合が誘導されると、Ste11→Pbs2へのリン酸化・活性化がひきおこされることになります。高浸透圧条件下にも関わらず構造変化をおこさない変異型Sho1では、高浸透圧によるSte50との結合誘導及びHog1のリン酸化が起きないこと、Hkr1やOpy2など他の膜タンパク質の存在なしでもSho1の構造変化は起きることなどから、Sho1は高浸透圧を感知しその構造変化を介して細胞内に活性化シグナルを伝達する自立的な浸透圧センサーであると考えられます。
さらにSho1は極めてユニークな多量体構造をとっていることが示されました。クロスリンク法を用いた生化学的な解析等から、Sho1は4つの膜貫通ドメイン(TM)のうちTM1/TM4面でホモ二量体を、TM2/TM3面でホモ三量体を作り、その繰り返しにより細胞膜上で平面格子状の多量体構造を形成していることを見いだしました(図B)。またTM1/TM4面でOpy2、TM2/TM3面ではHkr1と結合し、その結合はHog1の活性化に重要であったことから、Sho1はセンサーとしての機能に加えて、複数の膜タンパク質-キナーゼ複合体が細胞膜上で相互作用するためのプラットフォームとしての機能も有することが明らかになりました。
本研究により浸透圧センサーとして膜タンパク質が高浸透圧の感知に働く分子機構の一端が明かされたことで、今後、細胞が物理化学的刺激である高浸透圧をセンシングする仕組みの全容解明につながることが期待されます。
[Nat. Commun 6:6975]
