ヒトiPS細胞由来の機能的血小板産生
ヒトiPS細胞由来の機能的血小板産生
複数のヒトiPS細胞株を比較することで、初期化因子の一つであるc-MYCの発現の挙動が巨核球成熟、血小板放出を規定すること、ヒトiPS細胞由来の血小板は生体内でも血栓形成能を保持していることを明らかにしました。遺伝子操作を加えることで、ヒトiPS細胞由来血小板が効率よく産生されることが確認され、安定した血小板製剤のソースとして期待されます。
[詳説] 血小板は生体内のホメオスタシスを保つ為に必須の無核の機能細胞です。各種悪性腫瘍に対する抗がん剤治療、骨髄移植後の致命的な血小板減少、先天性血小板減少症の大量出血時に対しては、血小板輸血が現段階の唯一の対症療法ですが、これらは現在全て献血に依存している状態です。本邦での献血者の急激な減少、ウイルス感染症に汚染された献血者の増加も加わることで献血に代わる安定した輸血ソースを開発する研究が求められるようになってきています。また献血医療の問題点として、繰り返し血小板輸血を行うことで、主にヒト白血球型抗原(HLA)に対する抗体が産生され、血小板輸血に対して不応症になってしまうことも挙げられます。ヒト誘導型多能性幹(iPS)細胞は試験管内で無限に増殖可能であること、HLAの一致した細胞を提供できることから、我々は免疫学的に拒絶の受けない血小板を安定して産生することができるソースとして注目しました。
本研究では複数のヒトiPS細胞株からの試験管内での血小板産生効率を比較することで、①c-MYCの発現上昇が未熟な巨核球増殖を促進する一方、成熟過程においてはc-MYCの発現低下が必須であること、②産生されたiPS細胞由来血小板は生体内で血栓形成能を有していることを明らかにしました。
ヒト皮膚細胞から、レトロウイルスによる初期化4因子(OCT3/4、SOX2、KLF4、c-MYC)および、3因子(c-MYCを除く)導入により樹立した複数のヒトiPS細胞を巨核球へ分化誘導したところ、4因子により樹立されたクローンで有意に巨核球/血小板の産生効率が高いことが分かりました。外来遺伝子の発現をRT-PCRにより確認したところ、遺伝子のランダムな再活性化が観察されましたが、特に4因子クローンにおいては、全てにc-MYC遺伝子の再活性化が認められ、巨核球造血におけるc-MYCの関与が示唆されました。
c-MYCは多能性幹細胞やガン細胞などで重要な役割を果たしている転写因子です。血小板の前駆細胞である巨核球系特異的にc-MYCを強制発現するトランスジェニックマウスにおいては、未熟巨核球細胞の増殖、及び成熟巨核球の減少することが報告されています。一方、血液細胞系列特異的なc-MYCのコンディショナルノックアウトマウスでも、未熟巨核球細胞の増殖、及び成熟巨核球の減少が報告されており、巨核球増殖・成熟におけるc-MYCの役割は未解明な点が残されています。さらにヒト巨核球造血におけるc-MYCの役割は未だ明らかになっていません。
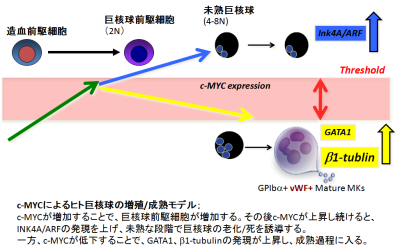
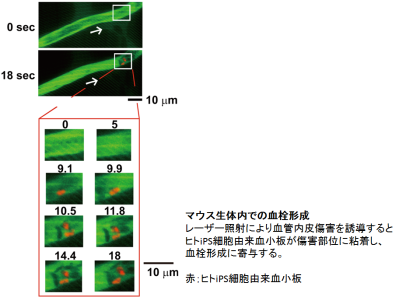
そこでヒトES細胞由来の造血前駆細胞にレトロウイルスを用いて初期化4因子を単独で強制発現させたところ、c-MYCのみが未熟な巨核球増殖を誘導すること、一方で、これらの細胞からは血小板放出が著明に低下していることが分かりました。c-MYCを含む4因子で樹立されたiPSクローン株の複数を詳細に比較すると、いずれも巨核球数は増えますが、1個あたりの巨核球からの血小板放出に差があることが判明しました。それぞれのクローン由来のa)造血前駆細胞、b)未熟巨核球、c)成熟巨核球の段階での遺伝子発現を確認したところ、いずれのクローンもc-MYCが造血前駆細胞段階では強く発現しておりましたが、その後のc-MYCの発現量が大きく異なり、血小板を多く産生するクローンは、c-MYC発現が成熟巨核球に発達する段階毎に経時的に減少していました。一方c-MYCの高い発現が維持されるクローンにおいては、1個の巨核球あたりの血小板数や血小板放出の課程である胞体突起(プロプレイトレット)形成が減少していることが分かりました。c-MYCの高い発現が維持されることで、生体防御機構の一つであるガン抑制遺伝子INK4AやARFの誘導され、さらに巨核球成熟に必須な転写因子であるGATA1の発現が抑制されることで成熟が阻害されていました。本分子の再活性化が起きないiPS細胞株をセンダイウイルスにより樹立後、テトラサイクリン添加依存的にc-MYCの発現をon/offさせる確認実験を行ったところ、未熟な巨核球増殖過程のみc-MYCが促進し、成熟過程においてはc-MYCの急激な発現低下が必須であることを確認しました。産生されたヒトiPS細胞由来血小板は、マウス生体内での傷害血管壁で血栓形成に寄与することも確認できました。
以上の結果から、遺伝子操作を用いて生体内で機能を有するヒトiPS細胞由来血小板を大量に且つ安定して産生する可能性を示唆することができました。血小板は無核であり、輸血時に放射線照射や輸血フィルターを通すことで、ガン化の原因となる有核細胞を排除することが可能です。将来的な輸血医療への貢献が期待されます。
