変異型ASXL1は骨髄異形成症候群発症を誘導する
変異型ASXL1は骨髄異形成症候群発症を誘導する
最近のシークエンス技術の発達とSNPアレイにより、造血器腫瘍を含む多くの腫瘍で今までに知られていなかった多くの遺伝子の変異が同定された。我々のグループは、造血器腫瘍患者細胞から同定した変異遺伝子を効率の良いレトロウイルスベクターによってマウス骨髄細胞に導入し、これらマウス骨髄細胞を照射したマウスに移植することによって造血器腫瘍のモデルマウスを作製し解析してきた。
骨髄異形成症候群(MDS:myelodysplastic syndromes)は、造血細胞形態異常、無効造血、アポトーシス亢進を特徴とする造血器疾患であり、白血病に移行しやすいという特徴も有する。最近ではDNAメチル化阻害剤がMDS患者の半数程度に効果があるということが大きな注目を集めている。このことはMDSがエピジェネティクスの異常によって起こる疾患であることを示唆している。高速シークエンスの発達は、MDSにおけるTET2、DNMT3a、EZH2、ASXL1などエピジェネティクスに関与する遺伝子の変異の存在を明らかにした。我々はこれらの遺伝子変異とMDS発症の関係を解析するために骨髄移植モデルを利用して研究を行なっている。本研究では変異型ASXL1を導入したマウス骨髄細胞を移植したマウスが典型的なMDSを発症し、一部のマウスは白血病に移行することが明らかになった。 この結果はASXL1遺伝子の変異がドライバーミューテーションとしてMDS発症に深く関わっていることを示している。さらに我々はMDS発症の分子機序を調べ、変異型ASXL1がポリコーム複合体PRC1の機能を抑制することにより遺伝子発現に異常を来すことがMDSの発症原因であることを明らかにした。通常ASXL1はPRC1機能を助けて、ヒストンH3のK4のメチル化を介してがん遺伝子などの発現を抑制している(図1)が、変異型ASXL1によりその機能が阻害され、遺伝子発現の脱抑制が引き起こされることがMDS発症につながることが判明した。
この結果はASXL1遺伝子の変異がドライバーミューテーションとしてMDS発症に深く関わっていることを示している。さらに我々はMDS発症の分子機序を調べ、変異型ASXL1がポリコーム複合体PRC1の機能を抑制することにより遺伝子発現に異常を来すことがMDSの発症原因であることを明らかにした。通常ASXL1はPRC1機能を助けて、ヒストンH3のK4のメチル化を介してがん遺伝子などの発現を抑制している(図1)が、変異型ASXL1によりその機能が阻害され、遺伝子発現の脱抑制が引き起こされることがMDS発症につながることが判明した。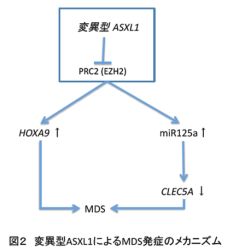 この時、脱抑制される遺伝子はHoxA9および造血器腫瘍発症に関与することが知られているマイクロRNA、miR125aなどである。さらに我々はmiR125aの新たな標的遺伝子として好中球分化に必要なClec5a/MDL1という遺伝子を同定した(図2)。この結果は変異型ASXL1によって脱抑制されたHoxA9とmiR125aがMDSの発症に深く関与していること、またmiR125aがClec5a/MDL1の発現を抑制することによって造血細胞分化が障害される可能性を示唆している。
この時、脱抑制される遺伝子はHoxA9および造血器腫瘍発症に関与することが知られているマイクロRNA、miR125aなどである。さらに我々はmiR125aの新たな標的遺伝子として好中球分化に必要なClec5a/MDL1という遺伝子を同定した(図2)。この結果は変異型ASXL1によって脱抑制されたHoxA9とmiR125aがMDSの発症に深く関与していること、またmiR125aがClec5a/MDL1の発現を抑制することによって造血細胞分化が障害される可能性を示唆している。
このマウスMDSモデルはMDS発症および白血病移行の分子機構の解析に有用である。さらに、このMDSモデルを含む我々が樹立してきた様々なMDSモデルを利用すれば、DNAメチル化阻害剤、マルチキナーゼ阻害剤、HDAC阻害剤、レナリドミドなどの薬剤を投与することによって、それぞれの薬剤の適応および作用機序を明らかにすることが期待できる。
JCIリンク
