過剰なアレルギー反応を抑える生体内の仕組み -レセプターLMIR3 と脂質セラミドの結合が肥満細胞の活性化を抑制する-
過剰なアレルギー反応を抑える生体内の仕組み -レセプターLMIR3 と脂質セラミドの結合が肥満細胞の活性化を抑制する-
アレルギー疾患を解明するためには、アレルギーの発症と抑制の仕組みを理解する必要があります。生体は、ダニや花粉などの抗原に暴露されると、抗原を認識するIgEを産生します。そのIgEと抗原が肥満細胞の高親和性IgEレセプター(FcεRI)を刺激すると、肥満細胞は活性化し、ヒスタミンなどの化学伝達物質を放出して、アレルギー反応を引き起こします。一方、アレルギーを発症させる肥満細胞の活性化を抑える仕組みについては謎のままでした。 免疫レセプターのなかには、細胞外領域の構造が似ている一方、細胞内領域の構造が異なるために、互いに正反対の機能を持つ免疫レセプター群が存在します。このようなレセプター群は、ペア型免疫レセプターとよばれています。一方は免疫細胞を活性化するレセプターであり、他方はその活性化を抑えるレセプター(抑制型レセプター)となります。Leucocyte mono-immunoglobulin-like receptor (LMIR) (別名:CD300)ファミリー分子は、ペア型免疫レセプターです。マウスでは少なくとも8種類のLMIRが存在し、LMIR3/CD300fは細胞内領域にimmunoreceptor tyrosine-based inhibitory or switch motif (ITIM or ITSM)と呼ばれるアミノ酸配列をもつ抑制型レセプターです。この配列内に存在するチロシン残基がリン酸化されると、チロシンフォスファターゼのSHP-1やSHP-2が結合して、細胞内の活性化シグナルを抑制します。一方、LMIR3の生理的なリガンドがわからないためにLMIR3の生体内における役割は不明でした。
本研究によりLMIR3が肥満細胞の過剰な活性化を抑える重要なレセプターであることを明らかにしました。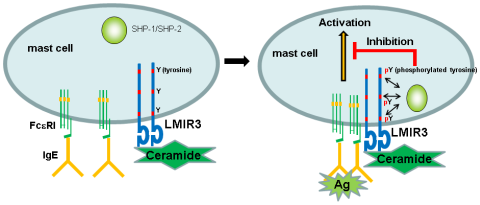 実際、LMIR3ノックアウトマウスでは、IgEと肥満細胞の関与するアレルギー疾患(アナフィラキシー・喘息・皮膚炎)の症状が悪化することを示しました。次に、LMIR3のリガンドを同定するために、LMIR3の細胞外領域を利用して、物理的な結合アッセイと機能的なレポーターアッセイを行いました。さまざまな蛋白や脂質をスクリーニングした結果、LMIR3のリガンドとして細胞外脂質のセラミドを同定しました。セラミドはマウスの皮膚上皮に豊富なことが知られていますが、肥満細胞が局在する皮膚真皮にも存在することを明らかにし、さらに、肥満細胞に発現するLMIR3とセラミドの結合が肥満細胞の活性化を抑え、アレルギー反応を減弱させることを証明しました。また、(1) 肥満細胞のLMIR3とセラミドが結合するだけではLMIR3のITIMやITSMはリン酸化されないこと、(2) IgEと抗原の刺激によりFcRIシグナルが活性化されるときにLMIR3のITIMとITSMも強くリン酸化されて肥満細胞の過剰な活性化が抑えられることが判明しました。細胞外脂質セラミドが皮膚上皮のバリアとして働くことは知られていますが、肥満細胞のLMIR3に結合するセラミドが抗アレルギー脂質として機能することが初めて明らかになりました。本研究は、順天堂大学医学部の奥村康教授、理化学研究所発生再生科学総合研究センターの清成寛研究員らの協力を得て行いました。
実際、LMIR3ノックアウトマウスでは、IgEと肥満細胞の関与するアレルギー疾患(アナフィラキシー・喘息・皮膚炎)の症状が悪化することを示しました。次に、LMIR3のリガンドを同定するために、LMIR3の細胞外領域を利用して、物理的な結合アッセイと機能的なレポーターアッセイを行いました。さまざまな蛋白や脂質をスクリーニングした結果、LMIR3のリガンドとして細胞外脂質のセラミドを同定しました。セラミドはマウスの皮膚上皮に豊富なことが知られていますが、肥満細胞が局在する皮膚真皮にも存在することを明らかにし、さらに、肥満細胞に発現するLMIR3とセラミドの結合が肥満細胞の活性化を抑え、アレルギー反応を減弱させることを証明しました。また、(1) 肥満細胞のLMIR3とセラミドが結合するだけではLMIR3のITIMやITSMはリン酸化されないこと、(2) IgEと抗原の刺激によりFcRIシグナルが活性化されるときにLMIR3のITIMとITSMも強くリン酸化されて肥満細胞の過剰な活性化が抑えられることが判明しました。細胞外脂質セラミドが皮膚上皮のバリアとして働くことは知られていますが、肥満細胞のLMIR3に結合するセラミドが抗アレルギー脂質として機能することが初めて明らかになりました。本研究は、順天堂大学医学部の奥村康教授、理化学研究所発生再生科学総合研究センターの清成寛研究員らの協力を得て行いました。
本研究結果を利用することにより、アレルギー疾患に対する新しい予防法や治療法の開発が期待されます。
