自己免疫疾患発症を抑制する胸腺上皮細胞に分化する前駆細胞の同定
自己免疫疾患発症を抑制する胸腺上皮細胞に分化する前駆細胞の同定
自己免疫疾患の発症抑制に必要な胸腺髄質上皮細胞の前駆細胞とその分化を制御する分子機構を解明しました。本研究はJournal of Experimental Medicine誌掲載号の表紙に選ばれています。
私たちの体にウィルスや細菌などの病原体が入ってくると、それらを排除しようと免疫機構が働きます。免疫機構において重要なのは、自分と自分でないもの(非自己)との識別です。この識別が破綻すると、自分の組織に対して免疫反応が起こり、自己免疫疾患を発症します。
自己-非自己を識別する細胞の一つがT細胞です。T細胞は胸腺で分化します。胸腺内では自己組織を認識する未熟なT細胞も出来ますが、それらは分化途中で除かれます。そのため、成熟したT細胞は末梢で自己組織に対して免疫反応を起こしません。この現象を自己免疫寛容と呼び、この機構により自己免疫疾患の発症は未然に防がれています。最近、自己免疫寛容の成立に、胸腺の髄質を構成する上皮細胞(胸腺髄質上皮細胞)が必須であることが分かってきました。
胸腺髄質上皮細胞は転写因子Aire を介して、通常は組織特異的に発現するタンパク質を異所的に発現し、抗原提示します。その組織特異的な抗原を認識するT細胞は細胞死を起こし除去されることにより、免疫寛容が成立します。私たちの研究グループはこれまでに、胸腺髄質上皮細胞の分化には、TNF受容体スーパーファミリーに属するRANKのシグナルが必須であることを明らかにしてきました。しかしこれまで、RANKシグナルを受け取ってAire陽性髄質上皮細胞に分化する前駆細胞は同定されていませんでした。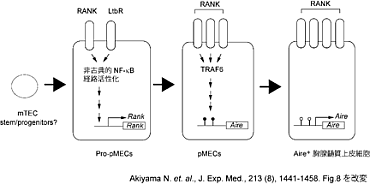 私たちは、RANKの発現をモニター出来るレポーターマウスを用い、胎仔胸腺のRANKシグナル遮断時にRANKを発現する上皮細胞を同定しました。これをpMECs (precursors of Aire-expressing medullary thymic epithelial cells)と名付け、pMECsがAire陽性髄質上皮細胞に分化することを移植実験で明らかにしました。またpMECsから分化した髄質上皮細胞は正常に機能し、自己免疫疾患の発症を抑制しました。加えてpMECsからAire陽性髄質上皮細胞への分化には、RANKシグナル下流で活性化するタンパク質TRAF6が必要であることが分かりました。さらに様々なノックアウトマウスの解析から、pMECsよりも早い分化段階の前駆細胞(pro-pMECs)も同時に発見しました。pro-pMECsからpMECsへの分化には、TNF受容体スーパーファミリーに属するLtbRとRANKの二つのシグナルが引き金となり、これらの下流で働く非古典的NF-κB経路の活性化が必要十分であることを示しました。
私たちは、RANKの発現をモニター出来るレポーターマウスを用い、胎仔胸腺のRANKシグナル遮断時にRANKを発現する上皮細胞を同定しました。これをpMECs (precursors of Aire-expressing medullary thymic epithelial cells)と名付け、pMECsがAire陽性髄質上皮細胞に分化することを移植実験で明らかにしました。またpMECsから分化した髄質上皮細胞は正常に機能し、自己免疫疾患の発症を抑制しました。加えてpMECsからAire陽性髄質上皮細胞への分化には、RANKシグナル下流で活性化するタンパク質TRAF6が必要であることが分かりました。さらに様々なノックアウトマウスの解析から、pMECsよりも早い分化段階の前駆細胞(pro-pMECs)も同時に発見しました。pro-pMECsからpMECsへの分化には、TNF受容体スーパーファミリーに属するLtbRとRANKの二つのシグナルが引き金となり、これらの下流で働く非古典的NF-κB経路の活性化が必要十分であることを示しました。
本研究の結果から、RANKシグナル下流で二つの異なるシグナル経路が順次に働き、胸腺髄質上皮細胞の分化段階を制御することが明らかになりました。本研究の成果は、自己免疫疾患の発症を回避する機構の解明に貢献します。未だ謎な部分が多い胸腺上皮細胞の分化制御機構の解明は、自己免疫疾患の新しい治療法を開発する研究へと展開することが期待されます。
