発表論文
- 2022 | 2021 | 2020 | 2019 | 2018 | 2017 | 2016 | 2015 | 2014
- 2013 | 2012 | 2011 | 2010 | 2009 | 2008 | 2007 | 2006 | 2005 | 2004
- 2003 | 2002 | 2001 | 2000 | 1999 | 1998 | 1997 | 1996 | 1995 | 1994
2022
1. Ishii T, Murakami Y, Narita T, Nunokawa H, Miyake K, Nagase T, Yamashita N. Myeloid differentiation protein-2 has a protective role in house dust mite-mediated asthmatic characteristics with the proinflammatory regulation of airway epithelial cells and dendritic cells. Clin Exp Allergy 2022, 52(1):149-161.
2021
1. Liu K, Sato R, Shibata T, Hiranuma R, Reuter T, Fukui R, Zhang Y, Ichinohe T, Ozawa M, Yoshida N, Latz E, Miyake K. Skewed endosomal RNA responses from TLR7 to TLR3 in RNase T2-deficient macrophages. Int Immunol. 2021, 33(9):479-490.
2. Gavin AL, Huang D, Blane TR, Thinnes TC, Murakami Y, Fukui R, Miyake K, Nemazee D. Cleavage of DNA and RNA by PLD3 and PLD4 limits autoinflammatory triggering by multiple sensors. Nat Commun. 2021, 12(1):5874.
3. Murakami Y, Fukui R, Tanaka R, Motoi Y, Kanno A, Sato R, Yamaguchi K, Amano H, Furukawa Y, Suzuki H, Suzuki Y, Tamura N, Yamashita N, Miyake K. Anti-TLR7 Antibody Protects Against Lupus Nephritis in NZBWF1 Mice by Targeting B Cells and Patrolling Monocytes. Front Immunol. 2021, 12:777197.
4. Miyake K, Saitoh SI, Fukui R, Shibata T, Sato R, Murakami Y. ADynamic control of nucleic-acid-sensing Toll-like receptors by the endosomal compartment. Ing Immunol. 2021, 25;33(12):835-840. (Review)
2020
1. Ishiguro N, Moriyama M, Furusho K, Furukawa S, Shibata T, Murakami Y, Chinju A, Haque ASMR, Gion Y, Ohta M, Maehara T, Tanaka A, Yamauchi M, Sakamoto M, Mochizuki K, Ono Y, Hayashida JN, Sato Y, Kiyoshima T, Yamamoto H, Miyake K, Nakamura S. Activated M2 Macrophages Contribute to the Pathogenesis of IgG4-Related Disease via Toll-like Receptor 7/Interleukin-33 Signaling. Arthritis Rheumatol. 2020, 72(1):166-178.
2. Tsukamoto Y, Tamura T, Maeda Y, Miyake K, Ato M. N6-methylated adenine on the target sites of mamA from Mycobacterium bovis BCG enhances macrophage activation by CpG DNA in mice. Tuberculosis (Edinb) 2020, 121:101890
3. Nakashima A, Tomono S, Yamazaki T, Inui M, Morita N, Ichimonji I, Takagi H, Nagaoka F, Matsumoto M, Ito Y, Yanagishita T, Miyake K, Watanabe D, Akashi-Takamura S. Phospholipase A2 from bee venom increases poly(I:C)-induced activation in human keratinocytes. Int. Immunol. 2020, 32(6):371-383.
4. Sakaguchi T, Okumura R, Ono C, Okuzaki D, Kawai T, Okochi Y, Tanimura N, Murakami M, Kayama H, Umemoto E, Kioka H, Ohtani T, Sakata Y, Miyake K, Okamura Y, Baba Y, Takeda K. TRPM5 Negatively Regulates Calcium-Dependent Responses in Lipopolysaccharide-Stimulated B Lymphocytes. Cell Rep. 2020, 31(10):107755.
5. Sato R, Reuter T, Hiranuma R, Shibata T, Fukui R, Motoi Y, Murakami Y, Tsukamoto H, Yamazaki S, Liu K, Saitoh SI, Latz E, Miyake K. The impact of cell maturation and tissue microenvironments on the expression of endosomal Toll-like receptors in monocytes and macrophages. Int. Immunol. 2020, 32(12):785-798.
2019
1. Furusho K, Shibata T, Sato R, Fukui R, Motoi Y, Zhang Y, Saitoh SI, Ichinohe T, Moriyama M, Nakamura S, Miyake K. Cytidine deaminase enables Toll-like receptor 8 activation by cytidine or its analogs. Int. Immunol. 2019, 31(3):167-173.
2. Imanishi T, Unno M, Kobayashi W, Yoneda N, Matsuda S, Ikeda K, Hoshii T, Hirao A, Miyake K, Barber GN, Arita M, Ishii KJ, Akira S, Saito T. Reciprocal regulation of STING and TCR signaling by mTORC1 for T-cell activation and function. Life Sci Alliance. 2019, 2(1). pii: e201800282
3. Orimo T, Sasaki I, Hemmi H, Ozasa T, Fukuda-Ohta Y, Ohta T, Morinaka M, Kitauchi M, Yamaguchi T, Sato Y, Tanaka T, Hoshino K, Katayama KI, Fukuda S, Miyake K, Yamamoto M, Satoh T, Furukawa K, Kuroda E, Ishii KJ, Takeda K, Kaisho T. Cholera toxin B induces interleukine-1β production from resident peritoneal macrophages through pyrin as well as NLRP3 inflammasome. Int. Immunol. 2019, 31(10):657-668.
4. Saitoh SI, Saitoh YM, Kontani K, Sato K, Miyake K. ADP-ribosylation factor-like 8b is required for the development of mouse models of systemic lupus erythematosus. Int. Immunol. 2019, 31(4):225-237.
5. Miyake K, Saitoh SI, Sato R, Shibata T, Fukui R, Murakami Y. Endolysosomal compartments as platforms for orchestrating innate immune and metabolic sensors. J Leukoc Biol. 2019, 106(4):853-862.
2018
1. Kusumoto Y, Okuyama H, Shibata T, Konno K, Takemoto Y, Maekawa D, Kononaga T, Ishii T, Akashi-Takamura S, Saitoh SI, Ikebuchi R, Moriya T, Ueda M, Miyake K, Ono S, Tomura M. Cell Immunol. 2018, 324:33-41
2. Mutoh H, Kato M, Akita T, Shibata T, Wakamoto H, Ikeda H, Kitaura H, Aoto K, Nakashima M, Wang T, Ohba C, Miyatake S, Miyake N, Kakita A, Miyake K, Fukuda A, Matsumoto N, Saitsu H. Biallelic Variants in CNPY3, Encoding an Endoplasmic Reticulum Chaperone, Cause Early-Onset Epileptic Encephalopathy. Am J Hum Genet. 2018, pii: S0002-9297(18)30004-1.
3. Maruzuru Y, Ichinohe T, Sato R, Miyake K, Okano T, Suzuki T, Koshiba T, Koyanagi N, Tsuda S, Watanabe M, Arii J, Kato A, Kawaguchi Y. Herpes Simplex Virus 1 VP22 Inhibits AIM2-Dependent Inflammasome Activation to Enable Efficient Viral Replication. Cell Host Microbe. 2018, 23(2):254-265.e7
4. Miyake K, Shibata T, Ohto U, Shimizu T, Saitoh SI, Fukui R, Murakami Y. Mechanisms controlling nucleic acid-sensing Toll-like receptors. Int. Immunol.2018, 30(2):43-51
5. Ohto U, Ishida H, Shibata T, Sato R, Miyake K, Shimizu T. Toll-like Receptor 9 Contains Two DNA Binding Sites that Function Cooperatively to Promote Receptor Dimerization and Activation. Immunity 2018, 48(4):649-658.e4
6. Pelka K, Bertheloot D, Reimer E, Phulphagar K, Schmidt SV, Christ A, Stahl R, Watson N, Miyake K, Hacohen N, Haas A, Brinkmann MM, Marshak-Rothstein A, Meissner F, Latz E. The Chaperone UNC93B1 Regulates Toll-like Receptor Stability Independently of Endosomal TLR Transport. Immunity 2017, 48(5):911-922.e7
7. Ishida H, Ohto U, Shibata T, Miyake K, Shimizu T. Structural basis for species-specific activation of mouse Toll-like receptor 9. FEBS Lett. 2018, 592(15):2636-2646
8. Fukui R, Murakami Y, Miyake K. New application of anti-TLR monoclonal antibodies: detection, inhibition and protection. Inflamm Regen. 2018, 38:11.
9. Fukui R, Yamamoto C, Matsumoto F, Onji M, Shibata T, Murakami Y, Kanno A, Hayashi T, Tanimura N, Yoshida N, Miyake K. Cleavage of Toll-Like Receptor 9 Ectodomain Is Required for In Vivo Responses to Single Strand DNA. Front Immunol. 2018, 9:1491.
10. Sato R, Kato A, Chimura T, Saitoh SI, Shibata T, Murakami Y, Fukui R, Liu K, Zhang Y, Arii J, Sun-Wada GH, Wada Y, Ikenoue T, Barber GN, Manabe T, Kawaguchi Y, Miyake K. Combating herpesvirus encephalitis by potentiating a TLR3-mTORC2 axis. Nat. Immunol. 2018, 19(10):1071-1082
11. Zhang Z, Ohto U, Shibata T, Taoka M, Yamauchi Y, Sato R, Shukla NM, David SA, Isobe T, Miyake K, Shimizu T. Structural Analyses of Toll-like Receptor 7 Reveal Detailed RNA Sequence Specificity and Recognition Mechanism of Agonistic Ligands. Cell Rep. 2018, 25(12):3371-3381.e5
2017
1. Miyake K, Shibata T, Ohto U, Shimizu T. Emerging roles of the processing of nucleic acids and Toll-like receptors in innate immune responses to nucleic acids. J Leukoc Biol. 2017, 101:135-142
2. Morita N, Yamai I, Takahashi K, Kusumoto Y, Shibata T, Kobayashi T, Nonaka MI, Ichimonji I, Takagi H, Miyake K, Takamura SA. C4b binding protein negatively regulates TLR1/2 response. Innate Immun. 2017, 23:11-19
3. Furukawa S, Moriyama M, Miyake K, Nakashima H, Tanaka A, Maehara T, Iizuka-Koga M, Tsuboi H, Hayashida JN, Ishiguro N, Yamauchi M, Sumida T, Nakamura S. Interleukin-33 produced by M2 macrophages and other immune cells contributes to Th2 immune reaction of IgG4-related disease. Sci. Rep. 2017, 7:42413
4. Pohar J, Yamamoto C, Fukui R, Cajnko MM, Miyake K, Jerala R, Benčina M. Selectivity of Human TLR9 for Double CpG Motifs and Implications for the Recognition of Genomic DNA. J. Immunol.2017, 198:2093-2104
5. Murakami Y, Fukui R, Motoi Y, Shibata T, Saitoh SI, Sato R, Miyake K. The protective effect of the anti-Toll-like receptor 9 antibody against acute cytokine storm caused by immunostimulatory DNA. Sci. Rep. 2017, 7:44042
6. Morita N, Yamazaki T, Murakami Y, Fukui R, Yamai I, Ichimonji I, Nakashima A, Nagaoka F, Takagi H, Miyake K, Akashi-Takamura S. C4b-binding protein negatively regulates TLR4/MD-2 response but not TLR3 response. FEBS Lett. 2017, 591:1732-1741
7. Oka M, Hashimoto K, Yamaguchi Y, Saitoh SI, Sugiura Y, Motoi Y, Honda K, Kikko Y, Ohata S, Suematsu M, Miura M, Miyake K, Katada T, Kontani K. Arl8b is required for lysosomal degradation of maternal proteins in the visceral yolk sac endoderm of mouse embryos. Cell Sci. 2017, 130:3568-3577
8. Iijima J, Kobayashi S, Kitazume S, Kizuka Y, Fujinawa R, Korekane H, Shibata T, Saitoh SI, Akashi-Takamura S, Miyake K, Miyoshi E, Taniguchi N. Core fucose is critical for CD14-dependent Toll-like receptor 4 signaling. Glycobiology 2017, 27:1006-1015
9. Sato R, Shibata T, Tanaka Y, Kato C, Yamaguchi K, Furukawa Y, Shimizu E, Yamaguchi R, Imoto S, Miyano S, Miyake K. Requirement of glycosylation machinery in TLR responses revealed by CRISPR/Cas9 screening. Int. Immunol. 2017, 29:347-355
10. Saitoh SI, Abe F, Kanno A, Tanimura N, Mori Saitoh Y, Fukui R, Shibata T, Sato K, Ichinohe T, Hayashi M, Kubota K, Kozuka-Hata H, Oyama M, Kikko Y, Katada T, Kontani K, Miyake K. TLR7 mediated viral recognition results in focal type I interferon secretion by dendritic cells. Nat. Commun. 2017, 8:Article Number 1592
2016
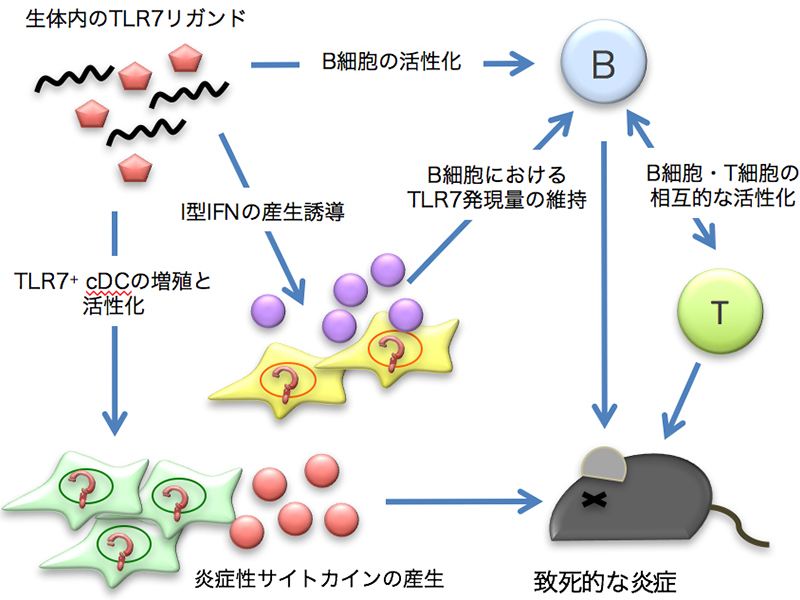
概要:Unc93b1D34A/D34Aマウス (D34Aマウス)はTLR7とTLR9の応答バランスが破綻し、TLR7が過剰応答することによって致死的な自然炎症が誘導されます。D34Aマウスの表現型に影響を与える因子を調べるため、各種サイトカインやインターフェロンの関与を調べたところ、I型インターフェロン受容体 (IFNAR1)をノックアウトしたD34Aマウスでは表現型が緩和されました。 |
2. Pelka K, Shibata T, Miyake K, Latz E. Nucleic acid-sensing TLRs and autoimmunity: novel insights from structural and cell biology. Immunol. Rev. 2016, 269:60-75
3. Watanabe Y, Nagai Y, Honda H, Okamoto N, Yamamoto S, Hamashima T, Ishii Y, Tanaka M, Suganami T, Sasahara M, Miyake K, Takatsu K. Isoliquiritigenin Attenuates Adipose Tissue Inflammation in vitro and Adipose Tissue Fibrosis through Inhibition of Innate Immune Responses in Mice. Sci. Rep. 2016, 6:23097
4. Tanji H, Ohto U, Motoi Y, Shibata T, Miyake K, Shimizu T. Autoinhibition and relief mechanism by the proteolytic processing of Toll-like receptor 8. PNAS 2016, 113:3012-3017
5. Shibata T, Ohto U, Nomura S, Kibata K, Motoi Y, Zhang Y, Murakami Y, Fukui R, Ishimoto T, Sano S, Ito T, Shimizu T, Miyake K. Guanosine and its modified derivatives are endogenous ligands for TLR7. Int. Immunol. 2016, 28:211-222
6. Honda S, Sato K, Totsuka N, Fujiyama S, Fujimoto M, Miyake K, Nakahashi-Oda C, Tahara-Hanaoka S, Shibuya K, Shibuya A. Marginal zone B cells exacerbate endotoxic shock via interleukin-6 secretion induced by Fcα/μR-coupled TLR4 signalling. Nat. Commun. 2016, 7:11498
7. Maekawa S, Ohto U, Shibata T, Miyake K, Shimizu T. Crystal structure of NOD2 and its implications in human disease. Nat. commun. 2016, 7:11813
8. Thomas Jennings R, Odkhuu E, Nakashima A, Morita N, Kobayashi T, Yamai I, Tanaka M, Suganami T, Haga S, Ozaki M, Watanabe Y, Nagai Y, Takatsu K, Kikuchi-Ueda T, Ichimonji I, Ogawa Y, Takagi H, Yamazaki T, Miyake K, Akashi-Takamura S. Inflammatory responses increase secretion of MD-1 protein. Int. Immunol. 2016, 28:503-512
9. Zhang Z, Ohto U, Shibata T, Krayukhina E, Taoka M, Yamauchi Y, Tanji H, Isobe T, Uchiyama S, Miyake K, Shimizu T. Structural Analysis Reveals that Toll-like Receptor 7 Is a Dual Receptor for Guanosine and Single-Stranded RNA. Immunity 2016, 45:737-748
2015
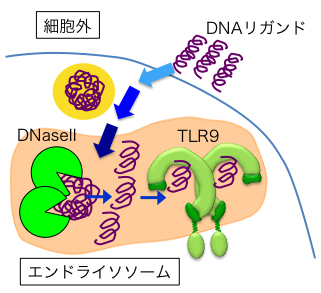
概要:Toll-like receptor9 (TLR9)は一本鎖DNAを認識して、免疫応答を惹起する自然免疫系の担当分子です。TLR9が認識するDNAは細菌やウイルスなどの病原体に由来するものの他に、宿主に由来するものも存在します。したがって、TLR9のDNA認識メカニズムの解明は感染症や自己免疫疾患などを理解する上で、重要な研究課題であると考えられています。 |
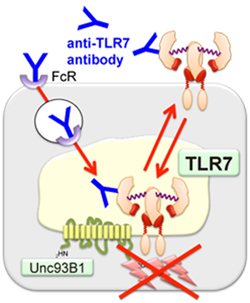
概要:Toll like receptor 7(TLR7)は外来微生物由来の一本鎖RNAを認識することで生体防御に関わっています。しかし、自己に由来するRNAにも応答し炎症を引き起こす可能性が指摘されています。実際に、全身性エリテマトーデスモデルマウスにおいて、核酸に対する自己抗体の産生にTLR7が関わっていることが報告されています。また当研究室では、TLRの局在を制御する分子Unc93B1のノックインマウス(Unc93b1D34A/D34Aマウス)がTLR7の自発的な過剰応答によって、脾腫や肝炎、血小板減少症などの病態を引き起こすことを見出しています。そのため、TLR7の応答は厳密に制御される必要があります。自己核酸はヌクレアーゼによって速やかに分解されるが、病原体由来の核酸は菌体膜やウイルス粒子などによって分解を免れ、エンドリソソームにまで到達します。したがって、TLR7は細胞内のエンドリソソームでのみ核酸を認識することで、自己核酸への応答を抑制していると考えられてきました。 |
3. Tanji H, Ohto U, Shibata T, Taoka M, Yamauchi Y, Isobe T, Miyake K, Shimizu T. Toll-like receptor 8 senses degradation products of single-stranded RNA. Nat Struct Mol Biol. 2015, 22:109-115
4. Nündel K, Green NM, Shaffer AL, Moody KL, Busto P, Eilat D, Miyake K, Oropallo MA, Cancro MP, Marshak-Rothstein A. Cell-intrinsic expression of TLR9 in autoreactive B cells constrains BCR/TLR7-dependent responses. J. Immunol. 2015, 194:2504-2512
5. Ohto U, Shibata T, Tanji H, Ishida H, Krayukhina E, Uchiyama S, Miyake K, Shimizu T. Structural basis of CpG and inhibitory DNA recognition by Toll-like receptor 9. Nature 2015, 520:702-705
6. Kimura T, Endo S, Inui M, Saitoh S, Miyake K, Takai T. Endoplasmic Protein Nogo-B (RTN4-B) Interacts with GRAMD4 and Regulates TLR9-Mediated Innate Immune Responses. J. Immunol. 2015, 194:5426-5436
7. Pohar J, Lainšček D, Fukui R, Yamamoto C, Miyake K, Jerala R, Benčina M. Species-Specific Minimal Sequence Motif for Oligodeoxyribonucleotides Activating Mouse TLR9. J. Immunol. 2015, 195:4396-4405
2014
1. Tanimura N, Saitoh SI, Ohto U, Akashi-Takamura S, Fujimoto Y, Fukase K, Shimizu T, Miyake K. The attenuated inflammation of MPL is due to the lack of CD14-dependent tight dimerization of the TLR4/MD2 complex at the plasma membrane. Int. Immunol. 2014, 26:307-314
2. Murakami Y, Fukui R, Motoi Y, Kanno A, Shibata T, Tanimura N, Saitoh S, Miyake K. Roles of the cleaved N-terminal TLR3 fragment and cell surface TLR3 in double-stranded RNA sensing. J. Immunol. 2014, 193:5208-5217
3. Huh JW, Shibata T, Hwang M, Kwon EH, Jang MS, Fukui R, Kanno A, Jung DJ, Jang MH, Miyake K, Kim YM. UNC93B1 is essential for the plasma membrane localization and signaling of Toll-like receptor 5. Proc Natl Acad Sci U S A. 2014, 111:7072-7077
4. Motoi Y, Shibata T, Takahashi K, Kanno A, Murakami Y, Li X, Kasahara T, Miyake K. Lipopeptides are signaled by Toll-like receptor 1, 2 and 6 in endolysosomes. Int. Immunol. 2014, 26:563-573
5. Miyake K, Kaisho T. Homeostatic inflammation in innate immunity. Curr Opin Immunol. 2014, 30:85-90
6. Latz E, Miyake K. Editorial overview: Special section: effects of endogenous immune stimulants: from a defence system against infection to a homeostatic mechanism linking metabolism with inflammation. Curr Opin Immunol. 2014, 30:viii-ix
7. Li X, Saitoh SI, Shibata T, Tanimura N, Fukui R, Miyake K. Mucolipin 1 positively regulates TLR7 responses in dendritic cells by facilitating RNA transportation to lysosomes. Int. Immunol. 2014, doi: 10.1093/intimm/dxu086 [Epub ahead of print]