| 発表のポイント |
|---|
|
発表内容
東京大学国際高等研究所 新世代感染症センター 河岡義裕 機構長らの研究グループは、新型コロナウイルス変異株・オミクロン株EG.5.1系統の、ハムスターモデルでの増殖性や飛沫伝播のしやすさ、並びに、抗原性を調べました。新型コロナウイルス変異株・オミクロン株の流行は、現在も続いています。2023年12月現在、日本を含む多くの国々で、XBB系統から派生したEG.5.1系統(注)が流行の主流となっています。しかし、EG.5.1系統の増殖能や、飛沫伝播性については明らかになっていませんでした。
臨床検体から分離されたEG.5.1系統の株(EG.5.1株)の増殖性および病原性をデルタ株やXBB.1.5株と比較しました。EG.5.1株およびXBB.1.5株を感染させたハムスターは体重減少を示しませんでした。一方、デルタ株を感染させたハムスターは全ての個体で体重が減少していました。ハムスターの肺や鼻におけるEG.5.1株の増殖能は、デルタ株と比べると低いものの、XBB.1.5株と同程度であることが明らかとなりました(図1)。
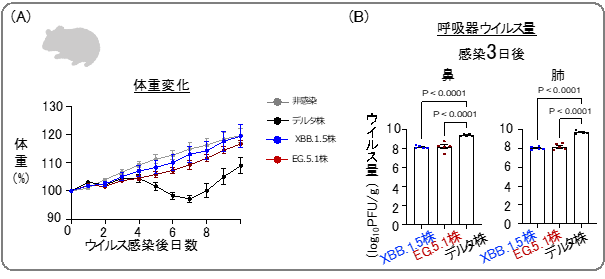
新型コロナウイルス・オミクロン株をハムスターの鼻腔内に接種した。
(A)接種後、非感染動物(対照群)と感染動物の体重を毎日測定した。EG.5.1株ならびXBB.1.5株に感染群では全ての株で体重が増加した。
(B)感染後3日目の鼻と肺におけるウイルス量を測定した。EG.5.1株はXBB.1.5株と同程度の増殖を示した。
続いて、ワクチン接種後にオミクロン株に感染(ブレイクスルー感染)した方の血漿を用いて、EG.5.1株に対する中和活性を検証しました。その結果、ブレイクスルー感染者の血漿はEG.5.1株に対して中和活性を示すものの、その活性はパンデミック初期株やXBB.1.5株に対する活性よりも低いことが明らかになりました。このことはEG.5.1株がXBB.1.5株よりも体内で産生される抗体に対して抵抗性を示すことを示唆します。
本研究を通して得られた成果は、オミクロン株各系統のリスク評価など、行政機関が今後の新型コロナウイルス感染症対策計画を策定・実施する上で、重要な情報となります。
本研究は12月15日、米国科学誌「Cell Reports」(オンライン版)に公表されました。
なお、ヒトで世界的に流行したBA.2系統がハムスターでは飛沫伝播を起こさないため、「ハムスターにおいてEG.5.1系統の方が伝播しやすい」という今回の結果が必ずしもヒトに当てはまるわけではありません。今後もオミクロン系統の飛沫伝播に関する継続的な検証が待たれます。
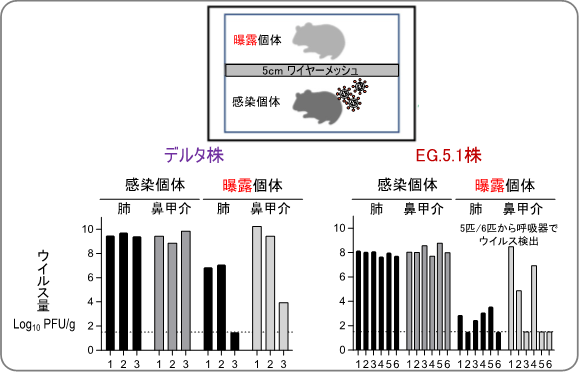
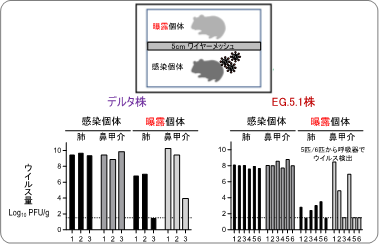
ハムスターに、デルタ株あるいはEG.5.1株を播種した(感染個体)。一日後に、非感染個体(曝露個体)を入れたケージを5 cm距離を離して隣接させ、飛沫による感染伝播が起こるか調べた(上図)。デルタ株では、曝露3日後3ペア中3ペアで伝播しており、EG.5.1株では、曝露3日後に6ペア中5ペアで伝播していた(下図)。
発表者
東京大学国際高等研究所 新世代感染症センター 機構長東京大学医科学研究所 ウイルス感染部門 特任教授
河岡 義裕
<国立国際医療研究センター 研究所 国際ウイルス感染症研究センター長>
論文情報
〈雑誌〉Cell Reports(12月15日オンライン版)〈題名〉Characterization of a SARS-CoV-2 EG.5.1 clinical isolate in vitro and in vivo
〈著者〉Ryuta Uraki*, Maki Kiso*, Kiyoko Iwatsuki-Horimoto*, Seiya Yamayoshi*, Mutsumi Ito, Shiho Chiba, Yuko Sakai-Tagawa, Masaki Imai, Yukie Kashima, Michiko Koga, Noriko Fuwa, Nobumasa Okumura, Masayuki Hojo, Noriko Iwamoto, Hideaki Kato, Hideaki Nakajima, Norio Ohmagari, Hiroshi Yotsuyanagi, Yutaka Suzuki, and Yoshihiro Kawaoka¶
*:筆頭著者 ¶:責任著者
〈DOI〉10.1016/j.celrep.2023.113580
〈URL〉https://doi.org/10.1016/j.celrep.2023.113580
研究助成
本研究は、東京大学国際高等研究所 新世代感染症センター、東京大学医科学研究所、国立国際医療研究センター、東京大学大学院新領域創成科学研究科、横浜市立大学、米国ウィスコンシン大学が共同で実施し、日本医療研究開発機構(AMED)新興・再興感染症に対する革新的医薬品等開発推進研究事業(動物モデルと患者検体を用いた新型コロナウイルス感染症(COVID-19)の病態メカニズムの解明II)、新興・再興感染症研究基盤創生事業 (中国拠点を基軸とした新興・再興および輸入感染症制御に向けた基盤研究)ならびに、AMED SCARDAワクチン開発のための世界トップレベル研究開発拠点の形成事業 (ワクチン開発のための世界トップレベル研究開発拠点群 東京フラッグシップキャンパス(東京大学新世代感染症センター))の一環として行われました。
用語解説
(注)オミクロン株EG.5.1系統
ウイルス感染は、コロナウイルス粒子表面に存在するスパイク蛋白質を介してウイルス粒子が宿主細胞表面の受容体蛋白質に結合することで始まる。実用化されたあるいは開発中のCOVID-19に対する抗体薬は、このスパイク蛋白質を標的としており、その機能を失わせる(中和する)ことを目的としている。EG.5.1系統のスパイク蛋白質は、XBB.1.5系統と共通する変異(約40箇所)に加えて、3ヶ所の変異を有する。
問合せ先
〈研究に関する問合せ〉東京大学国際高等研究所 新世代感染症センター 機構長
東京大学医科学研究所 ウイルス感染部門 特任教授
河岡 義裕(かわおか よしひろ)
https://www.ims.u-tokyo.ac.jp/imsut/jp/lab/dstngprof/page_00174.html
〈報道に関する問合せ〉
東京大学新世代感染症センター(広報)
https://www.utopia.u-tokyo.ac.jp/
東京大学医科学研究所 プロジェクトコーディネーター室(広報)
https://www.ims.u-tokyo.ac.jp/
国立国際医療研究センター 企画戦略局 広報企画室
https://www.ncgm.go.jp/