東京大学医科学研究所 癌・細胞増殖部門 腫瘍抑制分野
教授:山梨 裕司
東京大学医科学研究所 癌・細胞増殖部門 腫瘍抑制分野
教授:山梨 裕司
Division of Genetics, The Institute of Medical Science, The University of Tokyo
腫瘍抑制分野 主な研究成果(2006年以降)

1.
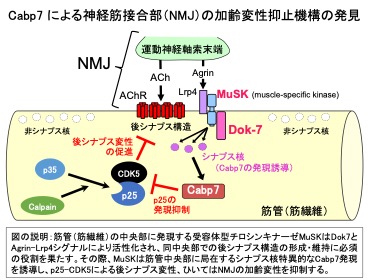
我々の運動機能には運動神経を介した骨格筋収縮の緻密な制御が必要であり、運動神経の軸索末端と、骨格筋の主要構成因子である筋管(筋繊維)の中央部に形成される後シナプス構造は神経筋接合部(NMJ:Neuromuscular Junction)と呼ばれる化学シナプス(神経筋シナプス)により結ばれている。当然のことながら、NMJの喪失は呼吸を含めた運動機能の喪失を意味する。我々は、このように重要なNMJの形成に不可欠のタンパク質としてDok-7を発見し(参考文献:英文原著12/和文総説7-10)、その劣性遺伝病としてNMJの形成不全病であるDOK7型筋無力症を発見した(参考文献:英文原著11)。さらに、DOK7発現ベクターの投与によるNMJ形成の増強(NMJの拡張)が、NMJ形成不全を呈するDOK7型筋無力症や常染色体優性エメリードレフュス型筋ジストロフィー(AD-EDMD)のモデルマウスに有効な治療戦略(NMJ形成増強治療)になることを実証した(参考文献:英文原著5)。近年、このようなNMJ形成不全との関連が、上記のDOK7型筋無力症やAD-EDMD等の筋原性疾患(ミオパチー)だけでなく、筋萎縮性側索硬化症(ALS)などの神経原性疾患(ニューロパチー)や加齢性の筋萎縮などにおいても報告されているが、その治療標的としての可能性については不明な部分が多い。
興味深いことに、哺乳動物のNMJ機能に必須の神経筋伝達物質であるアセチルコリン(図、ACh)の受容体(図、AChR)遺伝子やAChRが高密度に凝集するNMJの後シナプス構造、ひいてはNMJの形成・維持に必須のMUSK遺伝子などのNMJ関連遺伝子の多くは、多核細胞である筋管中央部のNMJ近傍に局在する少数の核(シナプス核)特異的に発現し、その発現はMuSK依存的であることが知られている(和文総説1)。そこで筋管中央部に特異的に高く発現し、Dok-7の強制発現によりその発現が顕著に亢進する遺伝子としてCabp7を単離し、それが加齢に伴うNMJ変性の抑制因子であることを発見した。さらに、Cabp7欠損マウスで促進される加齢性のNMJ変性、運動機能・筋力低下や筋萎縮が、当該マウスでの発現亢進を発見したp25によって活性化されるCdk5の阻害ペプチド(CIP:Cdk5 inhibitory peptide)の強制発現により回復することを発見した(原著論文1)。
本研究成果は、加齢性の運動機能低下に対する新たな抑制因子を発見すると共に、その知見に基づく分子標的治療の基礎となる知見を提示するものであり、高齢化社会における生活の質の向上に資する技術開発への発展が期待される。
2.
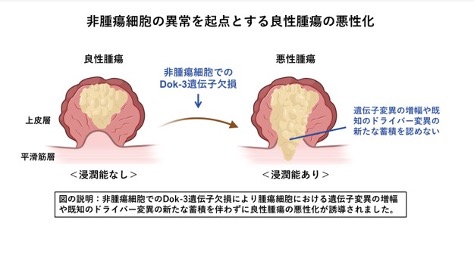
我々が同定したDok-1、Dok-7を含むDokファミリータンパク質のうち、Dok-1、Dok-2、Dok-3(Dok-1/-2/-3)から成るサブファミリーは、いわゆるアダプター分子として、免疫細胞におけるチロシンキナーゼシグナルを負に制御することが知られている(参考文献:英文総説3/和文総説11-14)。我々はこれまでにマウスDok-1/-2/-3ががん抑制遺伝子と機能することを報告しているが、それらの腫瘍悪性化における機能は不明であった。そこで腸管腫瘍の悪性化におけるDok-1/-2/-3の役割を明らかにすべく、良性腫瘍(腸管ポリープ)の自然発症モデルであるApcMin/+マウス(注1)に、Dokファミリー内で最も近縁なDok-1とDok-2の二重欠損、もしくは、Dok-3の単欠損を導入したところ、前者は腫瘍の増生を亢進させるのに対し、後者は腫瘍の増生に影響を与えず腫瘍の浸潤を誘導することが判明した(参考文献:英文原著2)。興味深いことに、Dok-3の発現は腫瘍上皮細胞では検出されず、また、この浸潤、つまり腫瘍悪性化の誘導は腫瘍細胞における遺伝子変異の増幅や多段階発がん説(注2)の根幹をなす新たなドライバー変異の蓄積を伴わないことが判明した。さらに、この腫瘍悪性化にはCD4陽性T細胞とCD8陽性T細胞が必須であると共に、異常な非腫瘍細胞であるDok-3欠損骨髄細胞の移植により再現できること、また、血球系細胞の腫瘍内浸潤等の炎症応答の亢進を伴わないことを解明した(参考文献:英文原著2)。
本研究成果は非腫瘍細胞に人為的な遺伝子変異を導入することで、良性腫瘍がその遺伝子変異の増幅や既知のドライバー変異の新たな蓄積を伴わずに浸潤能を獲得する、という全く新しい腫瘍悪性化機構の発見であり、当該分子機構の理解に基づく治療法開発への発展が期待される。
(注1) ApcMin/+マウス:ApcはWntシグナルに重要なシグナル伝達分子であるβ-カテニンの抑制因子であり、Apc遺伝子の機能欠失型変異は散発性のヒト大腸がんの約9割に認められています。ApcMinマウス/+はApc遺伝子の変異をヘテロに有するマウスであり、その対立遺伝子座欠失(loss of heterozygosity: LOH)によりWnt経路が活性化し、100%の個体が小腸及び大腸に良性腫瘍を発生する。
(注2) 多段階発がん説: 腫瘍形成やその悪性化を誘導する遺伝子の変異(ドライバー変異)の蓄積が腫瘍形成から悪性化の各段階を誘導するという概念。この概念が確立されている大腸がんでは、Apc遺伝子の不活性化により正常上皮細胞から良性腫瘍(腺腫)が発生し、Kras変異や p53変異などが加わることで悪性腫瘍(腺がん)に進展すると考えられている。
3.
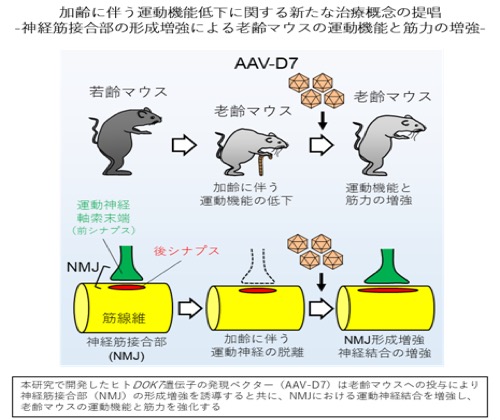
我々の運動機能には、運動神経を介した骨格筋収縮の緻密な制御が必要である。神経筋接合部(NMJ)は運動神経と骨格筋を結ぶ唯一の「絆」(神経筋シナプス)であり、その喪失は呼吸を含めた運動機能の喪失を意味する。我々は、これまでにNMJの形成に必須のタンパク質としてDok-7を(参考文献:英文原著13/和文総説7-10)、また、そのヒト遺伝子(DOK7)の遺伝病としてDOK7型筋無力症(参考文献:英文原著12)を発見した。さらに、マウスを用いた実験から、DOK7発現ベクターの投与によりNMJ形成を後天的に増強できることを発見し、そのような「NMJ形成増強治療」がDOK7型筋無力症だけでなく、ある種の筋ジストロフィーや筋委縮性側索硬化症を発症したマウスの運動機能を改善し、生存期間を延長することを実証した(参考文献:英文原著4,7)。以上の経緯をふまえ、我々は運動神経と骨格筋を結ぶNMJから運動神経が離れてしまう「神経脱離」が老化と共に進行することに着目し、NMJ形成増強治療による老齢マウスの運動機能に対する増強効果の研究を実施した。その結果、NMJでの運動神経脱離が進行し、運動機能が低下した老齢マウスにDOK7発現ベクターを投与することにより、1)NMJにおける運動神経結合の増強、2)運動神経刺激に対する骨格筋応答の増強、3)個体の運動機能と筋力の増強、を実証した(参考文献:英文原著3/和文総説1, 2)。この成果は、独自に開発したNMJ形成増強治療が、多様な要因により引き起こされる加齢性の運動機能低下に有効である可能性を提示するもので、高齢化社会における生活の質の向上に資する全く新しい医療技術としての発展が期待される。
4.
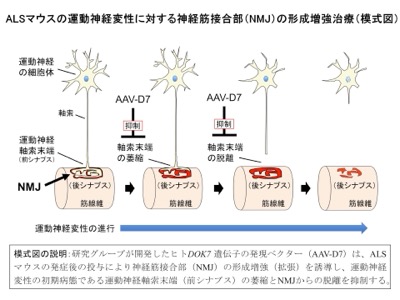
我々の運動機能には、運動神経を介した骨格筋収縮の緻密な制御が必要であり、両者は神経筋接合部(NMJ: Neuromuscular Junction)と呼ばれるシナプス(神経筋シナプス)により結ばれている(模式図、左端)。当然のことながら、NMJの喪失は呼吸を含めた運動機能の喪失を意味する。我々は、このように重要なNMJの形成に不可欠のタンパク質としてDok-7を発見し(参考文献:英文原著13/和文総説7-10)、その劣性遺伝病としてNMJの形成不全病であるDOK7型筋無力症を発見した(参考文献:英文原著12)。さらに、DOK7発現ベクターの投与によるNMJ形成の増強(NMJの拡張)が、NMJ形成不全を呈するDOK7型筋無力症や常染色体優性エメリードレフュス型筋ジストロフィー(AD-EDMD)のモデルマウスに有効な治療戦略(NMJ形成増強治療)になることを実証した(参考文献:英文原著7)。近年、このようなNMJ形成不全との関連が、上記のDOK7型筋無力症やAD-EDMD等の筋原性疾患(ミオパチー)だけでなく、筋萎縮性側索硬化症(ALS)などの神経原性疾患(ニューロパチー)や加齢性の筋萎縮などにおいても報告されているが、その治療標的としての可能性については不明な部分が多い。
以上の経緯を踏まえ、我々は現在に至るまで根本的な治療法が見出されていない運動神経変性疾患であるALSのモデルマウスを対象に、NMJ形成増強治療の有効性を検討した。具体的には、運動機能の低下を示したALSモデルマウスにDOK7発現ベクターを投与することで、1)NMJ形成不全(模式図に記載の運動神経軸索末端の萎縮とNMJからの脱離)の抑制、2)筋萎縮の抑制、3)運動機能の改善、4)生存期間の延長、を実証した(参考文献:英文原著4)。これらの成果は、独自に開発したNMJ形成増強治療が、根本的な治療法のないALSに対する新たな治療概念となり得ることを示す発見と言える。さらに、本研究の成果は、NMJ形成不全との関連が解き明かされつつある他の運動神経変性疾患や加齢性の筋萎縮に対する治療法の開発にもつながることが期待される。また、本研究はDOK7発現ベクターを用いた遺伝子治療だけでなく、化合物を用いたNMJ形成増強治療にも道を拓くべき「治療概念の実証研究」としての側面を有している。それ故、老齢マウスを含む様々な疾患モデル動物に対する有効性を検証すると共に、NMJ形成増強効果をもつ化合物の開発、さらには運動神経保護薬などのNMJ以外を標的とする他の薬剤との併用治療に関する研究の推進が求められる。
5.
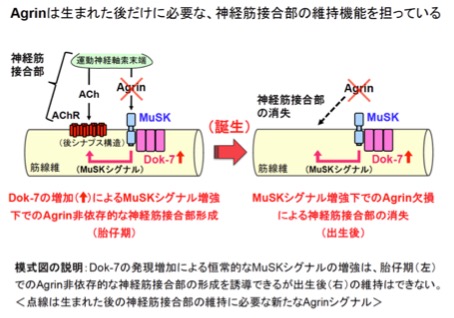
我々の運動機能には、運動神経を介した骨格筋収縮の緻密な制御が必要であり、両者は神経筋接合部(NMJ:Neuromuscular Junction)と呼ばれるシナプス(神経筋シナプス)により結ばれている。当然のことながら、NMJの喪失は呼吸を含めた運動機能の喪失を意味する。我々は、このように重要なNMJの形成に不可欠のタンパク質としてDok-7を発見し(参考文献:英文原著13/和文総説7-10)、その劣性遺伝病としてNMJの形成不全病であるDOK7型筋無力症を発見した(参考文献:英文原著12)。さらに、最近、神経筋接合部の形成不全を伴う様々な疾患に対する治療法として、DOK7発現ベクターの投与による「神経筋接合部の形成増強治療」をマウスにおいて創出した(参考文献:英文原著7)。
他方、我々はDok-7がMuSKというタンパク質(リン酸化酵素)を活性化することで神経筋接合部を形成することも解明しているが(参考文献:英文原著11/和文総説4-6)、MuSKにはAgrinと言う別の活性化因子の存在が古くから知られており、両者の違いは未解明であった。そこで、今回、Dok-7を多量に産生することでMuSKの活性化を恒常的に増強するマウスを作出し、そのマウスにAgrin欠損を導入したところ、胎仔期に形成された神経筋接合部が誕生後の数週間で消失してしまうことが判明した(模式図)。この事実は、胎仔期のAgrin機能がDok-7の発現増強によるMuSKの活性化で補えるのに対して、生まれた後のAgrinはMuSK活性化以外の、Dok-7では代替不可能な仕組みで神経筋接合部を守っていることを意味する(参考文献:英文原著6)。以上の成果は、我々が母体内で形成した神経筋接合部をどのようにして維持しているのかを理解するための鍵となる知見であり、また、その多くが生まれた後に発症する多様な神経・筋疾患の理解や制御につながる発見と言える。
6.
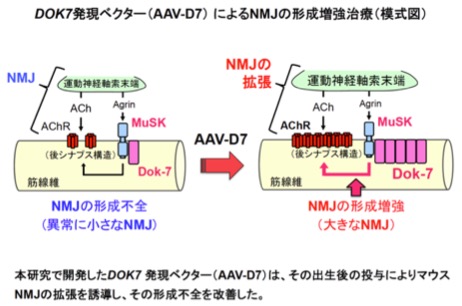
我々の運動機能には、運動神経を介した骨格筋収縮の緻密な制御が必要であり、両者は神経筋接合部(NMJ:Neuromuscular Junction)と呼ばれるシナプス(神経筋シナプス)により結ばれている。当然のことながら、NMJの喪失は呼吸を含めた運動機能の喪失を意味する。我々は、このように重要なNMJの形成に不可欠のタンパク質としてDok-7を発見し(参考文献:英文原著13/和文総説7-10)、その劣性遺伝病としてNMJの形成不全病であるDOK7型筋無力症を発見した(参考文献:英文原著12)。そこで、NMJの形成不全を伴う神経筋疾患に関する情報を広く検討したところ、NMJ疾患として知られる筋無力症の枠を超え、筋ジストロフィー、筋萎縮性側索硬化症(ALS)、脊髄性筋萎縮症(SMA)や加齢性筋肉減少症(Sarcopenia)などの多様な神経筋疾患にもNMJの形成不全が認められることに気づいた。これらの知見を踏まえ、我々はDok-7タンパク質の人為的な発現増強による「NMJ形成増強治療の創出」、つまり「小さくなってしまったNMJを大きくする治療の創出」を進めた(参考文献:英文原著7/和文総説3)。Dok-7の発現増強の手法としては、ヒト骨格筋での安全、かつ、長期にわたる外来遺伝子発現に優れたアデノ随伴ウイルス(AAV: adeno- associated virus)を選び、Dok-7発現ベクター(AAV-D7)を作成した。その上で、AAV-D7をDOK7型筋無力症モデルマウスの発症後に投与したところ、形成不全を呈するNMJの拡張、運動機能の改善、早期致死性の回避をもたらした。さらに、DOK7遺伝子そのものではなく、核内分子をコードするLMNA遺伝子の異常によるエメリードレフュス型筋ジストロフィー(AD-EDMD: autosomal dominant Emery-Dreifuss muscular dystrophy)のモデルマウスに対しても、AAV-D7の発症後の投与はNMJの拡張、運動機能の改善、延命効果をもたらした。以上の成果は、1)哺乳動物のNMJを後天的、人為的、かつ安全に拡張する方法の創出と、2)NMJの形成不全を伴う多様な神経筋疾患に対する新規治療概念の確立を意味するものである。
7.
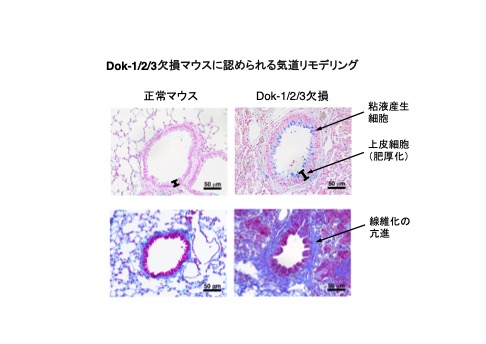
我々の生命活動に必須の呼吸機能は、骨格筋の収縮・弛緩が生み出す適切な気流の維持によって支えられている。それ故に、仮に骨格筋機能が正常であったとしても、気道構造の変化(リモデリング)による気流の障害は重篤な疾病の原因となる。喘息は肺組織の慢性的な炎症による気流障害を伴う呼吸器疾患であり、炎症性サイトカインの産生を伴う気道リモデリングや気道過敏性を特徴とする。今回、我々はDok-1/2/3欠損マウスが特定のアレルギー刺激の非存在下に気道過敏性の亢進や気道リモデリングを伴う喘息様病態を呈することを明らかにした(参考文献:英文原著9)。例えば、Dok-1/2/3欠損マウスの気道(細気管支)ではアルシアンブルーにより染色(青色)される粘液産生細胞の増多と気道上皮の肥厚が示されている(図の上段、矢印)。また、マッソントリクローム染色により染色(青色)される線維化の亢進も明らかにされている(下段、矢印)。以上の知見はDok-1/2/3が協調的に気道リモデリングや気道過敏性の亢進による気流障害の抑制に機能していることを示している。
8.
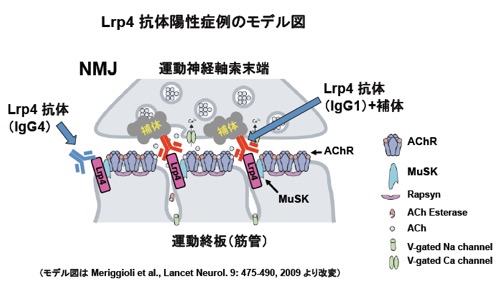
重症筋無力症(Myasthenia Gravis)は異常な自己抗体によって発症する疾患であり、骨格筋収縮に必須のシナプスである神経筋接合部(NMJ)の構造・機能不全による筋力低下と易疲労性を伴う難病である。その多くは、NMJの筋管側に局在するアセチルコリン受容体(AChR)に対する抗体をもつが、同じくNMJの筋管側に局在するMuSKに対する抗体をもつ症例も報告されている。これらの自己抗体は、補体を介したNMJの破壊や標的分子の機能阻害によって筋無力症を惹起すると理解されている。今回、我々は重症筋無力症の新たな病原性自己抗体として抗 Lrp4 抗体を発見し、AChRやMuSK抗体を持たない症例に対する診断・治療法への道を拓いた(参考文献:英文原著10)。上記のモデル図に記載の通り、抗Lrp4抗体の多くは補体の活性化による組織破壊能をもつIgG1であると共に、NMJの形成・維持に必須のLrp4とその活性化因子(Agrin)との結合を阻害する活性をもつ自己抗体である。
9.
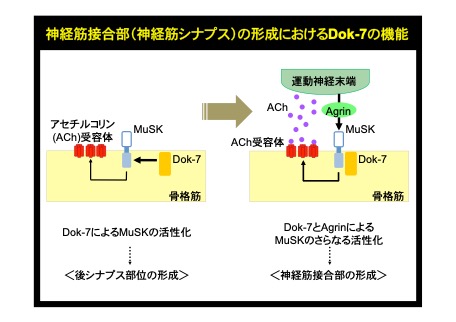
これまでの研究によって、我々は神経筋接合部の形成に必須のタンパク質としてDok-7を同定し、ヒトDOK7遺伝子の異常によって神経筋接合部の形成不全を伴う筋無力症(DOK7型筋無力症)が発症することを明らかにしている(参考文献:英文原著12、13/和文総説7-10)。しかしながら、Dok-7がどの様な動作原理の下で神経筋接合部の形成に機能しているかについては不明な部分が多く、治療法開発の基盤となる情報が求められていた。今回、我々はDok-7が神経筋接合部の形成を司るMuSKと言う受容体型チロシンキナーゼに直接、細胞内から働きかける筋内在の活性化因子であり、Dok-7を失った筋管ではMuSKが活性化されないことを解明した。さらに、このDok-7シグナルを人為的に増強することでマウスにおける神経筋接合部の形成が促進されることも明らかにした。これらの知見は、DOK7型筋無力症やMuSKの機能低下を伴う筋無力症の治療法開発にむけた手がかりとなるべき重要な情報であり、また、受容体型チロシンキナーゼが細胞外からの刺激を細胞内シグナルに変換すると言う原則に従わない、全く新しいシグナル制御機構の発見として、高度の学術的な意義をもつ(参考文献:英文原著11<当該号の表紙は本論文に関する顕微鏡写真です>/英文総説2/和文総説4-6)。事実、最近、受容体型チロシンキナーゼの2例目の細胞内活性化因子としてcytohesinが同定され、その機能阻害が標的PTKであるErbBに依存的な癌細胞の増殖を個体レベルで抑制することが報告されている(Cell, 143: 201-211, 2010)。
10.
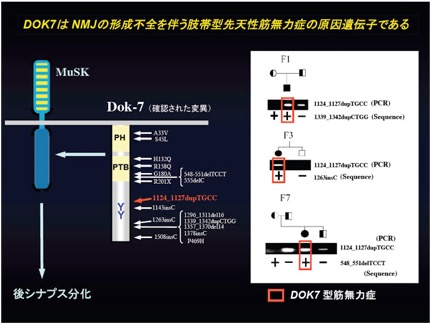
David Beeson教授らの症例についてdok-7遺伝子変異を探索したところ、その両アレル性の異常が神経筋接合部(NMJ)の形成不全を伴う先天性筋無力症候群の発症と一致することが判明した(右パネル)。また、最も多くの症例に認められるC末端欠失変異(1124_1127dupTGCC)がDok-7による後シナプス構造の誘導機能を著しく減弱させることも明らかとなった。これらの知見から、dok-7がNMJ形成不全型CMS(DOK7型筋無力症)の原因遺伝子であると結論された(参考文献:英文原著12/和文総説8-10)。
11.
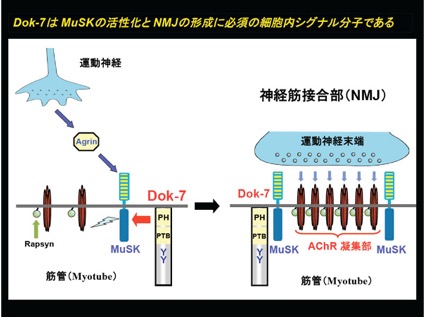
我々がDokファミリー分子の新たなメンバーとして単離したDok-7は、骨格筋収縮の運動神経支配に必須のシナプスである神経筋接合部(NMJ: Neuromuscular Junction)の後シナプス部位に局在し、受容体型チロシンキナーゼであるMuSKの活性化に必須の役割を担っている。MuSKの機能が神経筋接合部の後シナプス部位の形成に不可欠であることを考えると、この研究成果は、運動神経由来のAgrinと筋内在のDok-7によるMuSKの強い活性化がNMJの形成に必須であることを意味している。事実、我々が世界に先駆けて樹立したDok-7欠損マウスは神経筋接合部を欠き、呼吸を含めた運動機能の欠損を呈した(参考文献:英文原著13/和文総説8-10)。
[参考文献]
英文原著(各論文の詳細は主要原著論文リストを御覧下さい)
1.iScience: 27, 108997, 2024
2.Cancer Res. Commun. 2: 1590-1600, 2022
3.iScience: 23, 101385, 2020
4.EMBO Mol. Med, 9: 880-889, 2017
5.Biochem. Biophys. Res. Commun.: 478, 135-142, 2016
6.Proc. Natl. Acad. Sci. USA.: 111, 16556-16561, 2014
7.Science: 345, 1505-1508, 2014
8.FEBS Lett.: 587, 3749-3754, 2013
9.Genes Cells: 18, 56-65, 2013
10.Annals of Neurology: 69, 418-422, 2011
11.Science Signaling: 2, ra7, 2009
12.Science: 313, 1975-1978, 2006
13.Science: 312, 1802-1805, 2006
14.J. Exp. Med.: 201, 333-339, 2005
15.J. Exp. Med.: 200, 1681-1687, 2004
16.Genes & Development:14, 11-16, 2000
17.Cell: 88, 205-211, 1997
18.Science: 251, 192-194, 1991
英文総説
1.“Molecular signaling and its pathogenic alterations in neuromuscular junction formation and maintenance” in “Protein
?Modification in Pathogenic Dysregulation of Signaling (Springer)”: 309-325, 2015
2.J. Biochem. : 151, 353-359, 2012
3.Immunol. Reviews: 232, 273-285, 2009
和文総説
1.BRAIN and NERVE「神経筋接合部(NMJ)の形成・維持シグナルとNMJ標的治療の開発」: 76, 61-67, 2024
2.生体の化学 72巻6号「神経筋接合部(NMJ)の形成・維持メカニズムーNMJを標的とした治療技術の開発を目指して」:
pp527-531, 2021
3.実験医学3月号「神経筋接合部の形成不全を伴う神経筋疾患に対する新規治療概念の創出」: p603-606, 2015
4.実験医学増刊「シグナル伝達研究の最前線2012-’13」: 30, 740-745, 2012
5.生体の科学4月号「先天性筋無力症の分子基盤」: 62, 106-111, 2011
6.実験医学「受容体型キナーゼの細胞内からの活性化:Dok-7による神経筋シナプス形成の分子機構」: p1384-1387, 2009
7.実験医学増刊「シグナル伝達研究2008-‘09」: 26, 103-110, 2008
8.Clinical Neuroscience「神経筋接合部の分子構築」: 26, 962-963, 2008
9.細胞工学6月号「神経筋シナプス形成と筋無力症におけるDok-7/MuSKシグナル」: p674-678, 2007
10.実験医学10月号「神経筋シナプスの形成におけるDok-7の役割:細胞内因子による受容体型キナーゼの活性化」:
p2517-2520, 2006
11.Molecular Medicine増刊「免疫2006」: 42, 230-237, 2005
12.実験医学増刊「シグナル伝達研究2005-‘06」: 23, 39-47, 2005
13.実験医学4月号「血球の恒常性とDok-1/2の新たな機能」: p1126-1132, 2005
14.キーワードで理解するシグナル伝達イラストマップ: p18-20, p84-94, 2004